Nat Commun :卫涛涛研究组合作揭示Gabija复合物抗噬菌体侵染的分子机理
来源:生物探索 2024-02-01 13:28
本研究报道了Gabija八聚体复合物的结构,阐明了Gabija系统发挥免疫防御作用的分子机制。
中国科学院生物物理研究所卫涛涛研究组联合深圳湾实验室马军研究组及生物物理研究所章新政、许文青研究组在Nature Communications(IF 16.6)发表了题为Structural and biochemical insights into the mechanism of the Gabija bacterial immunity system的研究论文,报道了Gabija八聚体复合物的结构,阐明了Gabija系统发挥免疫防御作用的分子机制。
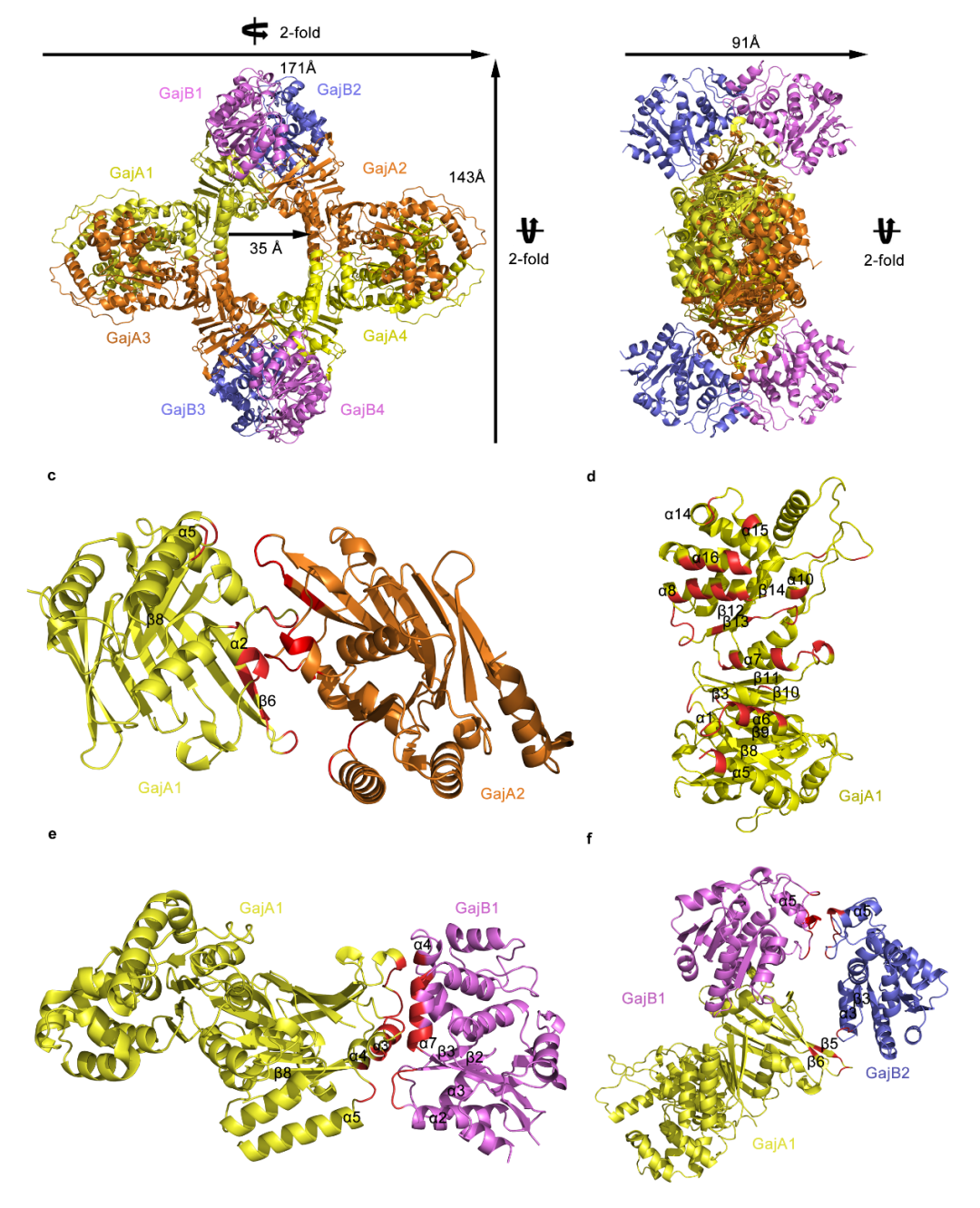
图1 Gabija复合物八聚体结构(Credit: Nature Communications)
Gabija复合物是由四个GajA蛋白和四个GajB蛋白组成的八聚体(图 1)。GajA蛋白首先形成四聚体,构筑Gabija复合物核心组件;四个GajB蛋白分别以单体的形式结合在复合物的外周。大肠杆菌抗噬菌体侵染实验证明,在细菌中单独表达GajA蛋白或GajB蛋白均无法抵抗噬菌体的入侵,而破坏GajA蛋白和GajB蛋白的相互作用界面也明显减弱Gabija复合物的抗噬菌体功能,提示4:4 组装的GajA/B复合物对抵御噬菌体至关重要。

该研究还发现Gabija复合物具有序列特异性的DNA内切酶活性,并更倾向于选择环状DNA作为底物,且其内切酶活性对核苷酸浓度的响应比单独的GajA蛋白更敏感。GajB蛋白中ATP酶结构域关键位点的突变能够解除核苷酸对于Gabija复合物DNA内切酶活性的抑制,提示GajB可作为细胞能量状态的感受器,通过响应胞内核苷酸的浓度,精确调节GajA蛋白的核酸酶活性。基于冷冻电镜结构解析及生化实验,该研究提出了Gabija免疫系统发挥抗病毒作用的模型:在正常生理状态下,细胞内的NTP和dNTP浓度较高,抑制了Gabija复合物的核酸内切酶活性;而在噬菌体入侵、病毒DNA高强度复制和转录时,细胞内的NTP和dNTP耗竭,迅速激活Gabija复合物,该复合物首先切割环状DNA以抑制噬菌体DNA复制,进而阻断噬菌体扩增。
该项研究被Nature Communications编辑遴选为Featured Article,并作为Editors’ Highlights推荐。在该项研究投稿及修稿期间,哈佛大学Philip Kranzusch团队向bioRxiv 、俄亥俄州立大学的Tianmin Fu团队向Research Square提交了预印本,分别独立报道了Gabija复合物的结构,其中Philip Kranzusch的工作于2024年1月11日在Nature以“加速预览”的形式发表。这些工作共同揭示了Gabija系统感知噬菌体入侵的分子机制及其切割DNA底物的偏好选择,并为探索宿主抗噬菌体免疫及噬菌体免疫逃逸的“军备竞赛”提供了新的研究方向。此外,Gabija系统也有望为分子生物学工具酶的研发提供重要的结构和生化基础。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


