北京大学姜长涛团队最新Cell论文揭示新型菌源胆汁酸调控血糖的新机制
来源:生物世界 2025-06-01 09:30
该研究发现了一种促进 GLP-1 分泌的新机制。
近来,在人类样本中发现,微生物来源的氨基酸结合型胆汁酸(amino-acid-conjugated bile acid,MABA)普遍存在。这是一类由肠道微生物利用多种氨基酸对胆汁酸进行共价修饰所形成的新型胆汁酸。然而,它们的生理意义尚不清楚,是否存在新受体也有待探索。
2025 年 5 月 29 日,北京大学姜长涛团队等在国际顶尖学术期刊 Cell 上发表了题为:A microbial amino-acid-conjugated bile acid, tryptophan-cholic acid, improves glucose homeostasis via the orphan receptor MRGPRE 的研究论文,这是 2025 年 姜长涛作为通讯作者发表的第四篇 Cell、Nature、Science 正刊论文。
该研究发现了一种新型胆汁酸受体——MRGPRE,能够被肠道细菌来源的氨基酸结合型胆汁酸——色氨酸胆酸(Trp-CA)特异性激活,揭示了 Trp-CA 发挥血糖调控的作用和机制,深入解析了 Trp-CA 激活 MRGPRE 通过 β-arrestin-1-ALDOA 磷酸化促进 GLP-1 分泌的新机制。
这项研究为新型菌源胆汁酸功能以及作用机制的解析提供了新范式,也为2 型糖尿病等代谢疾病的药物开发提供了新靶点和新策略。

在这项最新研究中,研究团队确定了色氨酸胆酸(Trp-CA)是 2 型糖尿病(T2D)患者中最显著减少的氨基酸结合型胆汁酸(MABA),而且其丰度与临床血糖指标呈负相关。研究团队进一步证明,色氨酸胆酸(Trp-CA)可改善糖尿病小鼠的葡萄糖耐量。
传统胆汁酸通过胆汁酸受体 FXR、TGR5 来发挥作用,而该研究显示,色氨酸胆酸(Trp-CA)并不激活这些传统的胆汁酸受体,而是特异性激活一种孤儿 G 蛋白偶联受体(GPCR)——MRGPRE,并通过冷冻电镜确定了二者之间的结合模式——色氨酸基团嵌入受体蛋白口袋形成 π-π 堆叠,胆酸羟基与受体蛋白关键氨基酸建立氢键网络。值得一提的是,MRGPRE 属于痒觉受体家族,而该研究显示,其并不激活瘙痒。
研究团队进一步揭示了色氨酸胆酸(Trp-CA)发挥血糖调控作用的机制——Trp-CA 通过 MRGPRE-Gs-cAMP 信号通路和 MRGPRE-β-arrestin-1-ALDOA 通路共同促进了 GLP-1 的分泌。而众所周知,GLP-1 能够促进胰岛素分泌,发挥降血糖作用。
在上述发现的基础上,研究团队从肠道共生菌中筛选到了一个动物双歧乳杆菌亚种(B. animalis subsp. lactis),具有最高的 Trp-CA 产量,其特有的 BSH/T 酶可催化生成 Trp-CA,定殖该细菌或表达 BSH/T 基因的大肠杆菌,都能够显著改善小鼠的葡萄糖耐量异常。
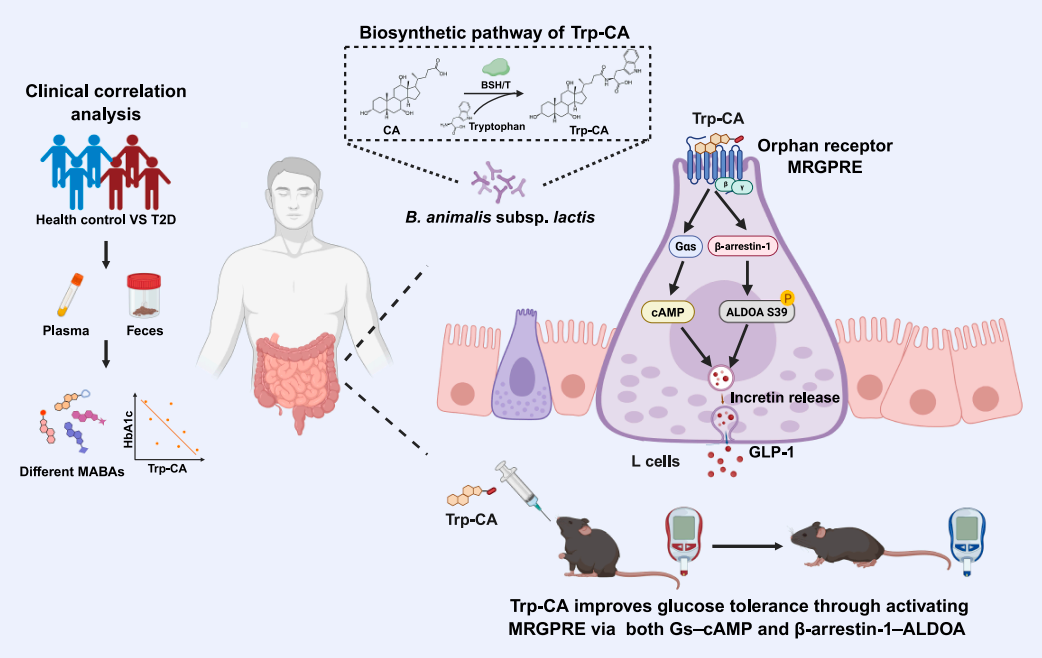
总的来说,该研究发现并证实了 Trp-CA 是孤儿受体 MRGPRE 的内源性配体,并解析了其通过两种机制调控 GLP-1 分泌,其中,MRGPRE-β-arrestin-1-ALDOA 是此前未知的调控 GLP-1 分泌的新机制。此外,Trp-CA 不会引起传统胆汁酸的副作用——瘙痒。
这些发现不仅揭示了肠道菌群合成氨基酸结合型胆汁酸(MABA)的生理意义,为进一步研究 MABA 铺平了道路,还为开发无瘙痒副作用的新型降糖药物提供了新靶点和新策略。
北京大学姜长涛教授、山东大学孙金鹏教授、北京大学庞艳莉研究员、纪立农教授以及山东大学于晓教授为该论文共同通讯作者。北京大学博士后林骏、聂启兴,山东大学程杰研究员,博士研究生钟亚妮、张天瑶,北京大学副主任医师张秀英,山东大学博士后葛晓燕,及北京大学博士后丁勇为共同第一作者。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


