Cell:肾脏足细胞的“断臂求生”!研究发现膜性肾病排毒新机制
来源:iNature 2025-12-07 11:46
该研究表明,这些自身抗体在足细胞FP质膜上触发抗原-自身抗体聚集体的形成。这些聚集体形成茎状囊泡,称为自身免疫球蛋白触发的细胞外囊泡(AIT-EVs),释放到尿液中。
全世界每10个人中就有1个人患有慢性肾脏疾病,肾脏中被称为足细胞的特殊血液过滤细胞的损伤起着至关重要的作用。膜性肾病(MN)是肾病综合征的主要原因,循环自身抗体攻击足细胞足突(FPs)上的蛋白质,破坏肾脏的滤过屏障。
2025年12月4日,德国汉堡大学Catherine Meyer-Schwesinger团队在Cell 在线发表题为“Autoantibody-triggered podocyte membrane budding drives autoimmune kidney disease”的研究论文,该研究表明,这些自身抗体在足细胞FP质膜上触发抗原-自身抗体聚集体的形成。这些聚集体形成茎状囊泡,称为自身免疫球蛋白触发的细胞外囊泡(AIT-EVs),释放到尿液中。
AIT-EVs携带致病自身抗体、它们的靶抗原、必需FP蛋白和疾病相关应激源,这些应激源代表了清除免疫复合物(IC)和废物的机制。然而,它们的过量释放会导致FP消失和足细胞功能障碍。在MN患者中,尿AIT-EVs对应于肾小球尿腔聚集物。富集AIT-EVs可以检测和监测病原性自身抗体,为自身免疫性肾脏疾病的诊断和治疗提供了一种无创方法。

肾脏疾病的发病率正在增加,演变为健康危机,迫切需要采取措施来预防、识别和治疗潜在的原因。肾小球损伤是慢性肾脏疾病最常见的原因之一。随着针对基本肾小球结构的自身抗体发现的增加,自身免疫介导的肾脏疾病病因的鉴定正在稳步上升。膜性肾病(MN)是一种肾小球足细胞的自身免疫性疾病,是肾病综合征的最常见原因,肾病综合征是一种重蛋白尿、水肿和高脂血症的临床症状。足细胞与肾小球内皮细胞和肾小球基底膜(GBM)一起对滤过屏障的形成至关重要。
足细胞通过其错综复杂的主突和足突(MP和FPs)网络从泌尿侧包裹肾小球毛细血管。FPs通过狭缝隔膜(SDs)相互连接,这是一种细胞-细胞连接点,其独特的蛋白质网络动态调节过滤。在MN中,循环自身抗体针对足细胞FP型-1跨膜蛋白的胞外结构域,如80%的M型磷脂酶A2受体(PLA2R1)和5%的血栓反应蛋白1型结构域7A (THSD7A)等。根据临床观察,自身免疫的多种原因可能驱动MN,正如最近发现的大量潜在MN自身抗原所反映的那样。
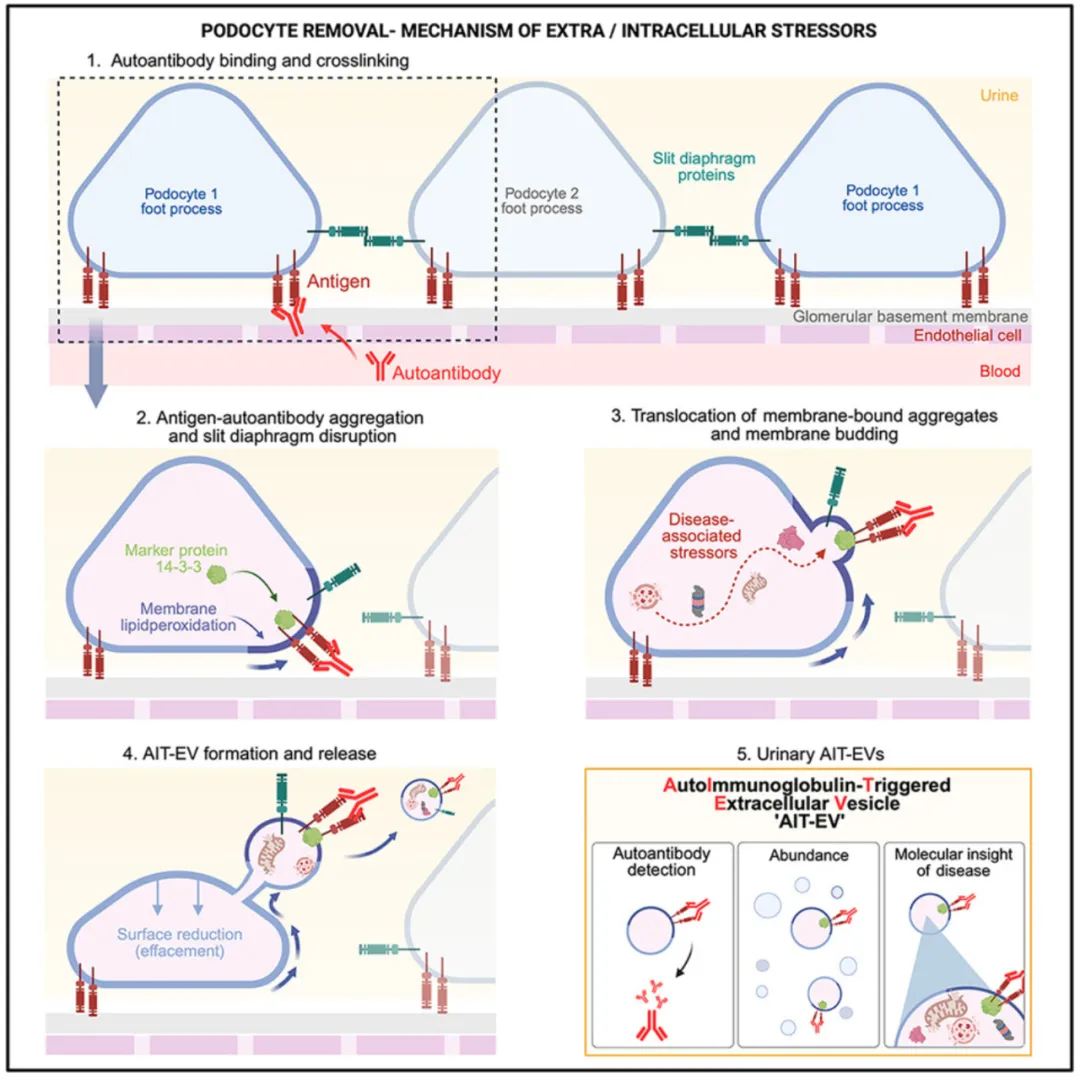
文章模式图(图源自Cell )
在目前对MN的认识中,循环中的自身抗体主要是人免疫球蛋白G型4 (huIgG4)类,它们与FPs底部各自的抗原结合,最初在靠近SD的地方,通过补体依赖和独立的机制引起疾病。随后在滤过屏障处的自身抗体-抗原反应导致它们在上皮下间隙(足细胞FP和GBM之间的间隙)内以免疫复合物(IC)的形式在肾小球内沉积,最终导致滤过屏障改变,足细胞FP表面积损失(消退)和肾范围蛋白尿。肾小球聚集形成和自身抗体结合下游沉积的潜在足细胞机制和临床意义尚不清楚。讨论的后遗症,如蛋白水解抗原脱落与上皮下沉积或抗原-自身抗体内化与足细胞降解受损仍有待证实。此外,在过去的几年中,已经发现许多蛋白质在MN患者的肾小球内积聚,具有未知的疾病意义。
该研究发现自身免疫球蛋白触发的细胞外囊泡(AIT-EVs)的形成是足细胞质膜出芽的病理生物学标志,这是由足细胞试图消除与FP跨膜抗原结合的致病自身抗体引起的。AIT-EVs将IC从上皮下空间去除和足细胞FP清除联系起来,并为MN异型肾小球蛋白积累提供了统一的、保守的机制。尿AIT-EVs分析是一种非侵入性的诊断工具,可以灵敏地检测和监测患者的肾脏自身免疫活性。
参考消息:
https://www.cell.com/cell/fulltext/S0092-8674(25)01306-6
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


