International Journal of Oral Science: 牙干细胞来源的细胞外囊泡转移miR-330-5p治疗外伤性脑损伤
来源:生物谷原创 2022-09-23 17:12
创伤性脑损伤(TBI)被认为是人群发病和死亡的常见原因,已成为负担全球卫生的一个主要因素。
创伤性脑损伤(TBI)被认为是人群发病和死亡的常见原因,已成为负担全球卫生的一个主要因素。到目前为止,尽管对症干预,如手术和药物给药在TBI的治疗中发挥着重要作用,但在改变预后方面的总体疗效仍存在争议。
越来越多的证据表明,基于干细胞的治疗为TBI的功能恢复提供了新的线索。其中,牙源性间充质干细胞(DSCs)因其固有的神经源性潜能而具有广阔的应用前景。研究表明,DSCs有助于TBI的精神和身体功能恢复。值得注意的是,DSCs分泌的细胞外囊泡(EV)被认为是治疗效应。

图片来源: https://doi.org/10.1038/s41368-022-00191-3
近日,来自西安交通大学的研究者们在International Journal of Oral Science杂志上发表了题为“Dental stem cell-derived extracellular vesicles transfer miR-330-5p to treat traumatic brain injury by regulating microglia polarization”的文章,该研究揭示了通过转移miR-330-5p, SHED-EVs调控Ehmt2介导的CXCL14转录促进抗炎小胶质细胞极化,从而治疗创伤性脑损伤。
创伤性脑损伤(TBI)是导致神经功能缺损的关键因素。然而,目前还没有开发出有效的治疗方法。在研究者之前的工作中,由人脱落乳牙(SHED)干细胞分泌的细胞外囊泡(EVs)为TBI功能恢复提供了新的见解。
本研究旨在阐明其作用机制,为未来的临床干预提供新的治疗靶点。随着miRNA阵列的完成和Real-time PCR的验证,研究者揭示了由shed衍生ev (shed - ev)转移的miR-330-5p在调节中枢神经系统的关键免疫调节剂小胶质细胞中的重要作用。
MiR-330-5p靶向Ehmt2,并介导CXCL14的转录,促进M2小胶质细胞极化,抑制M1极化。在本研究的体内数据中发现,shed - ev及其效应子miR-330-5p可以缓解炎症细胞因子的分泌,恢复TBI大鼠的运动功能恢复。
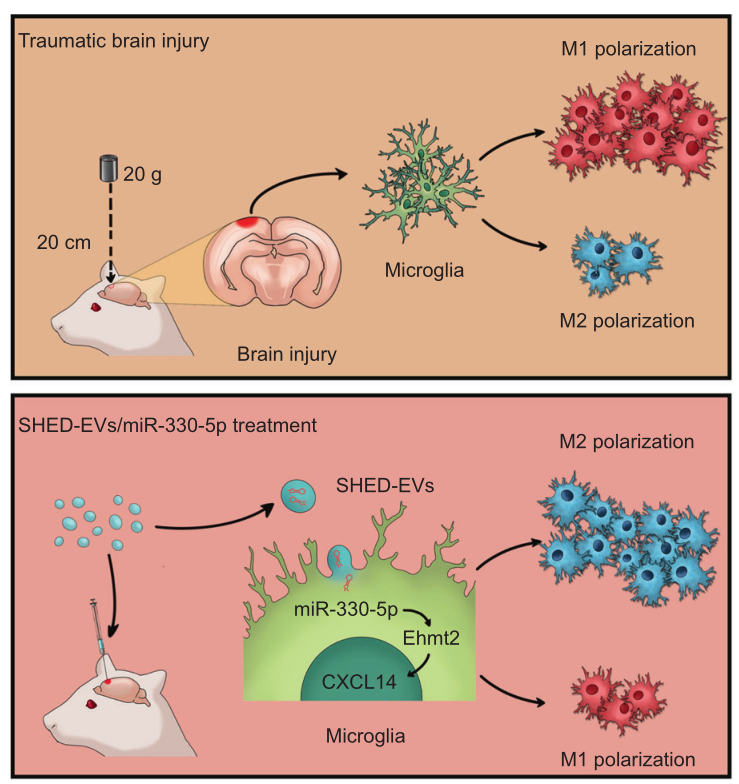
SHED-EVs/miR-330-5p治疗TBI的机制图
图片来源: https://doi.org/10.1038/s41368-022-00191-3
综上所述,目前的研究表明,从SHED - ev转移的miR-330-5p挽救了TBI导致的运动功能损伤。从机制的角度来看,SHED-EVs/miR-330-5p通过靶向Ehmt2-H3K9me2介导的CXCL14转录来改变小胶质细胞的极化,从而减轻神经炎症和增强脑损伤的修复。(生物谷 Bioon.com)
参考文献
Ye Li et al. Dental stem cell-derived extracellular vesicles transfer miR-330-5p to treat traumatic brain injury by regulating microglia polarization. Int J Oral Sci. 2022 Sep 5;14(1):44. doi: 10.1038/s41368-022-00191-3.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


