艾赛普生物泛肿瘤荧光显像剂创新药物iSAP-0909再获中国临床试验许可,开启肿瘤精准诊疗新征程
来源:医药魔方 2025-03-09 15:58
此次中国临床试验获批,标志着iSAP-0909在全球同步开发中迈出关键一步,为填补国内肿瘤术中精准导航技术空白提供创新的解决方案,同时加速中国创新药在全球范围内的转化应用。
艾赛普(北京)生物科技有限公司(以下简称“艾赛普生物”)宣布,其领先品种注射用iSAP-0909在获得美国FDA临床试验许可后,又正式获得中国国家药品监督管理局(NMPA)的临床试验默示许可(受理号:CXHL2401438),拟开展针对非肌层浸润性膀胱癌(NMIBC)辅助诊断与术中定位的临床试验。此次中国临床试验获批,标志着iSAP-0909在全球同步开发中迈出关键一步,为填补国内肿瘤术中精准导航技术空白提供创新的解决方案,同时加速中国创新药在全球范围内的转化应用。
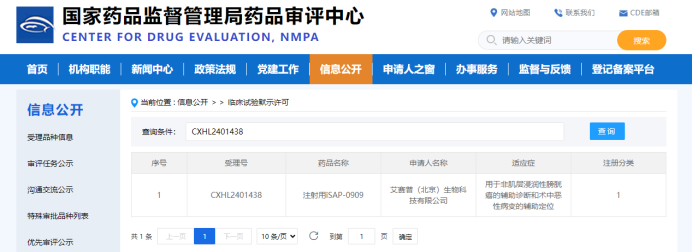
截图来源:CDE官网
iSAP-0909是艾赛普生物基于“体内原位自组装”纳米生物技术平台开发的首个创新药品种,具备高特异性、高灵敏性及长时稳定高亮成像的临床优势。临床前研究显示,iSAP-0909利用肿瘤细胞内的组装诱导滞留效应(AIR)实现荧光分子在肿瘤组织的高效富集与滞留,显著提升肿瘤成像的精准度与稳定性。iSAP-0909的高特异性可视化荧光成像技术,能够改变基于二维影像学诊断的传统诊疗模式,从分子、细胞层面解决肿瘤边界的界定、微小病灶的显示、淋巴结是否转移、切除断面是否存在残留病灶等临床问题。目前,该药物已获美国FDA及中国NMPA的双IND临床默认许可,标志着iSAP-0909正式进入全球同步开发的新阶段。
除已经获得批准的非肌层浸润性膀胱癌辅助诊断与术中定位的适应症之外,艾赛普生物正在联合多家医疗机构探索iSAP-0909在其他实体瘤术中导航中的可行性,未来或可覆盖超百万肿瘤患者的精准手术需求,市场前景广阔。
艾赛普生物CEO吕甘田博士表示,继去年10月该产品获批美国临床试验,成为全球第二款进入临床阶段的泛肿瘤靶向荧光显像剂,非常高兴此次又完成中国临床试验批准这一重要里程碑。这一阶段性里程碑也证明了艾赛普生物团队卓越的执行力和专业能力。艾赛普生物将继续推进“体内原位自组装”多肽偶联药物的设计与研发,为全球患者提供更精准、更有效、更安全的用药选择。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


