Cell子刊:鲍岚团队揭示m6A修饰lncRNA调控神经发育的分子机制
来源:生物世界 2022-11-23 19:28
本研究揭示了神经元发育中lncRNA的m6A动态修饰通过稳定RNA结合蛋白调控mRNA翻译的功能。该研究加深了对于非编码RNA上m6A动态修饰功能和机制的理解
神经元作为一类高度特化的细胞,具有复杂的树突和轴突。神经元胞体中的mRNA可以运输至树突和轴突,并通过mRNA局部动态翻译合成新蛋白从而调控神经元发育以及神经网络的正确建立。鲍岚课题组前期的研究工作发现,初级感觉神经元轴突中富集miRNAs,同时通过调控轴突中的局部翻译并参与轴突延伸。最近的研究发现,轴突富集的lncRNA ALAE通过竞争RNA结合蛋白KHSRP并与Gap43 mRNA相互作用从而调节轴突局部翻译和轴突生长。以上的研究表明,非编码RNA在神经元的发育中发挥重要调控作用。
2022年11月22日,中国科学院分子细胞科学卓越创新中心(生物化学与细胞生物学研究所)鲍岚研究组在 Cell Reports 期刊在线发表了题为:m6A-modified lincRNA Dubr is required for neuronal development by stabilizing YTHDF1/3 and facilitating mRNA translation 的研究论文。
该研究揭示长链非编码RNA(lncRNA)Dubr 的m6A修饰通过稳定YTHDF1/3复合体及其介导的mRNA翻译从而调控神经元轴突生长和迁移的分子机制。

RNA甲基化修饰是数百种RNA修饰中最普遍和富集的修饰。N6-腺苷酸甲基化(N6-methyladenosine,m6A)是其中丰度最高的动态修饰,参与RNA代谢、剪接、翻译、出核和运输等重要细胞生物学过程。已有的研究表明,m6A甲基化修饰在哺乳动物大脑中高度富集,在早期神经元发育以及学习记忆等方面都发挥重要作用。
最近的研究提示lncRNA调控神经元轴突发育,但lncRNA是否存在m6A修饰以及m6A修饰在lncRNA参与神经元发育中的功能和作用机制知之甚少。
该研究首先对小鼠背根神经节(DRG)组织中的m6A-CLIP和不同组织发育测序的数据进行了整合分析,发现lncRNA Dubr被 m6A高度修饰且在神经系统发育早期高表达。
利用小鼠体外DRG组织培养、神经元微流小室分隔培养以及胚胎电转等方法,发现敲减Dubr可以阻碍DRG神经元的轴突生长以及导致皮层神经元迁移和轴突投射缺陷,而将Dubr的m6A修饰位点突变后则无法挽回神经元的发育缺陷。
进一步研究发现,Dubr通过m6A修饰位点与m6A阅读蛋白YTHDF1和YTHDF3相互作用,同时敲减Dubr或Dubr突变m6A位点可以加速YTHDF1和YTHDF3蛋白进入蛋白酶体依赖的降解途径,最终导致蛋白水平显著下降。同时,Dubr、YTHDF1和YTHDF3均能调控与神经元发育相关基因Calmodulin和Tau的mRNA翻译,Dubr通过m6A甲基化促进YTHDF1/3蛋白复合体的稳定来维持Calmodulin和Tau的mRNA翻译并促进感觉神经元的轴突生长和皮层神经元的正确迁移。
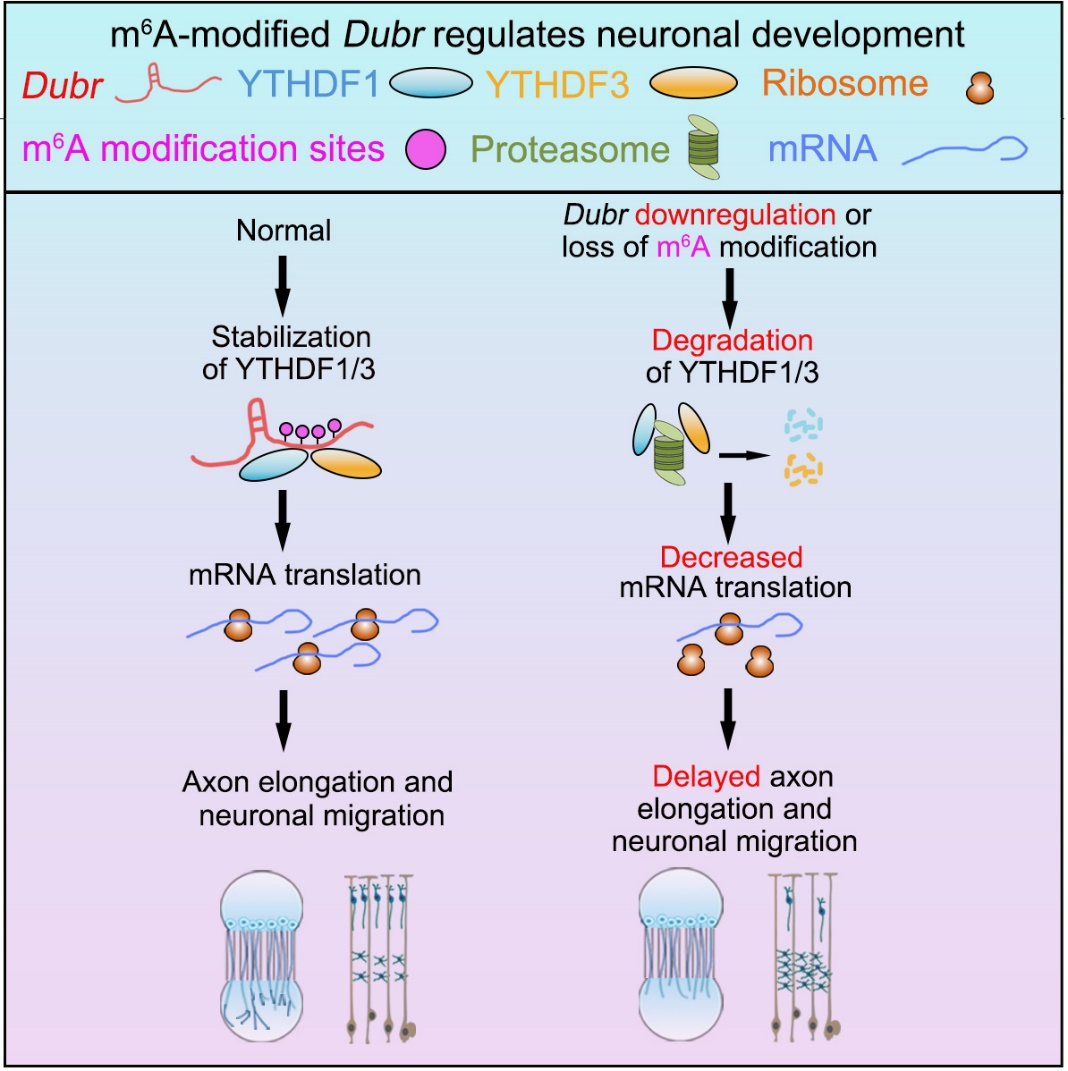
m6A修饰的lncRNA Dubr通过稳定YTHDF1/3复合体和促进mRNA翻译从而调控神经元发育
综上所述,本研究揭示了神经元发育中lncRNA的m6A动态修饰通过稳定RNA结合蛋白调控mRNA翻译的功能。该研究加深了对于非编码RNA上m6A动态修饰功能和机制的理解,也为探究神经系统发育的复杂调控机制提供了新的视角。
中科院分子细胞卓越中心鲍岚研究组博士研究生黄建松为论文第一作者,鲍岚研究员和广东省智能科学与技术研究院王斌研究员为论文共同通讯作者。这项工作得到了复旦大学生物医学研究院的杨力研究员、中科院上海高等研究院的张旭研究员和南方科技大学的蒋兴宇教授的大力支持。该工作得到了国家基金委和广东省高水平创新研究院项目的资助。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


