德国应用化学:发现酶促不对称合成N-取代1,2-氨基醇新方法
来源:天津工生所 2022-03-29 13:31
手性N-取代1,2-氨基醇是许多天然产物和药物的关键结构单元,也作为手性催化剂、手性配体或手性助剂应用于复杂分子的不对称合成。但是,现有的合成方法存在反应条件比较苛刻、区域/立体选择性较差等不足,开发高效、绿色不对称合成手性N-取代1,2-氨基醇的新方法具有应用价值。近期,中国科学院天津工业生物技术研究所生物催化与绿色化工研究团队利用亚胺还原酶和苯甲醛裂解酶
手性N-取代1,2-氨基醇是许多天然产物和药物的关键结构单元,也作为手性催化剂、手性配体或手性助剂应用于复杂分子的不对称合成。但是,现有的合成方法存在反应条件比较苛刻、区域/立体选择性较差等不足,开发高效、绿色不对称合成手性N-取代1,2-氨基醇的新方法具有应用价值。
近期,中国科学院天津工业生物技术研究所生物催化与绿色化工研究团队利用亚胺还原酶和苯甲醛裂解酶建立基于C1化合物(甲醛)的一锅两步酶法不对称合成手性N-取代1,2-氨基醇的新途径,实现抗疟疾和细胞毒性的四氢喹啉生物碱药物关键中间体的高效、绿色不对称合成。
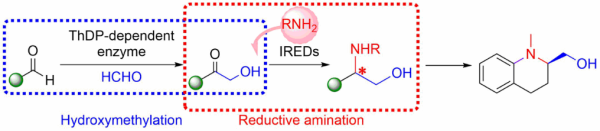
该研究从大量亚胺还原酶中筛选出10个立体选择性互补的亚胺还原酶进行底物特异性研究,发现部分亚胺还原酶对不同类型的芳香族及脂肪族α-羟甲基酮和胺类供体具有很高的活性和立体选择性,实现对映选择性互补的N-取代1,2-氨基醇的不对称合成(光学纯度为91%—99% ee,分离收率为41%—84%),拓展亚胺还原酶的底物适用范围;通过对焦磷酸硫胺素(ThDP)依赖型酶的挖掘及筛选,获得一个苯甲醛裂解酶可以催化芳基/烷基醛与甲醛的高效、选择性转化合成α-羟甲基酮类化合物,在此基础上构建“一锅两步”酶催化反应体系,以甲醛、简单醛类化合物和胺类化合物为底物,直接合成光学纯N-取代1,2-氨基醇,避免中间产物α-羟甲基酮的分离纯化,极大简化合成路径;利用化学-酶催化相结合的方法,通过羟甲基化、还原胺化以及分子内碳氮耦合反应合成抗疟疾和细胞毒性四氢喹啉生物碱的重要前体。
该研究为手性N-取代1,2-氨基醇的合成提供了新方法,也为C1化合物(甲醛等)的高值化利用开辟了新途径。
相关成果发表在《德国应用化学》上。研究得到国家重点研发计划、国家自然科学基金及天津市合成生物技术创新能力提升行动的支持。(生物谷 Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


