Nat Biomed Eng:揭示扩散到淋巴结中的癌细胞躲避宿主机体免疫破坏的分子机理
来源:本站原创 2021-07-21 23:39
2021年7月22日 讯 /生物谷BIOON/ --强烈而持久的抗癌免疫反应与抗肿瘤引流淋巴结中产生的活化癌症特异性T细胞直接相关,然而,癌细胞仍然可以定植于淋巴结中并驱动肿瘤进展。淋巴结对于机体抵御肿瘤的免疫反应至关重要,但矛盾的是,能扩散或转移到淋巴结中的癌细胞往往会躲避免疫细胞的清除作用。近日,一篇发表在国际杂志Nature Biomedical En
2021年7月22日 讯 /生物谷BIOON/ --强烈而持久的抗癌免疫反应与抗肿瘤引流淋巴结中产生的活化癌症特异性T细胞直接相关,然而,癌细胞仍然可以定植于淋巴结中并驱动肿瘤进展。淋巴结对于机体抵御肿瘤的免疫反应至关重要,但矛盾的是,能扩散或转移到淋巴结中的癌细胞往往会躲避免疫细胞的清除作用。近日,一篇发表在国际杂志Nature Biomedical Engineering上题为“Solid stress impairs lymphocyte infiltration into lymph-node metastases”的研究报告中,来自麻省总医院等机构的科学家们通过研究揭示了这种免疫逃避背后的细节,相关研究结果或能帮助科学家们开发新型疗法来克服癌细胞的这种作用。
图片来源:https://www.nature.com/articles/s41551-021-00766-1
研究者Timothy P. Padera博士表示,我们都知道,随着癌症的进展,淋巴结往往是癌症扩散蔓延的第一个位点,而且免疫系统能攻击并杀灭癌细胞。研究人员非常困扰的是,机体产生免疫反应的器官—淋巴结如何允许癌细胞生存并接管它们而并非对其发起攻击,这就是我们进行深入研究背后的动力。通过对来自乳腺癌、结肠癌、头颈癌患者的组织以及乳腺癌淋巴结转移的动物模型进行分析,研究者发现,T细胞在转移的淋巴结中非常丰富,但其却无法穿过能扩散到淋巴结中的肿瘤组织。随后研究者测定了发生癌症转移的淋巴结中的物理驱动力,即固相压力,他们推测,淋巴结肿瘤中的固相压力能损伤淋巴结中的血流和T细胞的运输能力。
随后研究人员开发了一种设备来压缩淋巴结从而刺激淋巴结肿瘤转移的逐渐生长,当将这种压缩李施加于淋巴结时,这种物理驱动力与进入到淋巴结中的T细胞的干扰之间或许就存在明显的关联;本文研究结果表明,随着癌细胞在淋巴结中生长,其就会识别并改变淋巴结,从而使得免疫系统的关键功能性反应失效。而通过理解癌细胞如何让淋巴结功能失调,研究人员希望能够进行反击来帮助淋巴结产生抗癌免疫反应,从而帮助抵御机体中的癌细胞。
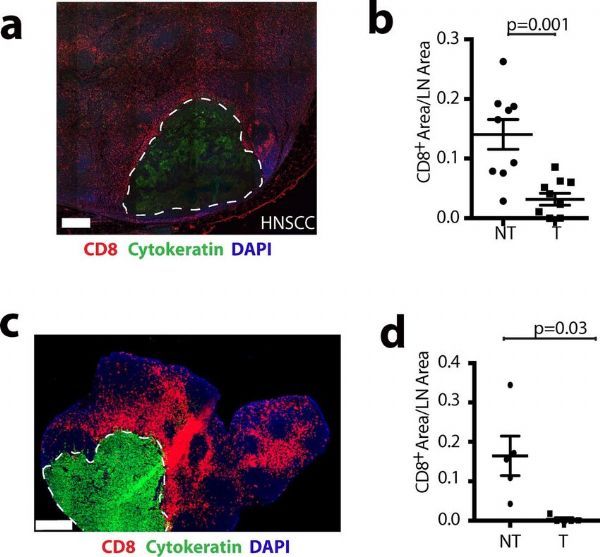
转移病灶内缺乏CD8 T细胞的浸润。
图片来源:Dennis Jones, et al. Nature Biomedical Engineering (2021). DOI:10.1038/s41551-021-00766-1
利用降压药氯沙坦(losartan)来缓解这种固相压力或能增强淋巴结转移中血管和T细胞的数量,这就表明,激活固相压力或许能作为一种潜在的 策略来改善T细胞进入到肿瘤中。研究者Jones指出,目前那我们的研究结果派生出了很多重要的问题,即氯沙坦疗法结合免疫疗法是否会通过T细胞的杀灭作用来清除淋巴结中转移性的癌细胞,而且这是否会导致机体出现强烈的全身性抗癌免疫反应,从而帮助清除整个机体中的癌症?找到这些问题的答案或将帮助开发治疗转移性癌症的新型疗法策略。
综上,本文研究结果表明,固相压力所介导的淋巴细胞浸润到淋巴结转移中的损伤或许就解释了一种治疗性的途径,从而帮助克服癌症患者免疫疗法期间的T细胞排斥作用。(生物谷Bioon.com)
原始出处:
Dennis Jones, Zixiong Wang, Ivy X. Chen, et al. lymphocyte infiltration into lymph-node metastases, Nature Biomedical Engineering (2021). DOI:10.1038/s41551-021-00766-1
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。