打破尘封!肥厚型心肌病突破性进展,首个精准靶向核心病理生理机制的药物在我国获批
来源:奇点糕 2024-05-07 09:20
玛伐凯泰作为现阶段全球首个且目前唯一一个获批上市的心肌肌球蛋白抑制剂,它直接针对HCM的核心病理生理机制,有效减少了β-肌球蛋白与肌动蛋白之间横桥的形成,减轻了心肌的过度收缩。
近日,肥厚型心肌病(HCM)——35岁以下年轻人心源性猝死的最大幕后黑手[1] ,终于迎来了自己的克星。
4月24日,中国国家药品监督管理局(NMPA)优先审评批准了全球首创心肌肌球蛋白抑制剂迈凡妥®(通用名:玛伐凯泰胶囊 Mavacamten)上市,用于治疗纽约心脏协会(NYHA)心功能分级II-III级的梗阻性肥厚型心肌病(HCM)成人患者,以改善患者的运动能力和症状[2]。
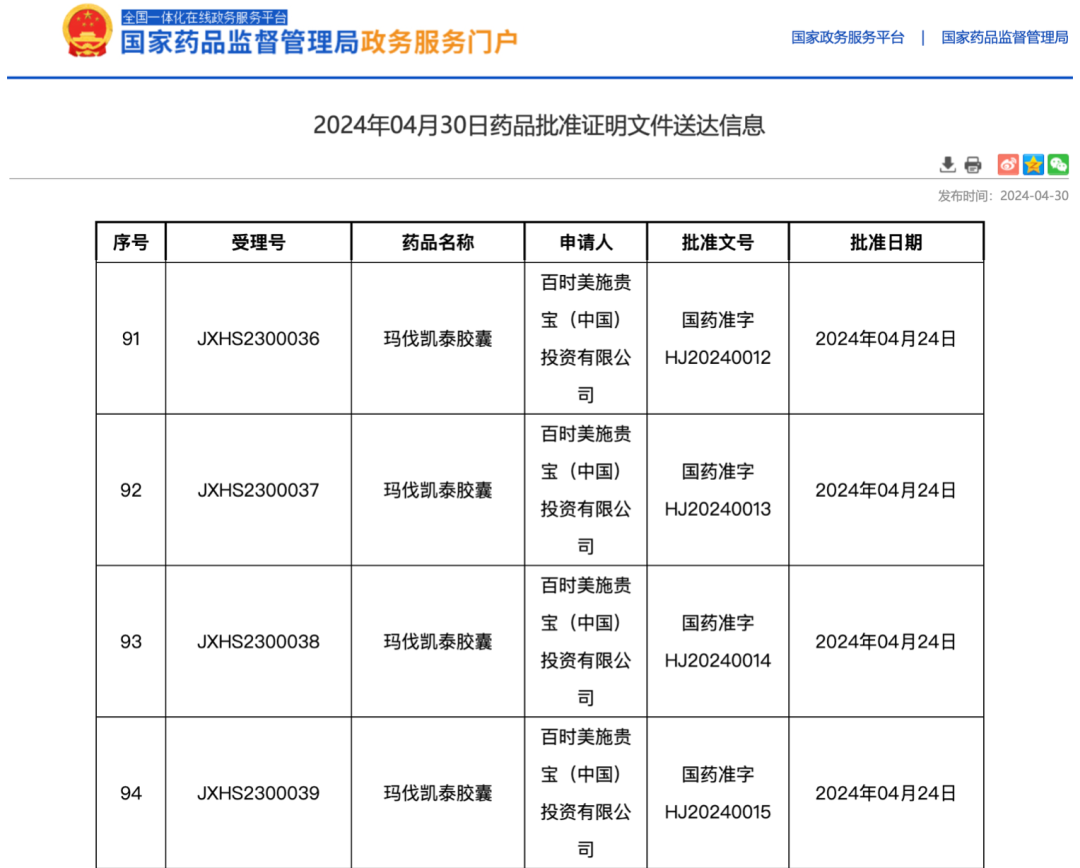
▲ NMPA批准的截图
值得一提的是,玛伐凯泰是HCM长达150余年的研究史中[3],首个针对HCM发病机制的治疗药物。在2020年和2022年,玛伐凯泰先后获得美国FDA和我国NMPA药品审评中心(CDE)授予的治疗梗阻性肥厚型心肌病“突破性治疗药物”认定,并于2022年率先获得美国FDA的批准[4],成为全球首个也是目前唯一一个获批的心肌肌球蛋白抑制剂。
在获得FDA批准的短短一年半之后,也就是2023年的10月,玛伐凯泰因其创新的机制在美国摘得医药和生物医疗行业的最高荣誉——享有医疗界“诺贝尔奖”之称的盖伦奖“最佳生物技术产品奖”[5]。

▲ 2023年盖伦奖截图
究竟是什么原因让盖伦基金会在如此短的时间内就对玛伐凯泰青眼相加呢?要想弄清楚这个问题,还得从科学家对HCM的认知以及玛伐凯泰的作用机制说起。
疯狂的心肌肌球蛋白
虽然现在我们已经知道,HCM是一种以心室壁增厚为主要特征(左心室壁受累最为常见)的原发性心肌病[6],约60%的患者表现为常染色体显性遗传[7],但是科学家认识HCM的过程并不容易。
从文献史料来看,对HCM的最早文献报道可以追溯到1868年[3]。在此后的100多年里,全球各地有越来越多的临床医生报道了HCM病例,并详细地描述了HCM患者的特征[3]。不过,由于HCM的异质性较强,且当时对HCM缺乏统一认知,导致在HCM的研究史上,HCM至少出现了75个不同名字[8]。
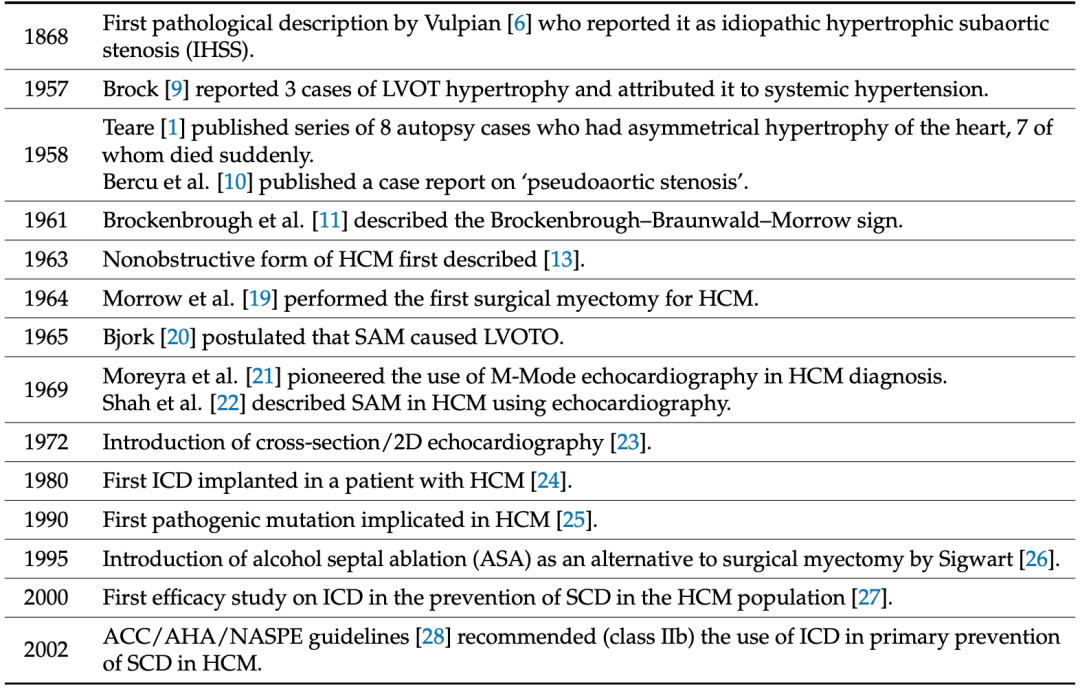
▲ 科学家认知HCM的过程[3]
科学家对HCM认知的突破,出现在1990年左右,当时美国布列根和妇女医院的研究人员接连在顶级杂志《新英格兰医学期刊》[9]和《细胞》[10]发表两篇论文,宣布找到了导致HCM的基因突变——编码β-肌球蛋白重链的MYH7。这两个重磅研究成果的诞生,意味着HCM是一种遗传病。
现在,科学家已经知道,遗传是HCM最主要的致病因素,但仍有部分患者病因不明。时至今日,科学家已经在至少8个编码心肌肌小节相关蛋白的基因(被称为HCM的“核心致病基因”)中,发现超1500个与HCM发病相关的变异。其中又以编码心脏型肌球蛋白结合蛋白C(MYBPC3)的基因和MYH7的变异最常见,二者约占基因变异阳性HCM患者的70%[11]。
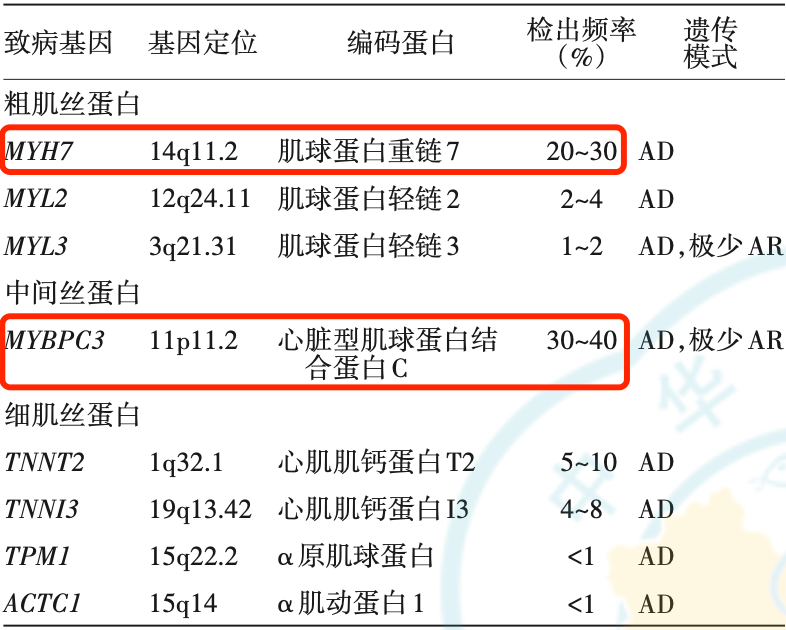
▲ HCM常见的致病基因变异[6]
不过,随着导致HCM的基因突变不断增加,从1969年就开始研究肌肉收缩的斯坦福大学心血管疾病专家James Spudich却越来越困惑了[11]。至于Spudich困惑的原因,还得从HCM的发病特征——心肌收缩亢进说起。
我们的心脏之所以能持续有节奏地跳动,与心肌张弛有度、勤勤恳恳地工作密不可分。心肌由心肌细胞组成,在心肌细胞里面有平行排列的粗肌丝和细肌丝。细肌丝主要由肌动蛋白构成,粗肌丝的结构相对比较复杂,想要搞清楚它的结构,得先认识一下老朋友β-肌球蛋白。
β-肌球蛋白是一种结构很独特的马达蛋白,长得就像个豆芽。科学家将β-肌球蛋白上面的两个“豆瓣”称作头部,因此β-肌球蛋白也被Spudich视作“双头怪物”;β-肌球蛋白下面长长的“豆芽茎”被称为尾部。心肌细胞中的粗肌丝,其实就是β-肌球蛋白编织而成的(就跟大蒜串很像)。
豆芽状的β-肌球蛋白有两种状态,两个“豆瓣”打开或者关闭。在“豆瓣”打开的情况下,β-肌球蛋白就可以夹住并拉扯肌动蛋白构成的细肌丝,让心肌收缩;在“豆瓣”关闭的情况下,β-肌球蛋白“耷拉着两个脑袋”,进入“打瞌睡”的休息状态,此时心肌松弛。如此一张一弛之间,我们的心肌就开始正常收缩了。
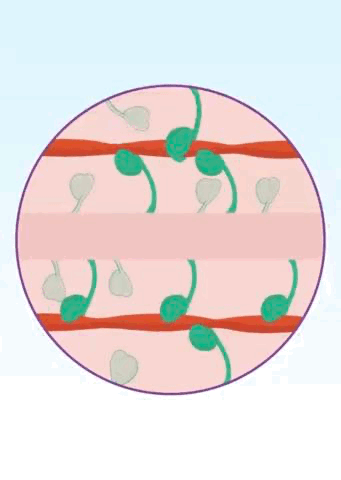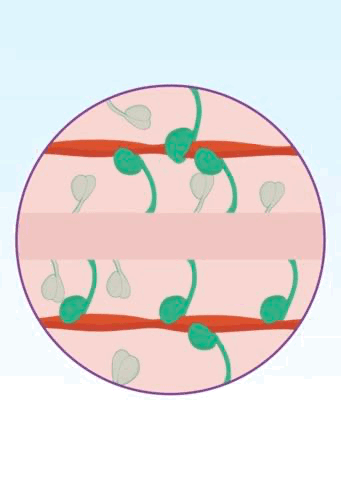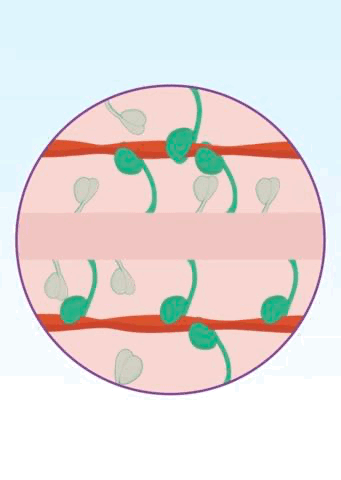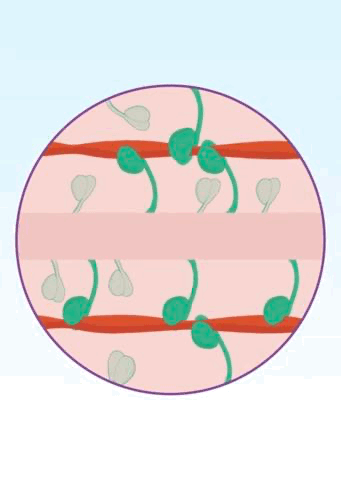
▲ 图中粉红色代表粗肌丝,绿色代表β-肌球蛋白,红色代表肌动蛋白组成的细肌丝[11]
搞清楚了心肌细胞的工作原理,再来看看HCM的心肌收缩亢进的原因。
在正常情况下,有一部分β-肌球蛋白处于工作状态,另一部分β-肌球蛋白则处于休息状态。二者之间的平衡,是心跳有节奏的关键。然而,在HCM病理状态下,这种美妙的平衡却被打破了,更多“打瞌睡”的β-肌球蛋白进入工作状态,开始拉扯细肌丝。有拔河经验的朋友们一定知道,参赛队员突然变多了,那拉扯的力量可就大了。
同样的道理,被基因突变“唤醒”的β-肌球蛋白的加入,无疑会让心肌处于收缩亢进状态。如果一天24小时心肌都这样收缩,后果可想而知,心肌会变厚、变硬,左心室流出道(LVOT)压差出现,患者运动能力下降,会出现疲累、胸闷等症状,最终心脏会受损、停跳,甚至导致患者死亡。

▲ 过多的β-肌球蛋白拉扯细肌丝[12]
刨根问底,革命性小分子问世
有了以上背景知识,现在终于可以谈谈Spudich的困惑了。
在Spudich看来,基因突变一般会导致蛋白质失去正常的功能,而发生在β-肌球蛋白上的突变却让β-肌球蛋白更有干劲儿了;更神奇的是,发生在β-肌球蛋白上的突变如此之多,它们居然都会导致β-肌球蛋白过度收缩。这也太不符合常理了。
这个问题困扰了Spudich好几个月,直到2014年12月14日,Spudich做了一个梦[11]。在他的梦中,一些平顶山竟然变成了β-肌球蛋白分子的样子。这个梦在我们看来可能平淡无奇,但是它却一下子惊醒了熟悉β-肌球蛋白结构的Spudich。
Spudich突然意识到,如果从一个合适的角度观看β-肌球蛋白的三维结构的话,就会发现β-肌球蛋白头部的一部分表面其实也是“一望无际”的,就像梦境中的平顶山一样。虽然研究人员早在1993年就知道这个大平台的存在;但直到2014年,还没有人考虑过它存在的意义。
很早之前Spudich团队就注意到,虽然从β-肌球蛋白的氨基酸序列上看,基因突变发生位点似乎没啥规律;但是,当β-肌球蛋白完成三维折叠之后,那些突变竟然有很多都聚集在大平台中央附近。
这究竟意味着什么呢?出现在梦中的平顶山状β-肌球蛋白让Spudich意识到,基因突变导致的氨基酸替换会影响β-肌球蛋白头部带的电荷,而电荷是异性相吸的。如果β-肌球蛋白头部的突变导致β-肌球蛋白两个头部的吸引力减小,那么β-肌球蛋白不就更容易处于“打开”的激活状态么!

▲ β-肌球蛋白的三维结构图:左图是打开状态,右图是关闭状态[10]
2015年1月,Spudich将他的上述猜想以论文的形式发表[13]。这篇论文认为,发生在β-肌球蛋白上的突变,其实是将处于“关闭”状态的β-肌球蛋白释放出来,增加了有结合能力的β-肌球蛋白,从而增加了心肌的动力输出,进而导致HCM的发生[13]。
目前,这一观点正在成为致病性β-肌球蛋白突变导致HCM的统一假说[14]。不过,在当时的情况下,Spudich提出的仅仅是个猜想,要证明这个假说并不容易。
为了验证上述假说,Spudich在1998年共同创办的MyoKardia公司(已被BMS收购)与哈佛医学院展开了合作。研究人员想到的方法是——找到一种能降低心肌动力输出的小分子。如果由粗肌丝和细肌丝等构成的肌小节的动力过剩,是HCM的发生原因;那么抑制肌小节动力输出的小分子,肯定可以从根源上改善HCM[15]。
之前已经有研究发现,肌小节动力输出是β-肌球蛋白头部产生的合力与其沿肌动蛋白丝运动速度的乘积[15]。既然如此,改变上面两个变量中的任意一个,就可以调节肌小节的动力输出,他们选择了减少β-肌球蛋白头部合力。简单来说,其实就是找到让β-肌球蛋白进入关闭状态的小分子。
β-肌球蛋白的ATP酶活性成为研究人员关注的焦点。众所周知,运动肯定要消耗能量,β-肌球蛋白也不例外,它是一种ATP依赖型马达蛋白,头部具有ATP酶活性。当β-肌球蛋白头部与ATP结合之后,会将ATP水解为ADP和磷酸盐并释放能量,帮助β-肌球蛋白与肌动蛋白强力结合,在粗肌丝和细肌丝之间形成横桥连接,然后输出动力,让心肌收缩;能量消耗完之后,β-肌球蛋白与肌动蛋白分离[14]。如此循环往复。
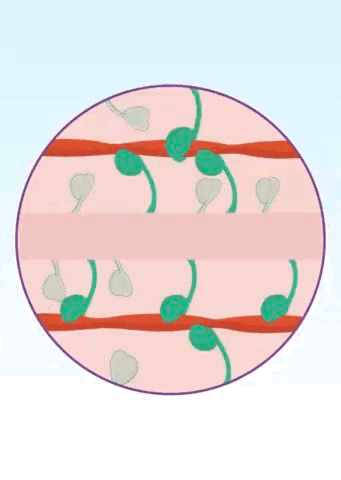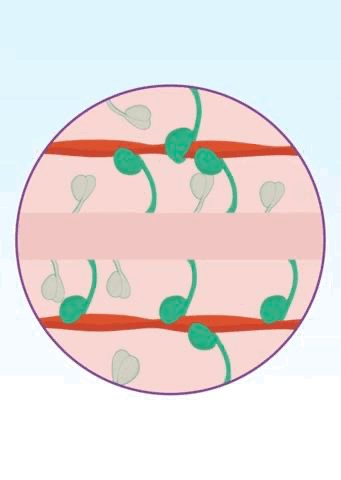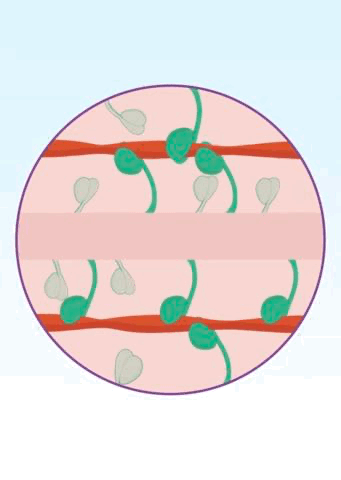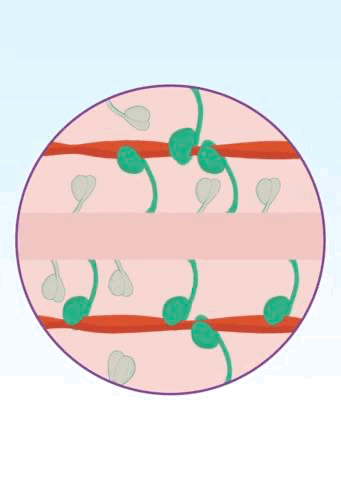
▲ 横桥这个名字是不是还挺形象?[12]
由于能量的释放是决定能否形成产力横桥的关键,因此,MyoKardia和哈佛团队认为,如果能抑制β-肌球蛋白的ATP酶活性,延缓或者阻止能量的释放,就可以让更多的β-肌球蛋白头部处于关闭状态。
2015年9月1日,MyoKardia和哈佛团队向《科学》杂志递交了研究论文,宣布筛选到了β-肌球蛋白ATP酶活性的理想小分子选择性变构抑制剂MYK-461,也就是现在为我们所熟知的玛伐凯泰,它能与β-肌球蛋白可逆性结合。2016年1月5日,研究论文在《科学》杂志正式发表[15],玛伐凯泰正式诞生。
两年半之后,Spudich团队进一步揭示了玛伐凯泰的作用机制[16],证实玛伐凯泰确实能将β-肌球蛋白头部稳定在关闭的状态。显然,玛伐凯泰减少了肌球蛋白-肌动蛋白横桥连接的形成,进而避免了心肌的过度收缩。
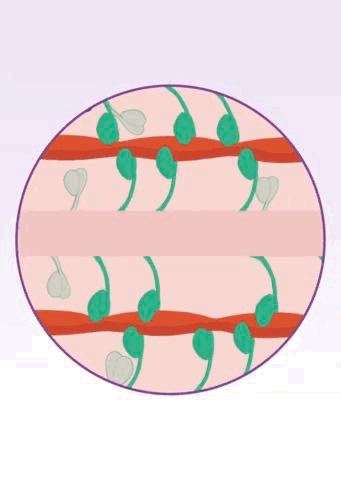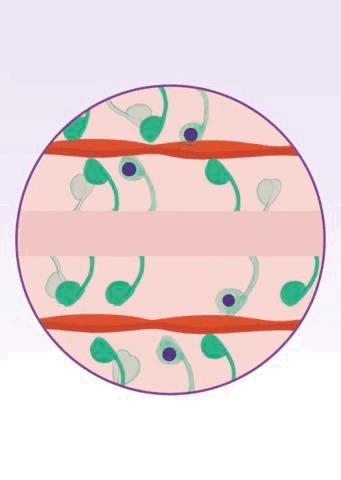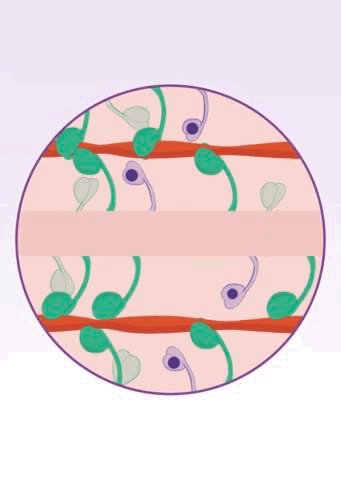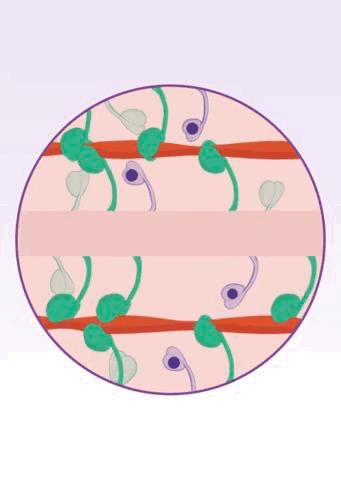
▲ 玛伐凯泰的作用机制[11]
不难看出,针对HCM发病机制而开发出来的玛伐凯泰具有革命性的意义。
要知道,自HCM首次被报道至今的150多年里,所有治疗HCM的疗法都是非特异性的,或者说“治标不治本”。
β受体阻滞剂和非二氢吡啶类钙通道阻滞剂,虽然能在一定程度上改善患者的症状,但是只能在少数患者完全缓解梗阻,大多数患者左心室流出道(LVOT)压差及症状仍持续存在,患者的生活质量改善非常有限。手术也可以改善HCM症状,但是在心脏上实施手术难度大且存在并发症风险,患者接受度较低,在临床上并未得到广泛应用。
那么玛伐凯泰的临床表现究竟如何呢?能从HCM疾病的本质上,改善患者的LVOT压差、运动能力和生活质量吗?
凯歌高奏,改变临床治疗规则
玛伐凯泰的临床研究推进速度同样非常快。
在筛选到玛伐凯泰的同一年,也就是2015年,斯坦福遗传性心血管疾病医学中心的研究人员就启动了临床探索,玛伐凯泰正式迎来了它的第一位患者[17]。
2018年5月,关键的多中心、国际性、双盲3期临床研究EXPLORER-HCM启动,研究结果于2020年发表在顶级医学杂志《柳叶刀》上[18]。

▲ 论文首页截图
这是一项为期30周、双盲、随机、安慰剂对照试验,在13个国家的68个中心进行,分别有123名和128名梗阻性HCM患者接受玛伐凯泰或安慰剂治疗,其中,玛伐凯泰组37%的患者达到主要终点,即峰值耗氧量(pVO2)提高≥1.5mL/kg/min且NYHA分级改善≥1级,或pVO2提高≥3.0mL/kg/min且NYHA分级无恶化;对照组仅有17%达到这一终点。研究结果表明,与安慰剂相比,玛伐凯泰可显著改善梗阻性HCM患者的症状、运动耐量,缓解LVOT梗阻,而且患者对治疗的总体耐受性较好。
EXPLORER-HCM的一项亚组研究证实,伴有或者未伴有肌小节基因突变的患者,都能从玛伐凯泰治疗中获益[19]。
在EXPLORER-HCM患者中,有231名参加了后续的长期扩展试验EXPLORER-LTE,评估玛伐凯泰治疗梗阻性HCM的长期安全性和有效性。在2023年欧洲心脏病学会(ESC 2023)大会上,MAVA-LTE研究的EXPLORER队列120周累积分析结果以口头报告的形式发布[20]。结果显示,75.9%的患者从LTE研究初始至第120周改善≥1个NYHA等级,同时观察到玛伐凯泰持续治疗相关的超声心动图改善,且未观察到新的安全信号,证实长期玛伐凯泰治疗能够为患者带来持续获益。

▲ 论文首页截图
VALOR-HCM是在美国进行的一项3期、多中心、随机、双盲、安慰剂对照临床研究[21],旨在探究有症状的严重梗阻性肥厚型心肌病患者服用玛伐凯泰16周后,是否可有效降低达到指南所要求的侵入性室间隔减容术(SRT)标准的患者人群比例,或者症状改善到患者不再选择进行SRT,主要终点是在第16周之前或第16周时继续接受SRT治疗,或治疗16周后仍符合SRT治疗标准。

▲ 论文首页截图
研究共入组112名患者,16周后显示,玛伐凯泰组不再符合SRT治疗指南要求的患者约为安慰剂组的3.5倍(分别为82% vs 23%)。研究结果表明:对于药物难治性、症状性梗阻性HCM患者,给予玛伐凯泰治疗16周后需进行SRT比例显著降低,且LVOT压差、NYHA等级、堪萨斯城心肌病问卷-临床总结评分(KCCQ-CSS)、NT-proBNP及心肌肌钙蛋白I指标均显著改善。
治疗结束时,绝大多数患者(包括安慰剂组的大多数患者)选择参加VALOR-HCM的长期试验[22]。其中16周至32周为活性药物对照阶段,原接受玛伐凯泰治疗的患者继续服用该药物,原安慰剂组患者从第16周开始转为接受玛伐凯泰治疗,剂量和剂量调整在盲法状态下进行,由核心实验室根据心超结果决定。第32到第128周为长期扩展期,在此期间所有患者均接受玛伐凯泰治疗,剂量由各研究中心根据心超结果进行调整[23]。第56周时,玛伐凯泰治疗在各关键研究终点均显示出持续的临床获益,89%的患者(96/108)继续接受玛伐凯泰治疗。
VALOR-HCM研究将EXPLORER-HCM的结果扩展到了症状更严重患者,并且证明玛伐凯泰可以降低患者对SRT的需求。

▲ 论文首页截图
2023年,中国关键3期临床研究EXPLORER-CN研究结果发布[24]。这项多中心、双盲、随机、安慰剂对照的临床试验共纳入12家中心81名有症状的梗阻性HCM患者,以2:1的比例随机接受玛伐凯泰或安慰剂对照治疗30周,主要终点为从基线到30周Valsalva LVOT峰值压差的变化。
研究结果显示:在中国梗阻性HCM患者中,玛伐凯泰在Valsalva LVOT峰值压差上表现出显著改善,同时在包括LVOT梗阻、临床症状、健康状态、心脏生物标志物及心脏结构在内的所有次要终点中均观察到改善,并且耐受性良好。

▲ 论文首页截图
EXPLORER-CN研究中患者报告健康状况的KCCQ详细数据在今年的美国心脏病学会科学年会(2024 ACC)上发布[25],在基线、第6、12、18和30周使用KCCQ-23评估患者治疗结果。研究结果显示,在第30周时,与安慰剂组相比,玛伐凯泰显著改善患者的KCCQ-23总体症状评分(TSS)、临床总结评分(CSS)和整体汇总评分(OSS),表明中国患者接受玛伐凯泰治疗30周可以显著改善健康状况。
正是因为玛伐凯泰在临床研究中的优异表现,所以在玛伐凯泰获得NMPA批准之前,《中国肥厚型心肌病指南2022》[6]、《中国成人肥厚型心肌病诊断与治疗指南2023》[26]、《国家心力衰竭指南2023》[27]和《2023欧洲心脏病学会(ESC)心肌病管理指南》[28]都推荐玛伐凯泰用于梗阻性HCM患者的治疗。
总的来说,玛伐凯泰作为现阶段全球首个且目前唯一一个获批上市的心肌肌球蛋白抑制剂,它直接针对HCM的核心病理生理机制,有效减少了β-肌球蛋白与肌动蛋白之间横桥的形成,减轻了心肌的过度收缩,改善了心肌舒张功能,减少能量过度消耗。在临床上,玛伐凯泰显著改善了LVOT压差和患者NYHA分级,也改善了患者运动能力和生活质量,首次有希望改变HCM的进程。值得一提的是,无论是遗传性HCM还是病因不明的HCM患者,玛伐凯泰均有效。
据了解,我国经年龄和性别校正后的HCM患病率约为80/10万[29]。对于这些患者中的梗阻性HCM患者群体而言,此次玛伐凯泰的获批带来的不仅是治疗方式的转变,也让他们迈向了新生。
参考文献:
[1].Frey N, Luedde M, Katus HA. Mechanisms of disease: hypertrophic cardiomyopathy. Nat Rev Cardiol. 2011;9(2):91-100. doi:10.1038/nrcardio.2011.159
[2].https://www.nmpa.gov.cn/zwfw/sdxx/sdxxyp/yppjfb/20240430111907197.html
[3].Liew AC, Vassiliou VS, Cooper R, Raphael CE. Hypertrophic Cardiomyopathy-Past, Present and Future. J Clin Med. 2017;6(12):118. doi:10.3390/jcm6120118
[4].https://www.fda.gov/drugs/news-events-human-drugs/fda-approves-new-drug-improve-heart-function-adults-rare-heart-condition
[5].https://www.galienfoundation.org/prix-galien-usa
[6].国家心血管病专家委员会心力衰竭专业委员会, 中国医师协会心力衰竭专业委员会, 中华医学会心血管分会心力衰竭学组, 等 . 中国肥厚型心肌病指南2022[J]. 中华心力衰竭和心肌病杂志, 2022, 6(2): 80-105. DOI: 10.3760/cma.j.cn1101460-20220805-00070.
[7]. Marian AJ, Braunwald E. Hypertrophic cardiomyopathy: genetics, pathogenesis, clinical manifestations, diagnosis, and therapy. Circ Res, 2017, 121(7):749-770.
[8].https://4hcm.org/hcm-many-names/
[9].Jarcho JA, McKenna W, Pare JA, et al. Mapping a gene for familial hypertrophic cardiomyopathy to chromosome 14q1. N Engl J Med. 1989;321(20):1372-1378. doi:10.1056/NEJM198911163212005
[10].Geisterfer-Lowrance AA, Kass S, Tanigawa G, et al. A molecular basis for familial hypertrophic cardiomyopathy: a beta cardiac myosin heavy chain gene missense mutation. Cell. 1990;62(5):999-1006. doi:10.1016/0092-8674(90)90274-i
[11].https://med.stanford.edu/news/all-news/2019/03/mystery-novel-and-dream-spur-key-scientific-insight.html
[12].https://www.camzyos.com/what-is-camzyos
[13].Spudich JA. The myosin mesa and a possible unifying hypothesis for the molecular basis of human hypertrophic cardiomyopathy. Biochem Soc Trans. 2015;43(1):64-72. doi:10.1042/BST20140324
[14].Nag S, Gollapudi SK, Del Rio CL, Spudich JA, McDowell R. Mavacamten, a precision medicine for hypertrophic cardiomyopathy: From a motor protein to patients. Sci Adv. 2023;9(30):eabo7622. doi:10.1126/sciadv.abo7622
[15].Green EM, Wakimoto H, Anderson RL, et al. A small-molecule inhibitor of sarcomere contractility suppresses hypertrophic cardiomyopathy in mice. Science. 2016;351(6273):617-621. doi:10.1126/science.aad3456
[16].Anderson RL, Trivedi DV, Sarkar SS, et al. Deciphering the super relaxed state of human β-cardiac myosin and the mode of action of mavacamten from myosin molecules to muscle fibers. Proc Natl Acad Sci U S A. 2018;115(35):E8143-E8152. doi:10.1073/pnas.1809540115
[17].https://scopeblog.stanford.edu/2023/02/28/basic-biochemistry-research-leads-to-heart-saving-drug/
[18].Olivotto I, Oreziak A, Barriales-Villa R, et al. Mavacamten for treatment of symptomatic obstructive hypertrophic cardiomyopathy (EXPLORER-HCM): a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet. 2020;396(10253):759-769. doi:10.1016/S0140-6736(20)31792-X
[19]. Carolyn Y Ho, et al. Circulation. 2023; 148:A12408
[20].Garcia-Pavia P, Oreziak A, Masri A, et al. Long-term effects of mavacamten treatment in obstructive hypertrophic cardiomyopathy (HCM): updated cumulative analysis of the EXPLORER cohort of MAVA-long-term extension (LTE) study up to 120 weeks[J]. European Heart Journal, 2023, 44(Supplement_2): ehad655. 1844.
[21]. Desai MY, Owens A, Geske JB et al. Myosin Inhibition in Patients With Obstructive Hypertrophic Cardiomyopathy Referred for Septal Reduction Therapy. J Am Coll Cardiol 2022; 80: 95–108.
[22].Desai MY, Owens A, Wolski K, et al. Mavacamten in Patients With Hypertrophic Cardiomyopathy Referred for Septal Reduction: Week 56 Results From the VALOR-HCM Randomized Clinical Trial. JAMA Cardiol. 2023;8(10):968-977. doi:10.1001/jamacardio.2023.3342
[23]. Desai MY, Wolski K, Owens A et al. Study design and rationale of VALOR-HCM: evaluation of mavacamten in adults with symptomatic obstructive hypertrophic cardiomyopathy who are eligible for septal reduction therapy. Am Heart J 2021; 239: 80–89.
[24]Tian Z, Li L, Li X, et al. Effect of Mavacamten on Chinese Patients With Symptomatic Obstructive Hypertrophic Cardiomyopathy: The EXPLORER-CN Randomized Clinical Trial. JAMA Cardiol. 2023;8(10):957-965. doi:10.1001/jamacardio.2023.3030
[25].Tian, Z, Li, L, Li, X. et al. EFFECT OF MAVACAMTEN ON HEALTH STATUS IN CHINESE PATIENTS WITH SYMPTOMATIC OBSTRUCTIVE HYPERTROPHIC CARDIOMYOPATHY: RESULTS FROM THE EXPLORER-CN STUDY. J Am Coll Cardiol. 2024 Apr, 83 (13_Supplement) 494. doi:10.1016/S0735-1097(24)02484-7
[26].国家心血管病中心心肌病专科联盟、中国医疗保健国际交流促进会心血管病精准医学分会“中国成人肥厚型心肌病诊断与治疗指南2023”专家组,宋雷,邹玉宝,等.中国成人肥厚型心肌病诊断与治疗指南2023[J].中国分子心脏病学杂志, 2023, 23(1):35.
[27].国家心血管病中心,国家心血管病专家委员会心力衰竭专业委员会,中国医师协会心力衰竭专业委员会,等. 国家心力衰竭指南2023[J]. 中华心力衰竭和心肌病杂志,2023,07(04):215-311. DOI:10.3760/cma.j.issn.101460-20231209-00052
[28].Arbelo E, et al; ESC Scientific Document Group. Eur Heart J. 2023 Oct 1;44(37):3503-3626.
[29].Zou Y, Song L, Wang Z, et al. Prevalence of idiopathic hypertrophic cardiomyopathy in China: a population-based echocardiographic analysis of 8080 adults. Am J Med. 2004;116(1):14-18. doi:10.1016/j.amjmed.2003.05.009
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


