登革热疫苗!武田Qdenga(TAK-003,四价减毒活疫苗)欧盟监管传喜讯:将于2月内获批上市!
来源:生物谷原创 2022-10-25 10:45
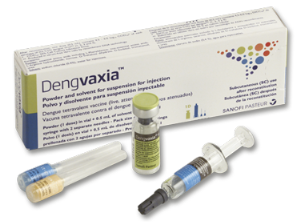
与赛诺菲登革热疫苗Dengvaxia不同,Qdenga(TAK-003)可用于没有感染过登革热的人,而且不需要进行接种前测试。

图片来源:摄图网
2022年10月25日讯 /生物谷BIOON/ --武田制药(Takeda)近日宣布,欧洲药品管理局(EMA)人用医药产品委员会(CHMP)已发布一份积极审查意见,建议批准TAK-003(登革热四价疫苗[减毒活疫苗]):用于欧盟及参与平行EU-M4all程序(EU-Medicines for all)的登革热流行国家中的4岁及以上人群,预防由任何登革热病毒血清型引起的登革热(dengue)疾病。武田预计,将在未来几个月内收到欧盟委员会(EC)的批准,并随后在拉丁美洲和亚洲收到监管审批决定。
2022年8月,Qdenga(TAK-003)获得印度尼西亚国家药物和食品管制局(BADAN POM)批准:用于6岁至45岁人群,预防任何血清型引起的登革热疾病。Qdenga可用于所有人,无论之前是否有登革热暴露史,而且也不需要进行疫苗接种前测试。Qdenga接种方案为:2剂接种方案(0月,3月),以0.5mL剂量皮下注射。
TAK-003是一款登革热四价减毒活疫苗,基于减毒的登革热血清型2病毒(DENV-2)开发,该病毒提供了针对全部4种疫苗病毒的遗传学骨架。来自儿童和青少年2期临床研究的数据显示,TAK-003在横跨各年龄组以及血清学阳性个体和血清学阴性个体中均诱导了针对4种血清型登革热病毒的中和性抗体,同时疫苗的安全性和耐受性良好。
欧盟CHMP对TAK-003的积极审查意见,基于对超过28000名儿童和成人开展的5项1/2/3期临床试验的结果。其中包括来自全球性关键3期TIDES试验的4.5年随访数据,这符合世界卫生组织(WHO)的建议,即在完成登革热疫苗接种后获得3-5年的随访数据,以便最准确地评估安全性和有效性。
TIDES试验的探索性分析表明,经过4.5年的研究随访(第2剂接种后54个月):在总体人群中(包括血清阳性和血清阴性个体),TAK-003表现出持续的整体保护作用,预防了84%的住院登革热病例和61%的症状性登革热病例。到目前为止,TAK-003的耐受性普遍良好,没有证据表明疫苗接种者的疾病增强,并且在TIDES试验中没有发现任何重要的安全风险。
新加坡杜克-新加坡国立大学医学院(Duke-NUS Medical School)新发传染病教授Ooi Eng Eong博士评价称:“全球卫生界一直渴望获得一种无需接种前检测障碍的登革热疫苗。武田提供的强有力临床数据表明,其登革热疫苗TAK-003有潜力帮助预防登革热病例和住院。今天,我们更接近于帮助改善登革热预防,减轻疾病对国家、社区和卫生系统的负担。”
Dengvaxia:全球首个登革热疫苗,赛诺菲出品
登革热(Dengue)又称“断骨热(breakbone fever)”,该病是一种由蚊子传播的病毒性疾病,在世界各地迅速传播,是世界卫生组织(WHO)2019年全球健康十大威胁之一。登革热主要由埃及伊蚊传播,其次是白纹伊蚊。它由4种登革热病毒血清型中的任何一种引起,每种血清型都能引起登革热或严重登革热。不同地理、国家、地区、季节以及随时间推移,每种血清型的流行程度不同。从一种血清型感染中康复后,只对该血清型具有终生免疫,以后暴露于任何其他血清型都会增加患严重疾病的风险。
近几十年来,世界各地登革热的发病率急剧上升,估计每年造成3.9亿例感染和50万例住院治疗。病例的增加可归因于城市化、全球化和气候变化等因素。严重登革热约占登革热病例的5%,是拉丁美洲和亚洲儿童和成人严重疾病和死亡的首要原因。在从登革热流行国家返回欧洲的旅行者中,登革热是第二大确诊发热原因。它在美洲、东南亚和西太平洋地区的流行国家具有深远的影响,在欧洲大陆的非流行地区,包括法国、意大利、德国、西班牙和美国,其影响日益扩大。
Dengvaxia(CYD-TDV,登革热四价减毒活疫苗)是赛诺菲耗时长达20年研制,该疫苗于2015年12月获墨西哥批准,作为全球获批的首个登革热疫苗产品。之后,该疫苗陆续获得拉丁美洲、亚洲多个登革热流行国家批准,并且在2018年12月获得欧盟批准。在美国,Dengvaxia于2019年5月获得FDA批准,成为美国市场针对登革热的首个医学预防工具。
然而,在推出一年多后,根据赛诺菲公布的临床试验新安全数据显示:对于接触过登革热病毒的人,Dengvaxia能够如期发挥作用,但对于之前没有感染登革热的人而言,使用该疫苗可能会引起严重的重症病情。世界卫生组织(WHO)也根据持续获得的跟踪数据,及时对Dengvaxia使用范围进行了建议:在使用Dengvaxia前应该进行检测,以评估疫苗接种者是否曾感染登革热病毒。(生物谷Bioon.com)
原文出处:Takeda Receives Positive CHMP Opinion Recommending Approval of Dengue Vaccine Candidate in EU and Dengue-Endemic Countries
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


