Science:揭示休眠的细菌孢子萌发新机制
来源:生物谷原创 2023-05-12 15:35
自从150多年前人们首次描述细菌孢子---惰性、沉睡的细菌---以来,来自美国哈佛医学院的研究人员在一项新的研究中解决了一个困惑生物学家的谜团,他们发现了一类新的细胞传感蛋白,使孢子能够检测到其环境中
自从150多年前人们首次描述细菌孢子---惰性、沉睡的细菌---以来,来自美国哈佛医学院的研究人员在一项新的研究中解决了一个困惑生物学家的谜团,他们发现了一类新的细胞传感蛋白,使孢子能够检测到其环境中存在的营养物并迅速恢复活力。

事实证实,这类传感蛋白是穿过细胞膜的离子通道,在休眠期间保持关闭,但当它们检测到营养物时迅速打开。一旦打开,这些离子通道允许带电离子通过细胞膜流出,启动孢子的保护性壳脱落,并在休眠多年甚至几个世纪后开启代谢过程。这些研究结果可能有助于设计出防止危险的细菌孢子休眠数月甚至数年后再次苏醒并导致疾病爆发的方法。相关研究结果发表在2023年4月28日的Science期刊上,论文标题为“Bacterial spore germination receptors are nutrient-gated ion channels”。
论文通讯作者、哈佛医学院布拉瓦特尼克研究所微生物学教授David Rudner说,“这项发现解决了一个已存在一个多世纪的难题。当细菌的系统在这种保护性壳内几乎完全关闭时,细菌是如何感知环境的变化并采取行动打破休眠的?”
休眠的细菌如何复活
为了在不利的环境条件下生存,一些细菌进入休眠状态,成为孢子,生物过程被搁置,它们的细胞周围有多层保护性壳。这些生物惰性的保护性壳使得细菌能够等待饥荒的结束,并保护自己免受极端高温、干旱、紫外线辐射、刺激性化学品和抗生素的破坏。
一个多世纪以来,科学家们已知道,当孢子检测到它们环境中的营养物时,它们会迅速脱去它们的保护壳,重新点燃它们的代谢引擎。尽管使它们能够检测到营养物的传感蛋白在近50年前就被发现了,但传递唤醒信号的方法以及该信号如何触发细菌的复苏仍然是一个谜。
在大多数情况下,信号传递依赖于代谢活动,并且经常涉及编码蛋白的基因,以制造特定的信号分子。然而,这些过程在休眠细菌内部都是关闭的,这就提出了这种信号如何诱使休眠的细菌复苏过来的问题。
在这项新的研究中,Rudner及其研究团队发现这种营养物传感蛋白本身组装成一种导管,使细菌细胞重新开始工作。在对营养物作出反应时,该管道(一种膜离子通道)打开,允许离子从孢子内部流出。这启动了一连串的反应,使休眠的细胞脱去保护性壳,恢复生长。
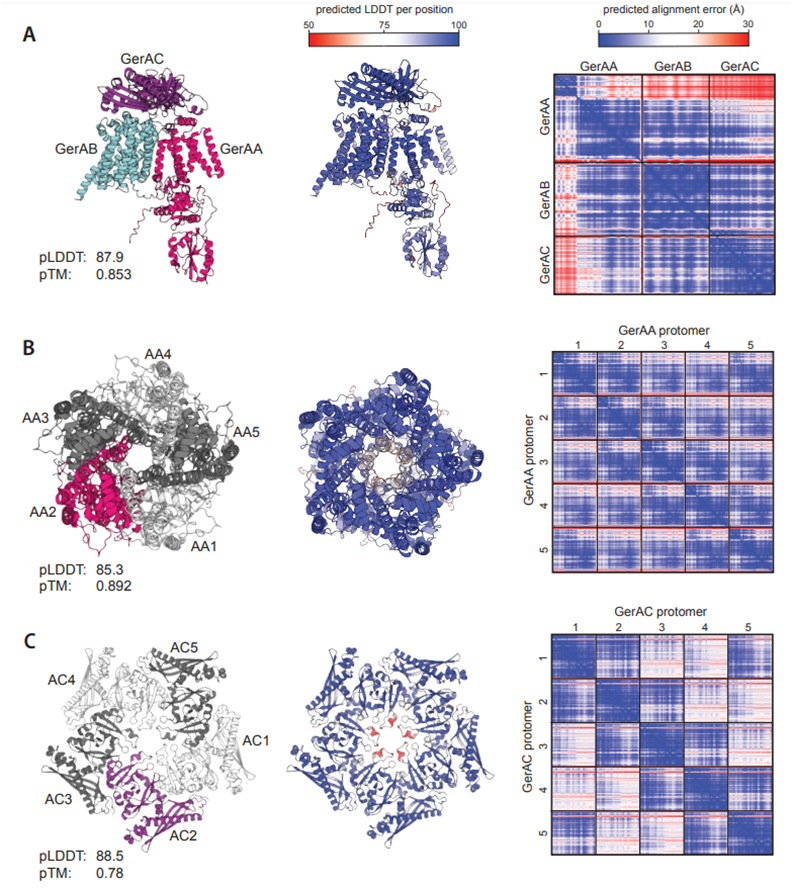
图片来自Science, 2023, doi:10.1126/science.adg9829。
这些作者利用多种方法追踪了这个谜团的曲折性。他们部署了人工智能工具来预测这种复杂折叠的传感蛋白复合物---由同一种传感蛋白的5个拷贝组成---的结构。他们应用机器学习来确定构成这种离子通道的亚基之间的相互作用。他们还使用基因编辑技术来诱导细菌产生传感蛋白突变体,以此来测试基于计算机的预测在活细胞中是如何进行的。
Rudner说,“我喜欢科学的一点是,当你有了一项发现,所有这些不相干的观察结果突然变得有意义。这就像你在进行拼图,你找到了一个拼块的位置,突然你可以很快地装上另外六个拼块。”
Rudner将这项研究中的发现过程描述为一系列令人困惑的观察结果,这些观察结果慢慢成形,这要归功于一组具有不同观点的研究人员协同合作。在这一过程中,他们不断有令人吃惊的使他们感到困惑的观察结果,这提示着了一些看起来不可能是真的答案。
将线索拼接在一起
当Rudner实验室研究员Yongqiang Gao在用枯草芽孢杆菌进行一系列实验时,出现了一条早期线索。Gao将其他形成孢子的细菌的基因引入枯草芽孢杆菌,以探索由此产生的不匹配的蛋白会干扰孢子萌发的想法。令他惊讶的是,Gao发现在某些情况下,休眠的细菌孢子在使用一组来自亲缘关系较远的细菌的蛋白后能完美地苏醒。
在进行这项研究时,Rudner实验室博士后Lior Artzi为Gao的这一发现提出了一个解释。如果这类传感蛋白是一种受体,在检测到信号(在这种情况下是一种营养物,如糖或氨基酸)之前,它的作用就像一扇关闭的门。一旦这类传感蛋白与营养物结合,它就会打开,允许离子从孢子中流出来。
换句话说,这些来自亲缘关系较远的细菌的蛋白不需要与不匹配的枯草芽孢杆菌孢子蛋白相互作用,而只是对离子开始流动时孢子的电状态变化作出反应。
Rudner最初对这一假设持怀疑态度,因为这类受体并不符合这一特征。它们几乎没有离子通道的特征。但是,Artzi认为,这类传感蛋白可能是由多个亚基组成的,在一种更复杂的结构中共同工作。
人工智能大显身手
Rudner实验室博士后Jeremy Amon是AlphaFold的早期使用者,AlphaFold是一种可以预测蛋白和蛋白复合物结构的人工智能工具。
这种人工智能工具预测这种特定的受体亚基组装成一种五聚体的环。它所预测的结构包括一个位于中间的通道,可以让离子通过孢子的膜。这种人工智能工具的预测与Artzi的猜测不谋而合。
Gao、Artzi和Amon随后合作测试了这种人工智能生成的模型。他们与Rudner实验室博士后Fernando Ramírez-Guadiana和哈佛医学院生物化学与分子药理学教授Andrew Kruse团队以及哈佛医学院系统生物学副教授、计算生物学家Deborah Marks团队密切合作。
他们利用改变的受体亚基对孢子进行改造,预计这会拓宽这种膜离子通道,并发现孢子在没有营养物信号的情况下会苏醒。反过来,他们产生了突变的受体亚基,他们预测这些突变的受体亚基会缩小该离子通道的孔径。这些孢子未能打开这种释放离子的闸门,在有充足的营养物诱导它们脱离休眠的情况下也未能从静止状态中苏醒。
换句话说,与预测的这种折叠的传感蛋白复合物的构型稍有偏差,就会使该离子通路打开或关闭,这就使得它作为唤醒休眠细菌的工具变得毫无用处。
对人类健康和食品安全的影响
Rudner说,了解休眠细菌如何恢复生命不仅仅是一个智力上的诱人难题,而且对人类健康也有重要影响。一些能够长时间进入深度休眠状态的细菌是危险的,甚至是致命的病原体:白色粉末状的炭疽菌武器是由细菌孢子组成的。
另一种危险的形成孢子的病原体是艰难梭菌(Clostridioides difficile),它导致危及生命的腹泻和结肠炎。艰难梭菌感染引起的疾病通常发生在使用抗生素之后,抗生素可以杀死许多肠道细菌,但对休眠的孢子没有作用。在治疗后,艰难梭菌从休眠状态中苏醒过来,并可能大量增殖,往往造成灾难性的后果。
消除孢子也是食品加工厂的一个核心挑战,因为休眠细菌由于其保护性壳和脱水状态,可以抵制消毒处理。如果消毒不成功,孢子萌发和生长会造成严重的食源性疾病和巨大的经济损失。
了解孢子如何感知营养物并迅速脱离休眠状态,可以使科学家们开发出较早地触发孢子萌发的方法,从而有可能对细菌进行消毒,或阻止孢子萌发,使细菌被困在其保护壳内,无法生长、增殖并使食物变质或导致疾病。(生物谷 Bioon.com)
参考资料:
Yongqiang Gao et al. Bacterial spore germination receptors are nutrient-gated ion channels. Science, 2023, doi:10.1126/science.adg9829.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


