《科学·免疫学》:小烧一点确实有用!科学家发现,发烧会导致部分T细胞的增殖和炎症效应功能,也会让部分T细胞线粒体应激和DNA损伤
来源:奇点糕 2024-10-24 09:52
这项研究强调了高温对T细胞功能和基因组稳定性的复杂影响。发烧能够让CD4+T细胞更好地发挥保护性免疫反应,但是也会引起细胞应激和DNA损伤。
近日,一篇发表在《科学·免疫学》期刊上的论文给出了答案[1]:小烧怡情,大烧伤身。
美国范德比尔特大学的Jeffrey C. Rathmell团队发现,发热温度(39°C)会显著增加CD4+T细胞的增殖和炎症效应功能,但会在其亚型TH1细胞中诱发线粒体应激和DNA损伤,进而激活p53和STING信号通路。这些损伤会导致部分TH1细胞死亡,但幸存的TH1细胞表现出增强的线粒体质量和促炎效应功能。
研究者们表示,这可能可以解释为什么长期以往的发烧和慢性炎症与癌症挂钩。

论文首页截图
在这项研究中,研究者们将小鼠的CD4+T细胞分别在常温(37°C)和发热温度(39°C)下进行体外培养,观察不同T细胞亚群的功能变化。
结果发现,发热温度能够增强CD4+T细胞的增殖能力和炎症表型,降低调节性T细胞的免疫抑制能力。CD4+T细胞的这种改变有利于维持发烧时的炎症状态,以应对病原体入侵。CD4+T细胞在39℃调节下培养后转移到常温体外培养或小鼠体内时,这些特性均能够得到保持。
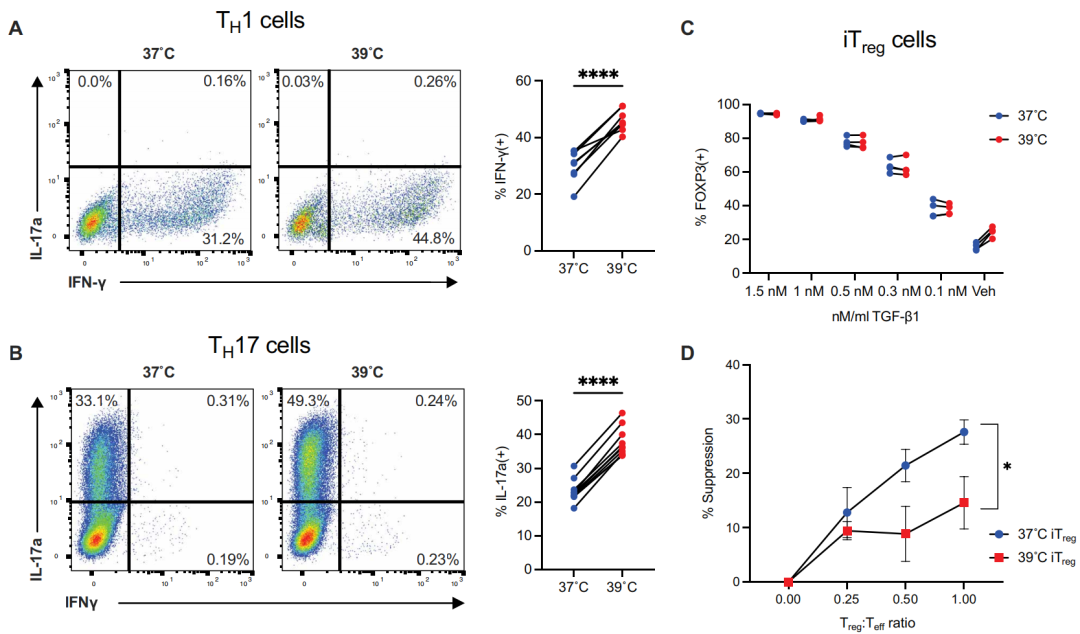
39℃会促进CD4阳性T细胞增殖和分泌炎症因子
但具体来看,不同CD4+T细胞亚群对温度升高的适应性有所差异。
通过电子显微镜分析,研究团队观察到TH1细胞中的线粒体形态在39°C下发生了明显变化,部分细胞的线粒体密度和嵴形成增加,显示其活性增强,但也检测到有TH1细胞发生线粒体功能障碍和DNA损伤。

39℃下TH1细胞的线粒体功能表现出异质性
此外,代谢分析结果显示,TH1细胞对高温的适应性较差,在39℃培养条件下糖酵解能力仅有小幅提高,其最大氧消耗速率(OCR)和备用呼吸能力(SRC)有所下降,显示出较高比例的线粒体功能障碍,线粒体电子传递链复合物1(ETC1)的功能显著下降,细胞里的活性氧(ROS)和DNA损伤标志物(γH2AX)水平升高,细胞存活率明显下降。
与TH1细胞不同,TH17细胞和Treg细胞能够很好地适应温度升高。它们在发热温度下虽然也经历了代谢的变化,但线粒体功能较为稳定,在高温下的适应能力较强,存活率保持不变。在TH17细胞中,线粒体表现出较高的基础和最大呼吸速率,更依赖于谷氨酸代谢以维持其能量需求,Treg细胞则主要依赖于糖酵解途径。
研究进一步揭示了TH1细胞暴露于39°C后究竟遭遇了哪些磨难。
结果显示,问题源头是能量工厂的“元件”被热坏了——发热温度会迅速导致线粒体中的复合物ETC1损伤。ETC1功能损伤导致电子传递效率下降,增加线粒体活性氧的生成,诱发DNA受损和肿瘤抑制蛋白p53、STING信号通路的激活,进而促进DNA修复,或是将彻底没救的细胞送向死亡,以保持基因组的完整性。
相比于其他CD4+T细胞亚群,TH1细胞更依赖于ETC1获得能量。因此,由于ETC1的温度敏感性,TH1细胞在39℃的发热温度下更加脆弱,线粒体遭受巨大压力,DNA受损,并通过p53和STING信号通路诱导其凋亡。然而,也有幸存者,部分TH1 细胞线粒体发生适应性改变,表现出线粒体质量增加,并维持其基因组完整性。
炎症疾病通常伴随着温度变化,无论是全身性的发热还是局部组织的温度升高。基因组测序结果显示,慢性炎症(如克罗恩病、类风湿性关节炎)患者的TH1细胞表现出与小鼠模型相似的高水平炎症因子IFN-γ,以及线粒体功能障碍和DNA损伤模式。这支持了高温与TH1细胞的炎症反应加强以及DNA损伤之间的关联。
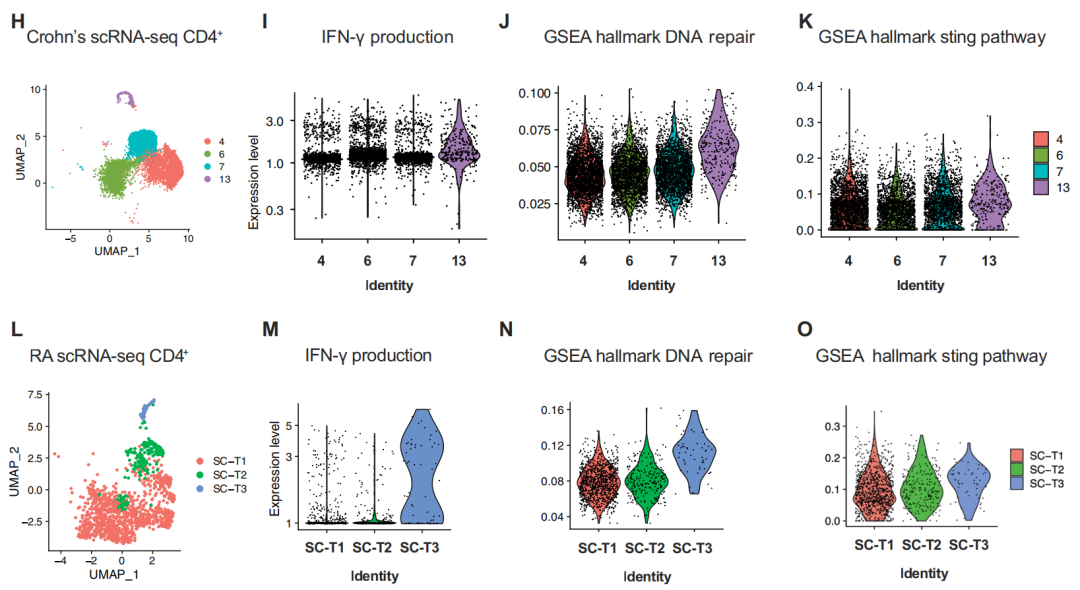
慢性炎症患者的TH1细胞也发生与小鼠模型相似的变化
这项研究强调了高温对T细胞功能和基因组稳定性的复杂影响。发烧能够让CD4+T细胞更好地发挥保护性免疫反应,但是也会引起细胞应激和DNA损伤。
发热导致的线粒体功能障碍可能是引发与炎症相关癌症突变的一个重要来源。持续的发烧情况下,DNA损失的TH1细胞在p53和STING通路的诱导下死的死、进化的进化,但长久以往难免会有细胞成为漏网之鱼,逃避修复或死亡,最终走向恶性转化的道路。
论文作者表示[2],持续的慢性炎症伴随高温可能解释了一些细胞如何变成肿瘤细胞,并指出多达25%的癌症与慢性炎症有关。
“人们问我,‘发烧是好还是坏?”作者谈论道,“简而言之,小发烧是好事,烧大了就不好了,现在我们找到了发烧有害的机制。”
参考文献:
[1]https://www.science.org/doi/10.1126/sciimmunol.adp3475
[2]https://news.vumc.org/2024/09/20/fever-drives-enhanced-activity-mitochondrial-damage-in-immune-cells/
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


