Nature子刊:新型LNP,靶向骨髓造血干细胞递送mRNA
来源:生物世界 2024-12-01 10:27
数据表明,在不使用靶向配体修饰的情况下,使用脂质纳米颗粒(LNP)靶向非人灵长类动物的造血干细胞(HSC)和造血干细胞/祖细胞(HSPC)进行体内mRNA的递送是可行的。
佐治亚理工学院和埃默里大学医学院的研究人员在 Nature 子刊 Nature Biotechnology 上发表了题为:Lipid nanoparticle-mediated mRNA delivery to CD34+ cells in rhesus monkeys 的研究论文。
该研究开发了一种名为LNP67的脂质纳米颗粒(LNP),无需骨髓动员或化疗预处理,且不使用靶向配体修饰,能够以低至0.25 mg/kg的剂量将mRNA递送到恒河猴的造血干细胞/祖细胞(HSPC)中。

此前的研究显示,使用CD117抗体修饰的LNP可将mRNA递送至小鼠骨髓。但这些研究的一个潜在局限性在于,根据人类蛋白图谱,人类CD117蛋白在呼吸系统中高表达,而在骨髓中低表达。在另一种方法中,基于腺病毒的递送系统主动靶向CD46 (CD46在小鼠和人类HSC中表达),实现了在非人灵长类动物中的高效递送。然而,这种方法也需要细胞动员和化疗。因此,在没有主动靶向配体或任何其他干预措施的情况下,在非人灵长类动物中进行临床相关剂量的LNP递送,被证明是困难的。
在这项最新研究中,研究团队报道了一种名为LNP67的脂质纳米颗粒(LNP),它以低至0.25 mg/kg的剂量将mRNA递送到恒河猴的CD34+细胞。
目前,FDA批准的三种LNP-RNA药物均使用四组分LNP,这四种组分分别是可电离脂质、辅助脂质(磷脂)、胆固醇和聚乙二醇化脂质。所有这四种成分都可以改变LNP在体内的行为,但利用细胞培养预测LNP在体内的趋向性是困难的。
在这项新研究中,研究团队使用4种不同的磷脂和4种聚乙二醇化脂质组合(共16种组合),再结合8个不同的摩尔比,生成了128种化学性质不同的LNP。分别使用这些LNP递送DNA条形码和编码糖基化磷脂酰肌醇(GPI)锚定的骆驼VHH抗体(aVHH)的mRNA。然后,分析所有这128种LNP的流体动力学直径和多分散性,将直径小于200纳米的单分散的LNP(共105种)混合在一起。
考虑到造血干细胞(HSC)数量稀少,并且难以分离出足够的细胞以便使用流式细胞术进行测序,研究团队使用他们此前开发的单细胞纳米颗粒靶向测序(SENT-seq)技术【2】评估了上述105种LNP在体内靶向小鼠骨髓递送RNA的效果。
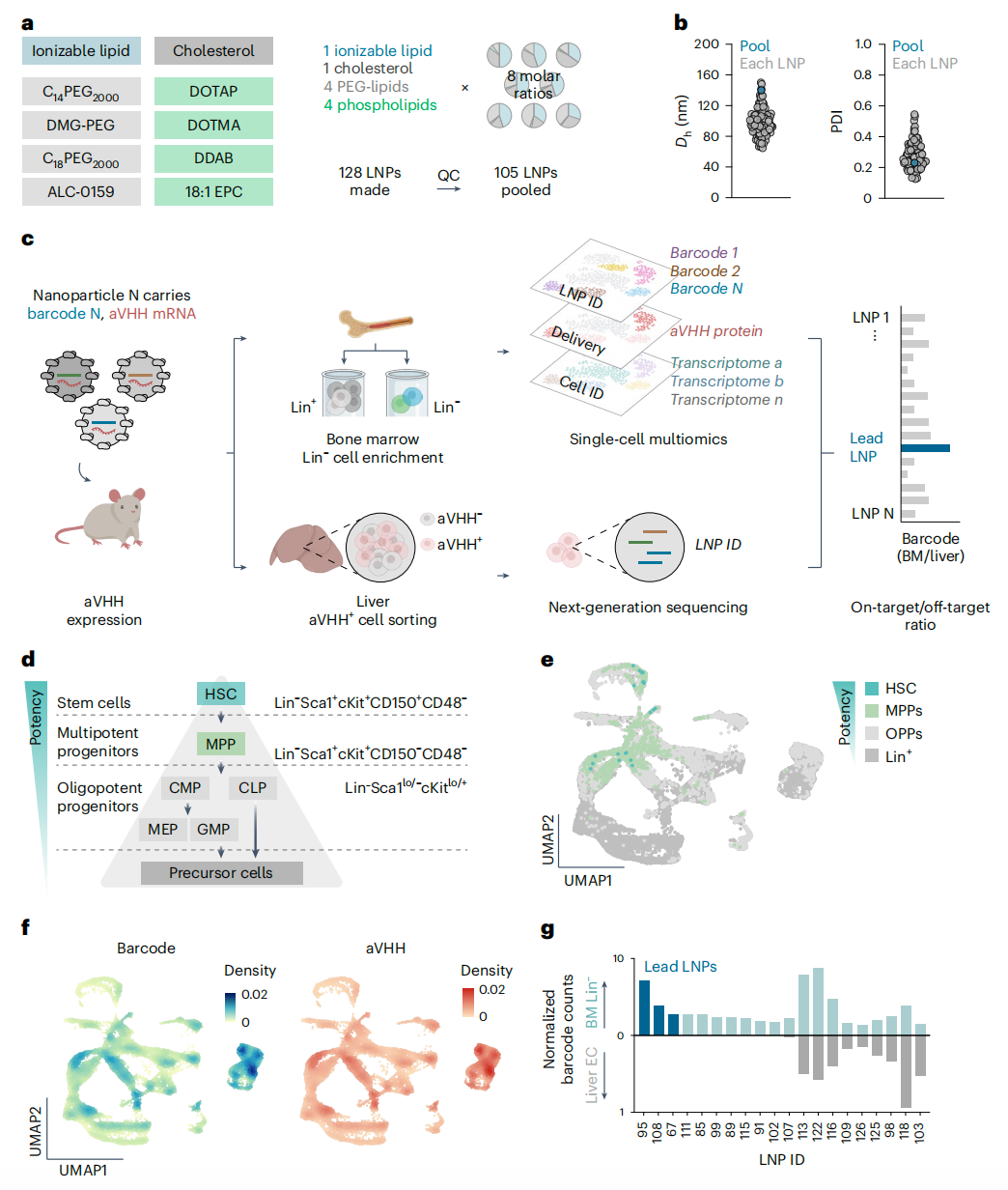
评估结果显示,LNP67能够很好地将mRNA靶向递送到小鼠骨髓以及体外培养的人类原代造血干细胞,还能够以0.25 mg/kg和0.4 mg/kg的剂量将mRNA递送到恒河猴体内的CD34+细胞(CD34是造血干细胞/祖细胞的生物标志物)。
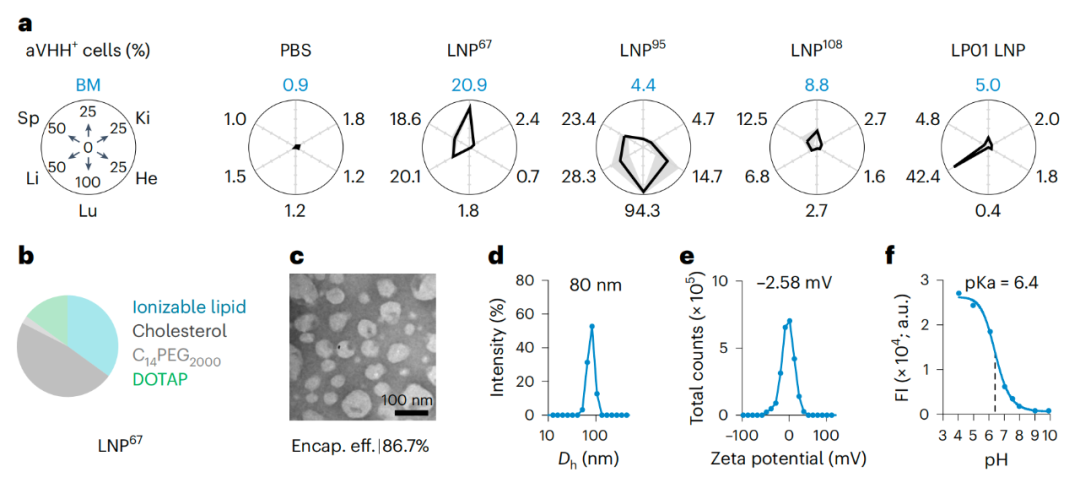
在没有骨髓动员和预处理的情况下,LNP67可将mRNA递送到恒河猴的造血干/祖细胞(HSPC)以及肝脏,而无需血清细胞因子激活。
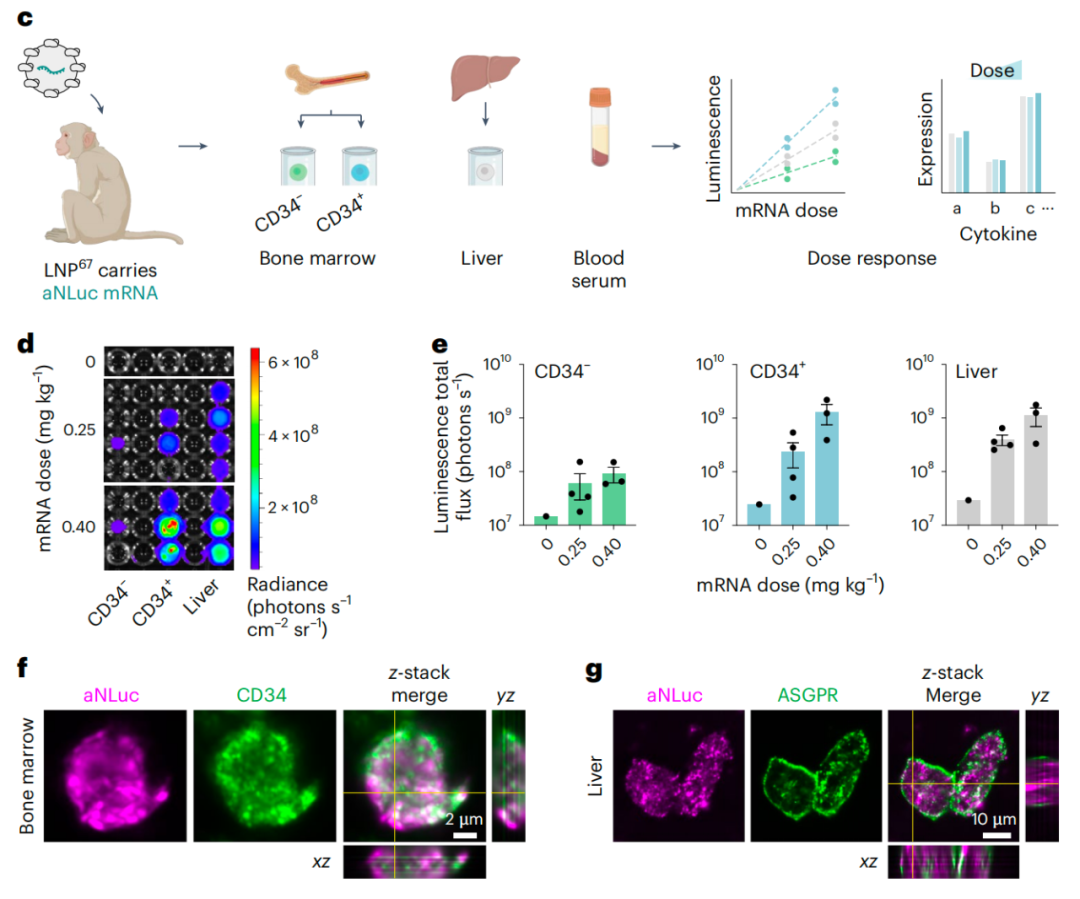
这些数据表明,在不使用靶向配体修饰的情况下,使用脂质纳米颗粒(LNP)靶向非人灵长类动物的造血干细胞(HSC)和造血干细胞/祖细胞(HSPC)进行体内mRNA的递送是可行的。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


