Nat Med:识别出多发性骨髓瘤逃脱靶向性免疫疗法攻击的特殊分子机制
来源:生物谷原创 2023-09-05 11:49
来自迈阿密大学米勒医学院等机构的科学家们通过研究揭示了为何一些多发性骨髓瘤会对最开始有效的T细胞疗法产生耐药性。
B细胞成熟抗原(BCMA, B cell maturation antigen)靶点丢失被认为是介导多发性骨髓瘤对抗BCMA前和抗原受体T细胞(CAR-T)疗法或双特异性T细胞衔接器(TCE)疗法的罕见事件,现有数据表明,下调G蛋白偶联受体家族C群5成员D(GPRC5D)蛋白常常会发生在抗GPRC5D CAR-T细胞疗法治疗复发的时候。近日,一篇发表在国际杂志Nature Medicine上题为“Tumor Intrinsic Mechanisms of Antigen Escape to Anti-BCMA and Anti-GPRC5D Targeted Immunotherapies in Multiple Myeloma”的研究报告中,来自迈阿密大学米勒医学院等机构的科学家们通过研究揭示了为何一些多发性骨髓瘤会对最开始有效的T细胞疗法产生耐药性。
如果目标T细胞所追踪的抗原发生突变,并从“雷达屏幕”上消失,其就会变得无用。这项研究中,研究人员报告了阻挠免疫疗法的突变,这些免疫疗法旨在再多发性骨髓瘤中寻找两个靶点,并允许此前治疗的癌症适应、躲避疗法和复发。医学博士Francesco Maura说道,识别出这些突变并更深入地理解这些潜在免疫疗法的耐药性机制或许是至关重要的;这些知识在帮助设计定制化的策略并未个别患者选择产品和目标方面做出明智选择方面发挥着重要的作用。
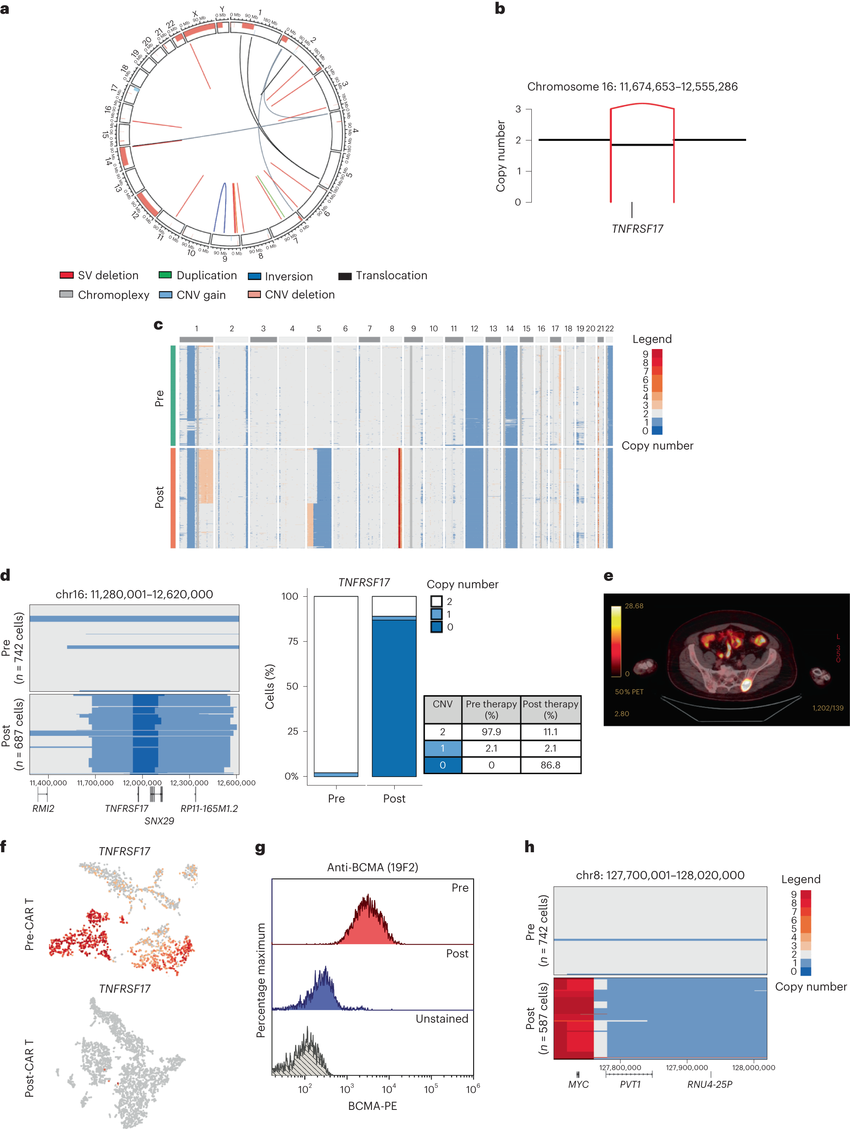
识别出多发性骨髓瘤逃脱靶向性免疫疗法攻击的特殊分子机制。
图片来源:Nature Medicine (2023). DOI:10.1038/s41591-023-02491-5
抗原漂移(Antigenic drift)是肿瘤用来对免疫疗法产生耐受性的机制,在这项涉及30名患者的研究中,研究人员重点关注了浆细胞上两个潜在靶点所发生的改变,即B细胞成熟抗原(BCMA)和G蛋白偶联受体家族C群5成员D(GPRC5D)蛋白;嵌合抗原受体T细胞(CAR-T细胞)以及双特异性T细胞衔接器(TCE)是能被工程化改造来靶向作用这些抗原的免疫疗法,如今其已经被证明在治疗复发性或对疗法耐受性的多发性骨髓瘤中展现出了一定的希望。
然而,随着时间推移,以及随着癌症发生改变,治疗效果往往会减弱,目前很少有研究能确定这种临床反应减少的原因,而这也被认为是首个对癌细胞内在机制的基因组学研究,这种机制能允许抗原在接受这些免疫疗法治疗后发生复发的患者中发生逃逸。如今研究人员发现了对抗-BCMA和抗-GPRC5D免疫疗法产生耐药性的独特而又新型的基因组事件,本文研究的另外一个重要方面在于,BCMA细胞外结构域的突变或许具有明显的效应,其能阻碍治疗性T细胞的结合,而不会对蛋白质的表达或下游信号通路产生任何影响,这一研究发现表明,骨髓瘤患者因抗原逃逸而发生复发的比例要比最初预期要广泛地多。
最后研究者表示,这些突变事件的发现或许会促使多发性骨髓瘤复发,从而就强调了对患者进行这些突变体筛选的关键必要性;此外,详细描述这些结合相互作用的特征或许也能允许科学家们合理设计新一代的T细胞重定向制剂,并未这些免疫治疗方法的最佳测序和组合提供宝贵的信息。(生物谷Bioon.com)
原始出处:
Lee, H., Ahn, S., Maity, R. et al. Mechanisms of antigen escape from BCMA- or GPRC5D-targeted immunotherapies in multiple myeloma. Nat Med (2023). doi:10.1038/s41591-023-02491-5
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


