Sci Adv:徐进/余涛团队合作阐明斑马鱼胚胎小胶质细胞的来源
来源:生物探索 2024-09-05 14:40
该研究通过更加可靠的遗传工具和实验方法,阐明了斑马鱼胚胎小胶质细胞全部来自于髓系造血并依赖髓系转录因子Pu.1,提示先前报道的不依赖于Pu.1且起源于淋巴管的小胶质细胞并不存在。
华南理工大学医学院徐进教授团队和深圳北京大学香港科技大学医学中心/深圳湾实验室余涛副研究员团队合作在Science Advances发表题为The embryonic zebrafish brain is exclusively colonized by pu.1-dependent and lymphatic-independent population of microglia的研究论文。研究团队利用在pu.1基因敲入的斑马鱼品系,并结合严谨的谱系追踪及突变体分析,阐明了斑马鱼胚胎中的小胶质细胞全部来自于髓系造血,并依赖于转录因子Pu.1,否认了先前报道的来自于淋巴管的小胶质细胞的存在。

为了回答斑马鱼胚胎大脑中是否可能存在此前报道的pu.1阴性,mrc1a及4C4(小胶质细胞特异性抗体)阳性的小胶质细胞,研究人员将pu.1敲入品系pu.1KI-DsRed 与 Tg (mrc1a:egfp) 转基因鱼杂交,并在不同时期进行 GFP、DsRed 和 4C4的免疫染色。结果显示,所有mrc1a+4C4+的小胶质细胞均为pu.1阳性。研究者进一步对早期发育阶段的斑马鱼胚胎进行免疫染色后发现,在受精后36小时,48小时和72小时(hpf)的斑马鱼胚胎中所有的mrc1a+4C4+小胶质细胞(前体)也均为pu.1阳性。此外,通过观察红细胞特异性标记的转基因鱼,研究人员发现关于小胶质细胞从淋巴管生成的研究中所观察到的淋巴管实际上是有血液循环的血管。综上所述,斑马鱼幼鱼中不存在mrc1a+pu.1-的小胶质细胞,小胶质细胞也非来源于mrc1a+pu.1-的前体细胞。
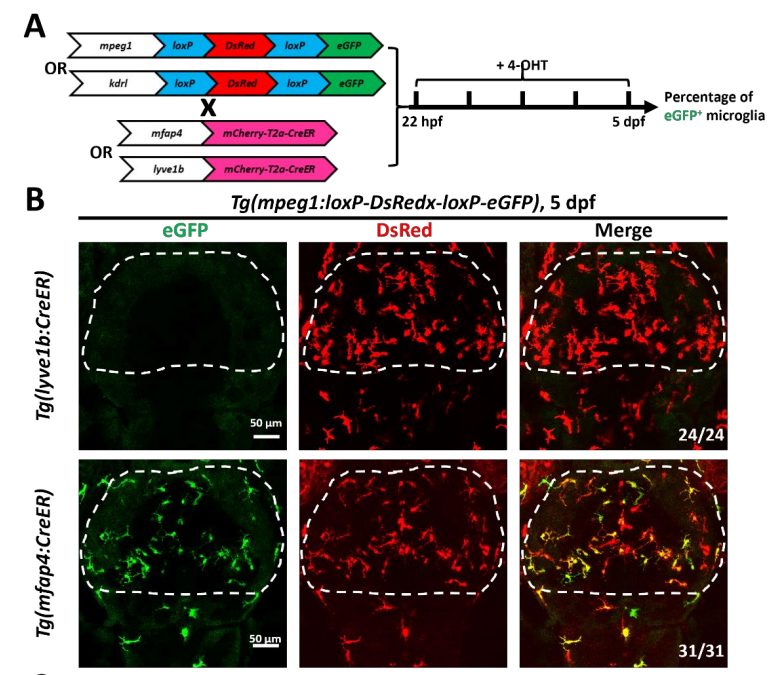
图1-谱系追踪结果显示斑马鱼胚胎大脑中的小胶质细胞来自于髓系造血,而非淋巴管(Credit: Science Advances)
为了更好地揭示斑马鱼胚胎小胶质细胞的来源,研究者利用标记淋巴管和静脉内皮细胞的 Tg(lyve1b:CreER) 转基因鱼与标记巨噬细胞/小胶质细胞的转基因鱼Tg(mpeg1:loxP-DsRedx-loxP-eGFP) 杂交后的胚胎进行谱系追踪。结果显示通过22 hpf 至 5 dpf 期间用4-羟基他莫昔芬 (4-OHT) 持续浸泡,淋巴管驱动的CreER并不能对斑马鱼幼鱼大脑中的小胶质细胞进行标记。相反地,利用标记巨噬细胞/小胶质细胞的Tg(mfap4:CreER)转基因鱼与转基因鱼Tg(mpeg1:loxP-DsRedx-loxP-eGFP)杂交后的胚胎进行谱系追踪,却能够很好地标记5 dpf时期斑马鱼幼鱼脑部的小胶质细胞 (图1)。此结果说明斑马鱼大脑中的小胶质细胞并非来源于lyve1b+的淋巴管。接下来,研究团队对淋巴管缺陷的突变体flt4ihb439和 ccbe1sa1019中小胶质细胞的数量进行了统计,发现突变体中的小胶质细胞也并无减少,进一步说明淋巴管对于小胶质细胞的发育并无作用。相反地,髓系转录因子pu.1基因突变体pu.1Δ839中小胶质细胞几乎完全缺失。
综上所述,该研究通过更加可靠的遗传工具和实验方法,阐明了斑马鱼胚胎小胶质细胞全部来自于髓系造血并依赖髓系转录因子Pu.1,提示先前报道的不依赖于Pu.1且起源于淋巴管的小胶质细胞并不存在。同时,该项研究还强调了使用可靠的遗传工具的重要性,并提醒从业者在生物研究中使用化学抑制剂和瞬时sgRNA阻断时要谨慎地得出结论。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


