《癌细胞》:中国医学科学院肿瘤医院王洁/王志杰团队提出,基于ctDNA的免疫分型,能助力晚期肺癌免疫+化疗方案精准分层施治!
来源:奇点糕 2024-09-18 10:27
结合此前分析的发现,bGIS-2亚组应该是最适合免疫+化疗方案的患者,数据分析也证实了这一点,但免疫+化疗方案的PFS和长期OS获益主要在非腺癌患者中体现。
近日,中国医学科学院肿瘤医院王洁、王志杰领衔的团队与国内众多专家合作,在Cancer Cell期刊发表的最新研究成果,提出了全新的精准分型策略:可通过检测晚期NSCLC患者的ctDNA,明确基于外周血的基因组特征免疫分型(bGIS),由此指导免疫+化疗方案使用[1]。
研究者们分析了临床III期关键研究CHOICE-01(评估PD-1抑制剂特瑞普利单抗+化疗用于一线治疗)460例入组患者的ctDNA样本,发现基于血液的肿瘤突变负荷(即bTMB)、染色体不稳定性(bCIN)等分子特征可预测免疫+化疗方案疗效,但单一特征的预测效能有限,而综合各种分子特征得到的bGIS分层策略,可准确将患者细分为治疗应答和预后不同的三个亚组(bGIS-1/2/3),且不同亚组肿瘤内在特征也有显著差异,显示了分层的合理性。
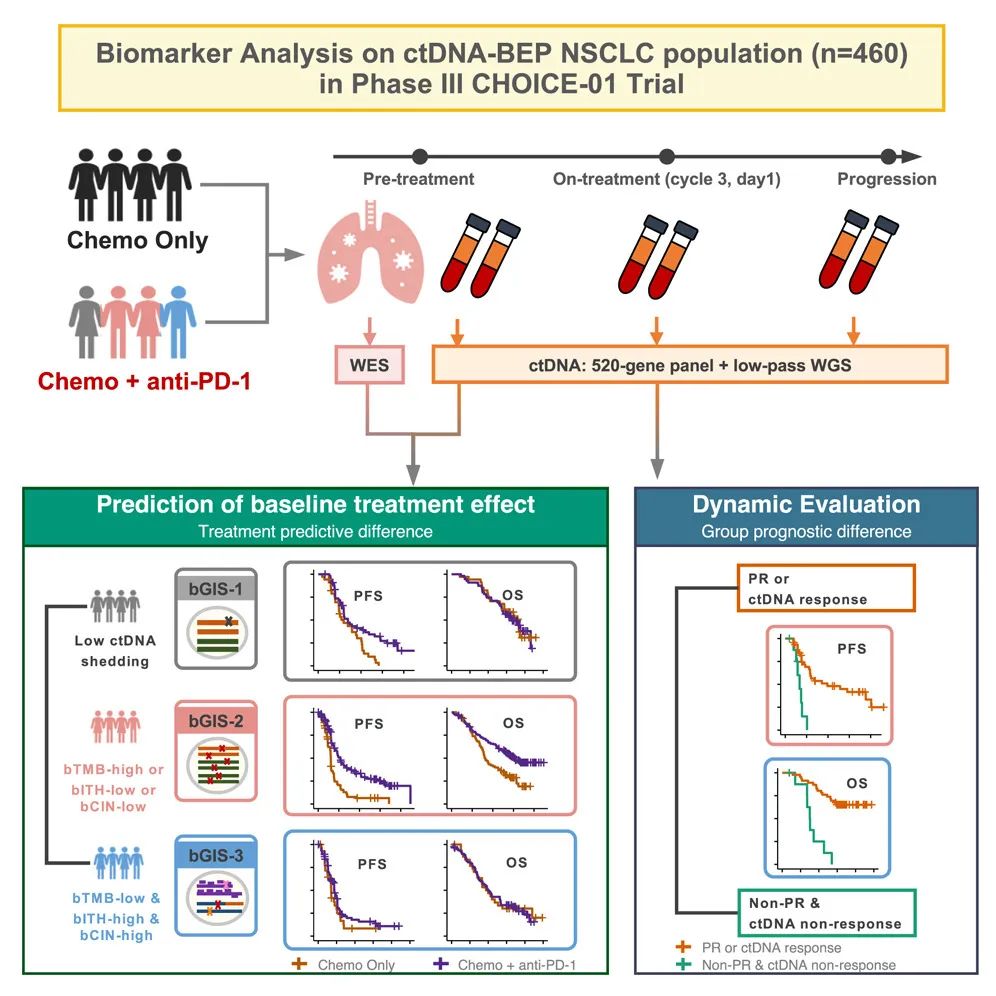
一图总结论文核心内容
CHOICE-01研究的主要结果已在去年以论文形式正式发表[2],奇点糕就不多赘述了,而本次分析囊括了CHOICE-01研究的几乎全部意向治疗人群(ITT, n=465),主要分析方法是对前瞻性收集的患者基线时血样进行二代测序(NGS),评估基于ctDNA获得的基因组特征,此外还对相应配对且充足的患者肿瘤组织样本进行全外显子组测序(WES)。
分析首先显示,基线时ctDNA为阴性【定义为最大体细胞等位基因频率(MSAF<0.5%)】的患者整体预后较好,但同时与化疗对照组相比,让PD-1抑制剂加入治疗并不能显著提升客观缓解率(ORR)和中位无进展生存期(mPFS)/总生存期(mOS);免疫+化疗方案对比化疗的优势,主要是在基线时ctDNA为阳性的患者中显现的。
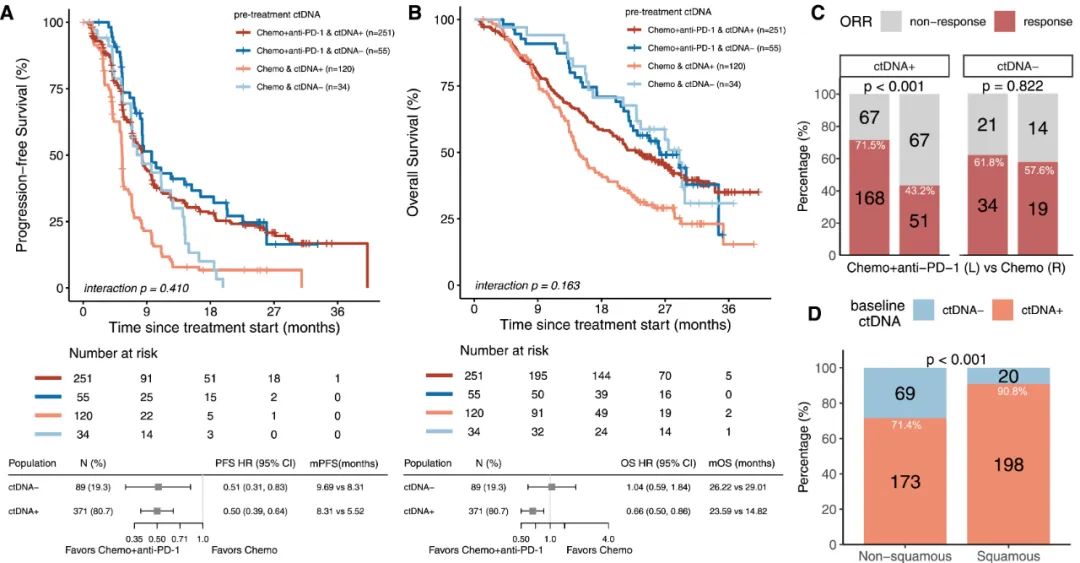
按患者基线时ctDNA状态,对免疫+化疗组和化疗组的疗效数据进行的细分评估
而单独以基线时ctDNA的检测关键指标,如MSAF或拷贝数变异(CNV)-肿瘤分数(TF),都不能有效预测免疫+化疗方案的治疗应答,那就得继续挖掘更多基因层面特征,但研究者们相继评估了bTMB、bCIN以及肿瘤内异质性(bITH)等多种特征,发现它们往往只对患者PFS和OS其中之一有明确预测价值,显然不足以单独作为Biomarker“挑大梁”。
单独使用不行,综合构建分型可好?研究者们整合了患者的bTMB、bCIN和bITH特征,再加上前面提到的基线时ctDNA阴性,获得了可有效预测免疫+化疗方案获益的bGIS分型策略,三个亚组的特征如下:
bGIS-1:基线ctDNA阴性亚组;
bGIS-2:携带任一可预测免疫+化疗方案获益的分子特征(bTMB-high、bITH-low、bCIN-low)亚组;
bGIS-3:不携带任何上述分子特征的亚组(即bTMB-low、bITH-high、bCIN-high)。
结合此前分析的发现,bGIS-2亚组应该是最适合免疫+化疗方案的患者,数据分析也证实了这一点,但免疫+化疗方案的PFS和长期OS获益主要在非腺癌患者中体现。研究者们又用两个在我国开展,设计、治疗模式乃至测序平台都相同的临床III期关键研究(RATIONALE-304/307)作为外部独立验证队列,证实了bGIS分型策略的可重复性和可靠性。
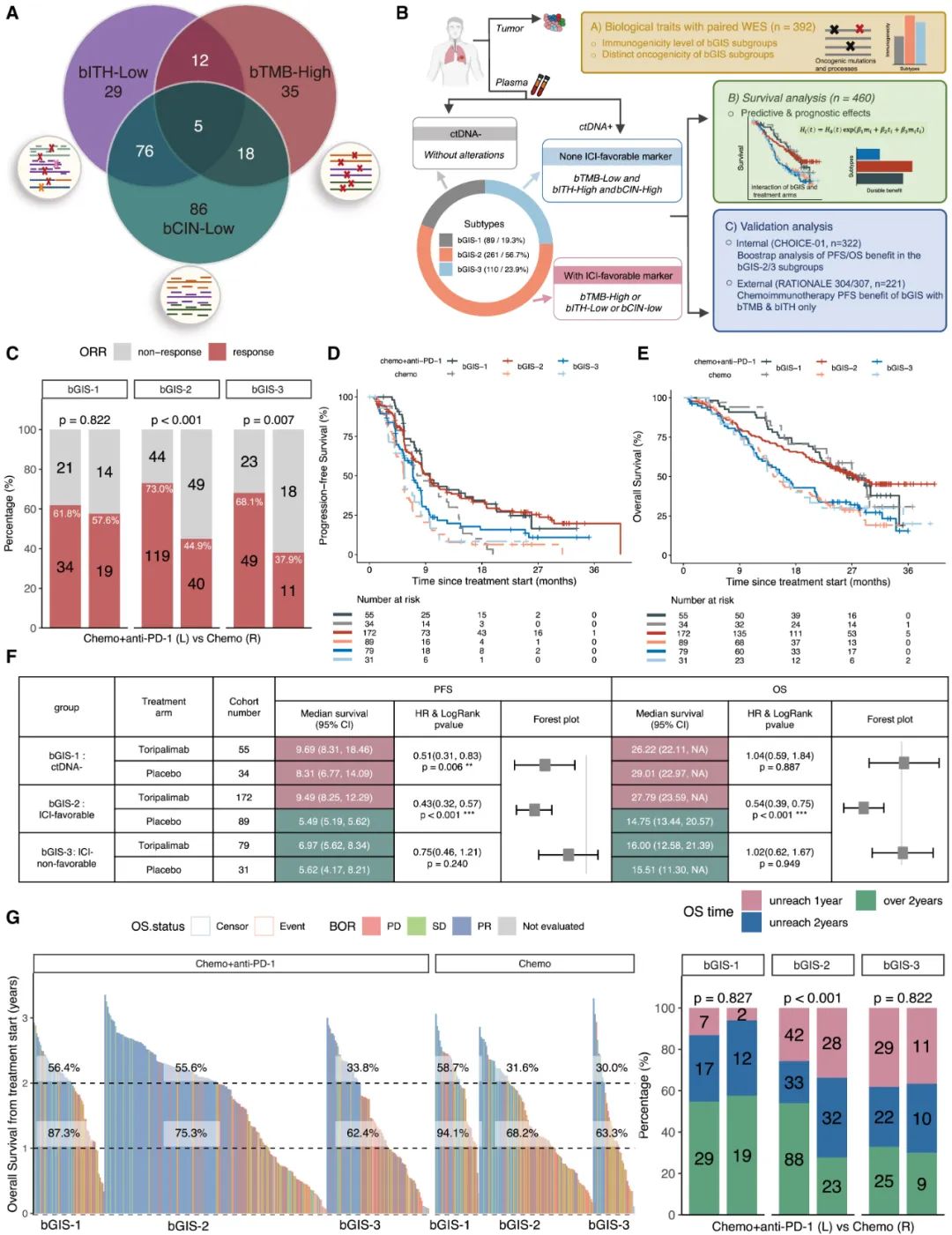
bGIS分型的提出过程和相关数据分析
对患者配对肿瘤组织样本的WES分析则显示,不同bGIS亚组的内在肿瘤分子特征确实不一样,如bGIS-1亚组的TMB水平和肿瘤新抗原负荷最低,bGIS-2亚组的TMB水平则显著更高,所以免疫原性更好,更适合免疫+化疗方案,bGIS-3亚组则多见合并KEAP1/NFE2L2等不利于免疫治疗的共突变,这些都能说明bGIS分型确实有合理性。
此外,研究还对治疗期间部分患者的外周血ctDNA动态变化进行了分析,发现“ctDNA应答”乃至“ctDNA清除”等指标,也可与影像学疗效评价互为补充,更好地预测治疗应答和患者长期生存;最后,研究者们综合各项发现,提出了基于ctDNA检测的驱动基因阴性晚期NSCLC分层治疗策略,要点包括可考虑将bGIS-1亚组的免疫治疗使用后置,强烈推荐bGIS-2亚组一线使用免疫+化疗方案,进一步探索bGIS-3亚组理想的一线治疗方案等。
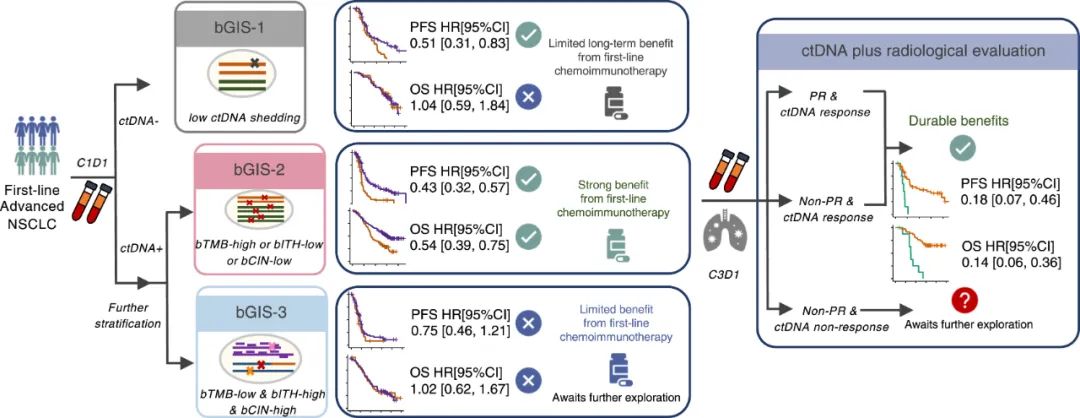
基于ctDNA检测的驱动基因阴性晚期NSCLC分层治疗策略要点
参考文献:
[1]Xu J, Wan R, Cai Y, et al. Circulating tumor DNA-based stratification strategy for chemotherapy plus PD-1 inhibitor in advanced non-small-cell lung cancer[J]. Cancer Cell, 2024, 42(9): 1598-1613. e4.
[2]Wang Z, Wu L, Li B, et al. Toripalimab plus chemotherapy for patients with treatment-naive advanced non–small-cell lung cancer: a multicenter randomized phase III trial (CHOICE-01)[J]. Journal of Clinical Oncology, 2023, 41(3): 651-663.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


