Cell Rep:科学家识别出能控制乳腺癌转移到大脑中的新型分子通路
来源:生物谷原创 2023-12-27 16:16
来自Moffitt癌症研究中心等机构的科学家们通过研究更好地理解了促进乳腺癌脑转移的发生和进展的分子机制,从而有望帮助开发新型诊断和治疗方法。
乳腺癌是导致癌症大脑转移的第二大常见原因,10%至30%的转移性乳腺癌患者都会都发生癌症脑转移,发生脑转移的乳腺癌患者往往治疗选择非常有限且生存率较差;近日,一篇发表在国际杂志Cell Reports上题为“Brain metastasis-associated fibroblasts secrete fucosylated PVR/CD155 that induces breast cancer invasion”的研究报告中,来自Moffitt癌症研究中心等机构的科学家们通过研究更好地理解了促进乳腺癌脑转移的发生和进展的分子机制,从而有望帮助开发新型诊断和治疗方法。
文章中,研究者识别出了一种能控制乳腺癌脑转移的新型细胞信号通路,研究人员重点分析了癌症相关成纤维细胞和岩藻醣化过程(fucosylation),癌症相关成纤维细胞是肿瘤环境中一类特殊的细胞类型,其能支持并促进癌症发生和进展。癌症相关成纤维细胞因其在原发性乳腺癌发生过程中的贡献而得到证实,然而,其在癌症脑转移过程中所扮演的关键角色,研究人员并不清楚。岩藻醣化是一类特殊的蛋白质修饰过程,即将糖类L-岩藻糖(L-fucose)添加到蛋白质中,从而就会影响其行为和功能,细胞信号通路能被岩藻醣化所调节,而且高水平的岩藻醣化蛋白似乎与乳腺癌进展过程直接相关。
研究者Eric Lau表示,新兴研究强调了岩藻醣化在多种癌症类型发病机制中所扮演的关键作用,包括脑癌等,然而,异常的岩藻醣化大白如何改变肿瘤相关的成纤维细胞的相互作用从而促进大脑肿瘤进展,目前我们并不清楚。在早期实验中,研究人员发现,乳腺癌相关的成纤维细胞含有高水平与癌症转移相关的岩藻醣化过程,这就表明,癌症成纤维细胞或许在这一过程中会促进乳腺癌进展。
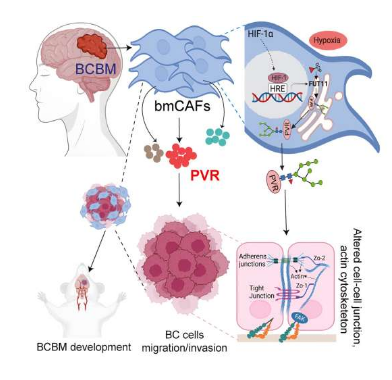
科学家识别出能控制乳腺癌转移到大脑中的新型分子通路。
图片来源:Cell Reports (2023). DOI:10.1016/j.celrep.2023.113463
随后一系列综合实验结果表明,来自乳腺癌脑转移中的癌症相关成纤维细胞能分泌脊髓灰质炎病毒受体蛋白(PVR,protein poliovirus receptor),其能有效刺激转移性乳腺癌细胞的迁移和侵袭能力,并增加大脑中乳腺癌细胞的侵袭。重要的是,研究人员确定,来自成纤维细胞中PVR的分泌是通过岩藻醣化作用所诱发的,而这是由缺氧诱导蛋白FUT11所介导的;此外,研究人员还在患者机体的样本中证实,来自乳腺癌脑转移的癌症相关成纤维细胞中岩藻醣化的PVR的水平要比乳腺癌细胞中的高。
这些综合性观察结果表明,PVR岩藻醣化以及随后由癌症相关成纤维细胞分泌或许是大脑中乳腺癌转移和侵袭的重要调节子,研究人员希望这些研究发现或能帮助科学家们设计出针对乳腺癌脑转移患者的更好的诊断和治疗性策略。研究者Emma Adhikari博士说道,我们的研究为阐明乳腺癌脑转移的发病机制首次提出了重要的机制性见解,同时强调了大脑转移性癌症相关成纤维细胞分泌/岩藻醣化的PVR和FUT11或能作为乳腺癌脑转移的新型治疗性靶点和生物标志物。
综上,本文研究描述了一种缺氧和岩藻醣化调节的机制,其中脑转移的癌症成纤维细胞或能促进乳腺癌脑转移在大脑中的侵袭和扩散。(生物谷Bioon.com)
原始出处:
Emma Adhikari,Qian Liu,Joseph Johnson, et al. Brain metastasis-associated fibroblasts secrete fucosylated PVR/CD155 that induces breast cancer invasion, Cell Reports (2023). DOI:10.1016/j.celrep.2023.113463
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


