Nature Methods:振动光纤光度法(vibrational fiber photometry)——重塑脑分子研究未来
来源:生物探索 2025-01-07 09:15
这种方法通过直径仅为1微米的渐细光纤探针,可最小化组织损伤并深入小鼠大脑内部,实时监测脑组织的分子组成变化。
在探索脑功能的过程中,如何无创且精确地捕捉深层脑区的分子动态一直是研究者面临的巨大挑战。现有技术,如荧光标记的基因编码分子传感器,虽在神经活动监测中取得了巨大的成就,但其依赖荧光标记的特性使其在复杂生物分子信息的全面呈现方面受到限制。尤其是当研究对象是脑深层区域时,光学噪声、分辨率限制和标记依赖性等问题更加突出。
针对这些技术瓶颈,12月31日Nature Methods的研究报道“Vibrational fiber photometry: label-free and reporter-free minimally invasive Raman spectroscopy deep in the mouse brain”,开发了一种创新性的“振动光纤光度法”(vibrational fiber photometry),这是一种基于拉曼光谱(Raman spectroscopy)的无标签、无报告分子检测技术。这种方法通过直径仅为1微米的渐细光纤探针,可最小化组织损伤并深入小鼠大脑内部,实时监测脑组织的分子组成变化。相比传统方法,振动光纤光度法以更高的信噪比揭示了脑组织的分子架构,成功捕捉了脑外伤(traumatic brain injury, TBI)和脑转移肿瘤(brain metastasis)等病理状态下的分子信号。
该研究不仅提出了一种新型的光学装置,同时结合深度学习算法,有效抑制了探针背景干扰,为分子谱数据的可靠解读提供了强有力的工具。这种技术在脑科学领域具有广阔的应用前景,不仅能用于基础神经科学研究,还可服务于疾病诊断与治疗,如癌症检测和脑损伤恢复评估。

突破光学监测瓶颈:无标签技术的新视野
在神经科学领域,光学监测技术已经成为研究脑功能的重要工具,但现有方法的局限性也逐渐显现。传统的光学手段主要依赖荧光标记,利用基因编码的分子传感器(如钙或神经递质指示剂)记录神经活动。然而,这些技术因其对光谱信号的依赖性,无法在复杂环境中精准捕捉多分子信息,尤其在研究深层脑区时,其低信噪比更是难以克服。
为解决这一瓶颈,研究者们开发了一种创新的振动光纤光度法(vibrational fiber photometry),这是基于拉曼光谱的无标签检测技术。该技术最大的突破在于,它不依赖外部标记分子,而是通过光与组织分子自然散射形成的独特“指纹”,实现对分子组成的直接检测。这种无标签方法能捕捉复杂的生物分子变化,如蛋白质、脂类和其他关键分子特征,为研究脑功能及病理变化提供了新视角。
振动光纤光度法的一大创新在于探针的设计。与传统光学探针不同,这种探针的尖端直径仅为1微米,显著降低了对脑组织的损伤,同时其渐细结构允许光信号的高效采集和传输。此外,红外激发波长的使用有效减少了组织自发荧光干扰,大幅提升了深层脑区的信号质量。
通过结合深度学习算法,振动光纤光度法进一步突破了技术限制。算法的引入成功抑制了探针本身的拉曼背景信号,使得分子数据更加清晰可靠。这一技术的独特性不仅在于其可获取多分子信息的能力,还在于其在深层脑区实现精准监测的潜力,为研究脑功能多样性及疾病发展提供了革命性工具。
深入大脑的微型探针:渐细光纤的巧妙设计
在振动光纤光度法的技术核心中,微型探针的设计是关键。这种渐细光纤(tapered fiber, TF)以其极致的微型化和功能性,突破了传统光学探针在体积和性能上的限制。探针的尖端直径仅为1微米,而渐细部分的长度为2毫米,从纤维主体到尖端呈现流畅的锥形过渡。这种设计不仅显著减少了植入过程中对脑组织的损伤,还能大幅提高光信号的收集效率和分辨率。
探针的独特结构赋予其双重功能:一方面,其极小的尖端能深入到脑组织的深层区域,覆盖从皮层到海马等多个脑区,实现高空间分辨率的分子信息采集;另一方面,探针的渐细部分通过调节光学模式的分布,扩大了信号收集的活跃区域。研究表明,这种设计有效增强了探针的光学耦合效率,使其能够捕捉到从浅表到深层脑区的连续分子谱信息。
此外,探针的材料选择也体现了巧妙的平衡。通过采用具有低光学损耗的特殊光纤材料,探针在传输光信号的同时最大程度减少了自发荧光背景的干扰。结合红外激发波长(785纳米)的使用,这种设计在深层脑区的光信号采集中表现尤为突出。实验数据表明,探针在小鼠大脑不同深度收集的拉曼信号准确反映了组织中蛋白质与脂类分子的分布变化,其光谱细节与先前报道的数据高度一致。
更重要的是,这种微型探针还具备良好的机械稳定性和灵活性,可在脑组织内实现多次插入和移除而不破坏组织结构。
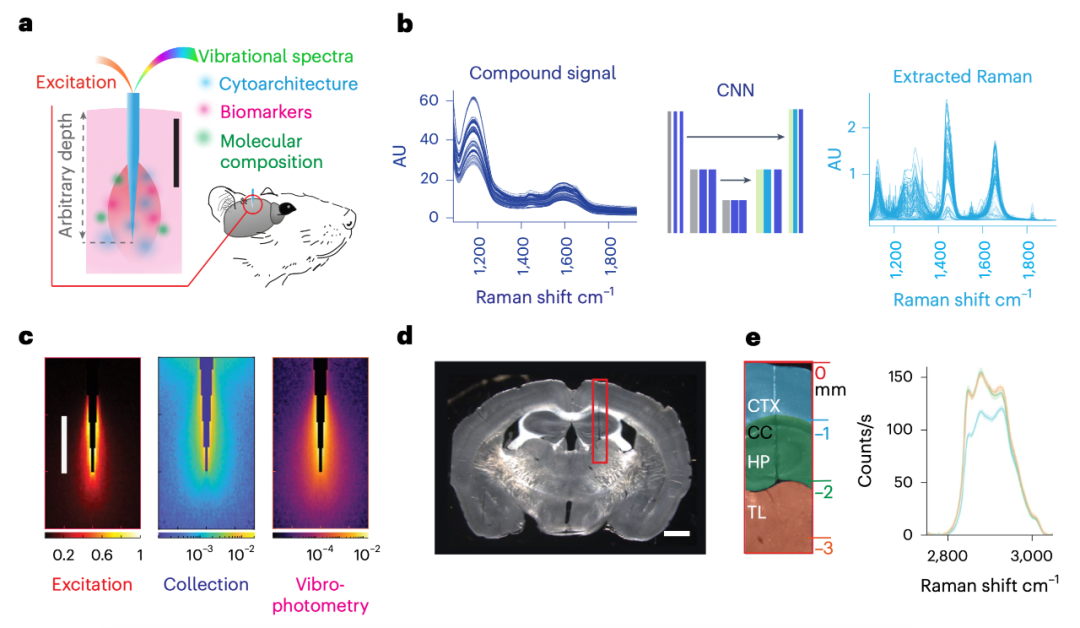
基于渐细光纤的深层脑区振动光度技术(Credit: Nature Methods)
(a) 振动光度技术的概念
图a展示了渐细光纤(tapered fiber, TF)作为神经植入探针的基本概念。该探针可以插入到脑组织的任意深度,通过自发拉曼散射(spontaneous Raman scattering)同时获取多种分子成分的信息。这一方法实现了深层脑区的无标签分子信号采集,是技术的核心创新点。
(b) 深度学习算法处理流程
图b描述了用于信号优化的卷积神经网络(Convolutional Neural Network, CNN)的处理流程。通过分块连续处理,CNN成功将光纤背景信号与脑组织拉曼信号分离,使得分子信号的解读更为清晰。这一算法显著提升了数据质量,克服了背景干扰对信号准确性的限制。
(c) 光学模型
图c展示了光学模型的数值模拟结果,包括光激发(左图)、信号采集(中图)和光度区域(右图)的分布情况。模拟采用了785 nm的激发光和885 nm的收集光波长,结果显示渐细光纤在散射介质中的光学相互作用范围具有高度均匀性。这一模型为技术优化提供了理论支持。
(d) 探针足迹
图1d通过广域成像展示了渐细光纤在脑切片中的植入轨迹(红框所示)。实验显示,探针能够在多个脑区实现精准插入且对组织损伤极小。
(e) 脑层分子信号变化
图e展示了不同脑层(如皮层、胼胝体、海马和丘脑)的分子信号特征变化。左图显示了探针轨迹的放大图,而右图通过拉曼光谱详细描述了随着探针深度增加,蛋白质与脂类含量比例的变化。这些光谱数据不仅揭示了不同脑区的分子组成差异,也验证了技术的高灵敏度和深层检测能力。
分子信号的“指纹”:拉曼光谱的魔力
每种分子都有其独特的“指纹”,而拉曼光谱正是解读这些分子指纹的关键工具。在振动光纤光度法中,拉曼光谱的核心原理源于光子与分子振动之间的相互作用。当激光照射在生物组织上时,部分散射光的能量会因分子振动而发生微小偏移,这种偏移形成了特定的光谱峰,精准映射出分子的化学组成和结构特征。
与传统的荧光标记技术相比,拉曼光谱的独特优势在于其无标签特性。它能够直接检测蛋白质、脂类和其他生物分子,而无需外源性标记物的介入。这种方法不仅避免了荧光标记可能引发的生物干扰,还能揭示生物体系中多种分子同时存在的复杂动态。这种特性在多分子环境中,尤其是神经科学研究中,提供了无与伦比的灵活性和精确性。
振动光纤光度法进一步优化了拉曼光谱在深层组织中的应用。实验数据表明,通过探针采集的拉曼光谱可以清晰区分大脑不同区域的分子特征。例如,在脑外伤模型中,研究人员观察到脂类(如在1440 cm⁻¹的拉曼峰)显著减少,而蛋白质相关的信号(如2930 cm⁻¹)在病变区域更为突出。此外,在脑转移肿瘤研究中,拉曼光谱成功捕捉到肿瘤核心区域的黑色素特征峰(如1400 cm⁻¹和1590 cm⁻¹),这些分子信号的变化为疾病诊断提供了可靠依据。
更重要的是,拉曼光谱的多光谱探测能力允许研究人员在同一时间窗口内解析多种分子的信号。这种“全景式”的分子检测,不仅提供了对局部微环境的深入理解,还能够连接神经活动与分子变化的桥梁,为揭示脑功能和病理的复杂机制开辟了新途径。
脑外伤的分子信号图谱
脑外伤(traumatic brain injury, TBI)是一种常见但复杂的脑损伤形式,其分子变化过程对于理解损伤机制和评估治疗效果至关重要。然而,传统方法在捕捉深层脑区的分子信号时往往面临技术瓶颈。振动光纤光度法以其精准的分子检测能力,成功为这一领域提供了新工具。
在该研究中,研究人员使用小鼠TBI模型,通过渐细光纤探针采集脑损伤区域的拉曼光谱。数据揭示了损伤核心区域(TBI)与损伤边缘区域(pTBI)及对侧正常脑组织(Clat)之间显著的分子差异。具体而言,在损伤核心区域,研究发现脂类相关的拉曼峰(如1440 cm⁻¹和2850 cm⁻¹)明显减弱,而蛋白质振动相关的信号(如1660 cm⁻¹的酰胺I峰)也显著下降。这一趋势与组织中细胞丢失和髓鞘脱失的病理特征相一致。
此外,在损伤边缘区域,尽管分子信号的变化不及核心区域明显,但研究仍检测到轻微的脂类减少和蛋白质信号的变化,提示了损伤波及范围可能超出肉眼可见的病变区域。这些观察通过拉曼光谱的高分辨率和灵敏度得以捕捉,证明了振动光纤光度法在检测分子级病理变化方面的优势。
值得一提的是,在伤区核心,研究还记录到1350–1400 cm⁻¹范围内信号增强的现象。这一变化可能与血清分子的外渗相关,因为IgG免疫组织化学染色显示,损伤区域存在显著的血脑屏障破坏和血液成分渗出。此外,结合2910 cm⁻¹的轻微信号增强,提示这些分子可能与炎症反应有关。
通过精准捕捉TBI的分子特征,振动光纤光度法展示了其作为诊断工具的潜力。它不仅能为脑外伤的早期识别和损伤评估提供可靠依据,还为研究损伤后炎症、神经再生等过程提供了全新的技术支持。
揭示脑转移肿瘤的隐藏信息
脑转移肿瘤(brain metastasis)是一种复杂的疾病,其微环境中的分子变化对肿瘤的诊断和治疗具有重要意义。然而,传统方法对深层脑转移区域的分子特征检测能力有限。振动光纤光度法凭借其高灵敏度的分子识别能力,在揭示肿瘤隐藏信息方面展现了卓越潜力。
在该研究中,研究人员利用渐细光纤探针,结合拉曼光谱技术,成功检测到了脑转移肿瘤区域的分子特征变化。实验显示,在肿瘤核心区域,黑色素(melanin)相关的拉曼特征峰(如1400 cm⁻¹和1590 cm⁻¹)显著增强,表明该区域的肿瘤细胞富含黑色素。这一发现为脑内黑色素瘤的诊断提供了重要的分子证据。此外,与对侧健康脑组织相比,肿瘤核心的脂类(如1440 cm⁻¹)和酰胺I(1660 cm⁻¹)峰显著减弱,进一步反映出肿瘤侵袭导致的分子组成变化。
研究还检测了肿瘤周边区域的拉曼光谱,发现此处的分子特征介于健康组织与肿瘤核心之间,提示这些区域可能是肿瘤的侵袭边缘或转移的前沿。这种现象与临床观察中肿瘤侵袭性扩散的模式相符,为进一步研究肿瘤的扩展机制和侵袭性提供了新线索。
为了提升数据分析精度,研究人员引入了深度学习算法处理拉曼光谱数据。通过去除探针背景信号,算法增强了肿瘤特征峰的显著性,使得黑色素相关信号在980 cm⁻¹和1400 cm⁻¹的强度更加清晰。此外,主成分分析(PCA)结果表明,肿瘤区域和健康组织的光谱特征能够实现高效区分,准确率达到91%。
振动光纤光度法在脑转移肿瘤检测中的成功应用,证明了其无标签、深层分子检测的独特优势。这一技术不仅为肿瘤的早期诊断提供了可能性,还为深入探索肿瘤微环境的分子机制提供了强有力的工具,具有广阔的临床转化潜力。
深度学习助力:数据解读的新工具
振动光纤光度法的成功,离不开深度学习算法在信号处理中的关键作用。由于探针本身的拉曼信号(背景噪声)会干扰分子检测,研究人员引入了卷积神经网络(Convolutional Neural Network, CNN)来优化光谱数据处理,从而提升信号的精度和可靠性。
在具体操作中,研究团队开发了一种基于级联U-Net架构的深度学习模型。该模型使用合成的拉曼信号训练,包括探针背景、真实光谱数据及噪声干扰等多种模拟成分。这种创新的训练方法,使得模型能够精准识别并剔除探针背景信号,同时保留组织拉曼信号中的关键分子特征。在实验中,经过CNN处理的光谱显示,探针背景信号在900–1300 cm⁻¹范围内几乎完全消除,使得关键分子峰(如980 cm⁻¹的黑色素和1440 cm⁻¹的脂类信号)更加突出。
这种深度学习算法不仅增强了数据质量,还优化了分子信号的可解读性。例如,在脑转移肿瘤的检测中,CNN处理后,拉曼光谱清晰显示肿瘤核心区域的黑色素峰(980 cm⁻¹和1400 cm⁻¹)以及脂类和酰胺I峰的衰减信号。这些结果为肿瘤区域的分子诊断提供了更为精确的依据。此外,在主成分分析(PCA)中,经过CNN处理的数据分类准确率大幅提升,不仅能准确区分健康组织与肿瘤组织,还能识别肿瘤周边区域的特征谱,这对揭示肿瘤扩散机制具有重要意义。
深度学习算法还展现了其在不同实验条件下的通用性。在脑外伤模型中,CNN成功剔除了由血清分子外渗引起的光谱噪声,使损伤区域的脂类减少和蛋白质变化更为显著地呈现。总的来说,深度学习的引入不仅为拉曼光谱数据解读提供了全新思路,也为无标签光学技术在神经科学中的广泛应用奠定了坚实基础。
从实验室到临床的跨越
振动光纤光度法的出现为脑科学研究注入了新的活力,而其未来的发展前景更是令人振奋。作为一种无标签、低侵入性的光学技术,它不仅在基础研究中表现出色,更有潜力走出实验室,成为临床应用的关键工具。
在脑科学领域,这一技术可以用于深层脑区分子组成的实时监测,为解析神经活动与分子变化之间的关系提供独特视角。通过精准捕捉病理状态(如脑外伤和脑转移肿瘤)中的分子变化,振动光纤光度法可帮助研究人员深入探索神经退行性疾病、脑癌和免疫系统与脑的相互作用机制。此外,这一技术还有望在脑组织发育与衰老的研究中发挥作用,为脑健康的全生命周期监测提供科学依据。
在临床应用中,振动光纤光度法有潜力在肿瘤手术中提供实时分子信息,帮助外科医生更准确地确定肿瘤切除边界。这种技术还能应用于术后监测,通过无创检测了解治疗效果和疾病复发的风险。特别是其在识别脑转移肿瘤侵袭边缘的表现,显示出它对癌症诊疗的广泛适用性。
更值得期待的是,随着微纳光学和神经技术的进步,振动光纤光度法可以进一步实现微型化和多功能化。例如,通过在光纤尖端集成微型光学元件或金属纳米结构,研究人员可以增强光信号的采集效率并实现特定分子的选择性检测。这种跨领域的技术融合将进一步推动光学神经探针从基础研究到精准医疗的全面升级。
不仅限于脑科学,这一技术在其他领域的潜在应用同样令人期待。心脏和肝脏等器官的分子检测、炎症和感染的分子成像,甚至体外培养器官(如脑类器官)中的分子研究,都可能受益于这一工具的强大性能。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


