癌症治疗迎新突破!MIT 团队改造出“隐身”CAR-NK 细胞,躲过免疫追杀还降副作用
来源:生物谷原创 2025-10-14 11:14
从 “定制化” 到 “现货化”,这场免疫细胞的 “隐身革命”,不仅让癌症治疗更高效、更安全,更让 “患者不等药” 成为可能。
在抗癌战争中,科学家们一直在寻找更智能的武器,近年来,CAR-T细胞疗法在治疗血液癌症方面取得了显著成功,但其有个致命弱点,即制备过程长达数周且价格昂贵,许多患者在等待中错失了最佳治疗时机。更令人沮丧的是,即使用患者自身的免疫细胞进行治疗,这些“改造战士”有时也会被体内的其他免疫细胞误伤从而导致治疗功亏一篑。
如今,一篇发表在国际杂志Nature Communications上题为“Selective HLA knockdown and PD-L1 expression prevent allogeneic CAR-NK cell rejection and enhance safety and anti-tumor responses in xenograft mice”的研究报告中,来自MIT和哈佛医学院等机构的科学家们通过研究成功设计出了能“隐身”的CAR-NK细胞,其不仅能有效躲避宿主免疫系统的攻击,还能更持久地对抗癌症。

现货型疗法的困境
免疫细胞疗法被誉为癌症治疗的革命性突破,截至目前,全球已有8种CAR-T疗法获批,主要用于治疗淋巴瘤、白血病等血液肿瘤。然而,个性化定制这些“活体药物”需要耗费3-6周时间且成本高达数十万美元。对于进展迅速的癌症患者来说,这段时间往往意味着病情的不可逆恶化。
科学家们一直在探索“现货型”疗法的可能性,即使用健康供体的免疫细胞提前制备、冷冻保存,随时可用于治疗,这就像建立了一个“免疫细胞血库”,患者随取随用。但这条路充满挑战,外来细胞会被患者自身的免疫系统识别为“异己”而遭到清除,就像身体会排斥移植的器官一样。
设计“隐身”免疫细胞
NK细胞(自然杀伤细胞)是人体免疫系统的第一道防线,其就像体内的“巡逻警察”一样专门负责识别并清除癌细胞和病毒感染细胞。与CAR-T细胞相比,CAR-NK细胞具有独特优势,其不会引起严重的移植物抗宿主病,这意味着供体细胞可以安全地用于不同个体。文章中,研究人员决心解决供体细胞被排斥的难题。通过深入研究免疫细胞间的相互作用,他们发现了一个关键机制,即CD8+T细胞是介导异体排斥的主要细胞类型,而这一过程依赖于NK细胞表面的HLA class I蛋白。
研究者Rizwan Romee教授解释道,这就像给了免疫系统一个攻击靶点,如果我们能隐藏这个靶点,供体细胞就能在患者体内‘隐身’。
于是,研究团队想出了一个解决方案——给 NK 细胞设计一套 “三位一体” 的基因改造方案。首先,他们筛选出一种特殊的 shRNA(小干扰 RNA),能精准降低 NK 细胞表面 HLA-ABC 的表达,却不影响另一种关键蛋白 HLA-E——HLA-E 能与宿主 NK 细胞的抑制性受体 NKG2A 结合,避免 NK 细胞被自身免疫细胞误杀。这种 “精准敲除” 就像给 NK 细胞的 “识别标签” 做了伪装,既隐藏了被 CD8⁺T 细胞攻击的靶点,又保留了躲避自身 NK 细胞的 “保护信号”。
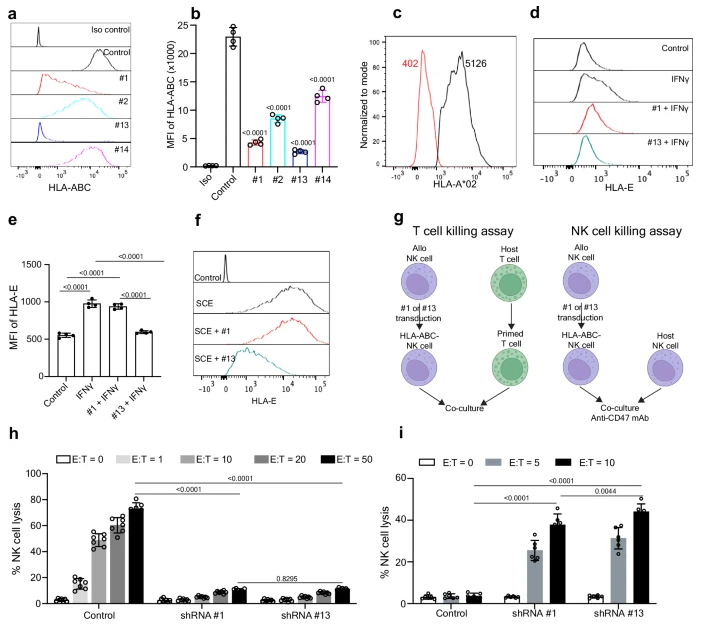
HLA-ABC减少的异体NK细胞能逃避宿主CD8+ T细胞的杀伤
在人源化小鼠模型中,这套 “隐身系统” 的效果得到了验证。研究人员给小鼠注射人类淋巴瘤细胞后,分别输注普通 CAR-NK 细胞和改造后的 “隐身” CAR-NK 细胞。结果显示,普通 CAR-NK 细胞在两周内就被小鼠的 CD8⁺T 细胞完全清除,肿瘤快速复发;而 “隐身” CAR-NK 细胞在三周后仍能检测到大量存活,且保持强效杀癌能力——小鼠肿瘤体积大幅缩小,部分甚至完全消失。更意外的是,改造后的细胞还能上调颗粒酶 B、穿孔素等细胞毒性基因的表达,同时减少耗竭相关基因的激活,意味着它们能更持久地对抗癌症。
安全性上的突破同样关键。CAR-T 疗法常见的致命副作用 “细胞因子释放综合征(CRS)”,在这套系统中显著减轻。研究发现,“隐身” CAR-NK 细胞能减少 IL-6、IFNγ、TNF 等炎症因子的释放——这些因子正是引发 CRS 的 “元凶”。在小鼠血清中,改造后的细胞使 IL-6 等关键炎症因子水平下降超 60%,部分因子甚至完全检测不到,解决了免疫疗法的一大安全隐患。
这套技术的应用前景不止于癌症。研究团队指出,目前针对 CD19(淋巴瘤)、间皮素(卵巢癌)的 “隐身” CAR-NK 细胞已在预临床模型中验证效果,接下来将推进临床试验;由于 NK 细胞对实体瘤的穿透性更强,未来还可能用于肺癌、乳腺癌等实体癌治疗。更令人期待的是,他们还在探索用类似技术改造 NK 细胞治疗狼疮等自身免疫病——通过 “隐身” 和免疫调节,让 NK 细胞既能调节异常免疫反应,又不被宿主清除。
从 “定制化” 到 “现货化”,这场免疫细胞的 “隐身革命”,不仅让癌症治疗更高效、更安全,更让 “患者不等药” 成为可能。也许不久后,癌症患者就能像输血一样,随时接受一袋冻存的 “隐身” CAR-NK 细胞,用最少的等待换取最大的治愈希望。(生物谷Bioon.com)
参考文献:
Liu, F., Tarannum, M., Zhao, Y. et al. Selective HLA knockdown and PD-L1 expression prevent allogeneic CAR-NK cell rejection and enhance safety and anti-tumor responses in xenograft mice. Nat Commun 16, 8809 (2025). doi:10.1038/s41467-025-63863-8
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


