《自然·癌症》:科学家发现肝转移专属基因突变,PI3K抑制剂联合SGLT2抑制剂或生酮饮食有望破解!
来源:奇点糕 2024-03-14 10:12
Pip4k2c基因表达缺失不仅可以增强黑色素瘤肝转移的潜力,而且是“专职掌管”,对肝部位转移具有高度特异性(FDR<0.06)。
美国哥伦比亚大学的Benjamin Izar等人发表在《自然·癌症》期刊上的最新研究,找到了驱动癌症肝转移的专属基因变异。
Pip4k2c是一种激酶的编码基因,研究者们发现,Pip4k2c缺失突变能够帮助肿瘤细胞更加有效地利用胰岛素来促进自身生长,从而特异性地驱动肿瘤细胞向富含胰岛素的肝脏转移。
PI3K抑制剂与SGLT2抑制剂或生酮饮食联合治疗,可以在控制胰岛素水平的同时,减少Pip4k2c缺失介导的肝转移。

论文截图
为找到肝转移的驱动因素,Benjamin Izar等人利用黑色素瘤小鼠模型和体内CRISPR-Cas9筛选等技术,从713种激酶中识别得到激酶PIP4K2C。Pip4k2c基因表达缺失不仅可以增强黑色素瘤肝转移的潜力,而且是“专职掌管”,对肝部位转移具有高度特异性(FDR<0.06)。
进一步结合小鼠模型和体外细胞系培养实验,研究者们发现,Pip4k2c的特定结构域缺陷(aa69-75[VMLLPDD→EIFLPNN])(Pip4k2cAD),会导致肿瘤细胞在胰岛素的刺激下发生PI3K/AKT信号通路被过度激活,提高肿瘤细胞对胰岛素的敏感性,有利于其生长和存活。
由于相比于体内其它部位,肝脏大量富集着胰岛素,因此Pip4k2c缺失能够驱动肿瘤细胞依赖于胰岛素梯度特异性地转移至肝脏,而不是肺部,也几乎不影响原发肿瘤的生长。
在结直肠癌小鼠模型中可以观察到,Pip4k2c缺失的荷瘤小鼠有75%发生肝转移,远高于携带野生型Pip4k2c的小鼠(20%),肺部转移情况没有增加。另外,Pip4k2c缺失对原发结直肠癌的生长影响较小,证明大幅提高的肝转移率是侵袭能力增强的结果。
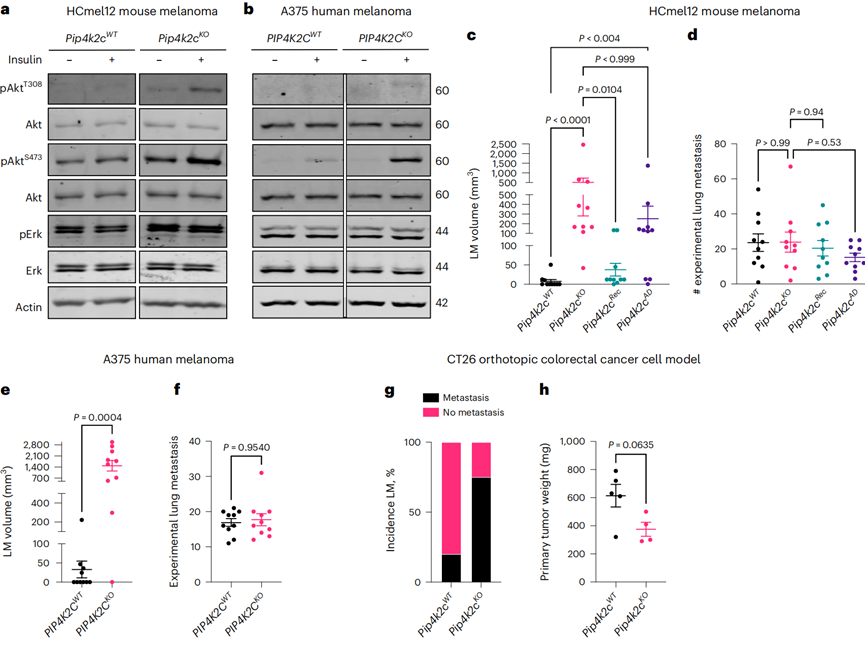
Pip4k2c缺失促进了肝转移
既然Pip4k2c缺失是给PI3K/AKT信号通路的激活拱火,研究者们便想到使用PI3K抑制剂(GDC0941)来使该通路冷静下来,让肿瘤细胞不要对胰岛素这么上头,别一路追到肝脏。
结果出乎意料。PI3K抑制剂哪里是雪中送炭,那是雪上加霜啊。
研究者们发现,抑制PI3K/AKT信号通路方面,PI3K抑制剂确实做得很好。但另一方面,可能与机体的代谢补偿机制相关,PI3K抑制剂给药竟然会导致荷瘤小鼠肝脏的胰岛素水平升高,加剧肝脏与其它部位的胰岛素水平梯度,反而加重Pip4k2c缺失的荷瘤小鼠肝转移负荷。
不过,研究者们很快想到应对之策。他们想到了两种方式,来抵消PI3K抑制剂所引起的肝脏胰岛素水平提高。
一种是使用钠-葡萄糖协同转运蛋白2(SGLT2)抑制剂。SGLT2抑制剂作用于肝脏,可以阻止葡萄糖在肝脏中的重新吸收,从而防止胰岛素水平的剧烈波动。
另一种是生酮饮食,可以减少肝脏中的糖原储存,有助于改善胰岛素敏感性,降低血糖水平。
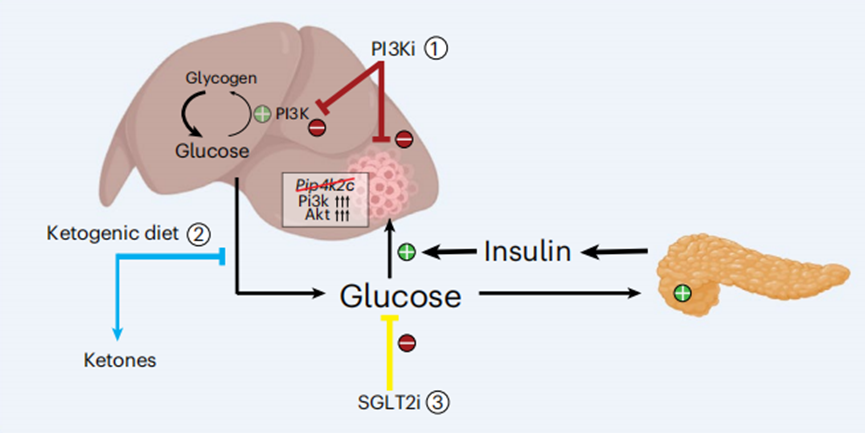
治疗策略
这回成功了。
在Pip4k2c缺失的荷瘤小鼠实验中,相比于PI3K抑制剂单独治疗,PI3K抑制剂与SGLT2抑制剂或生酮饮食的联合治疗显著降低肝转移负荷,血糖峰值和血浆C肽水平明显降低。值得注意的是,不管是哪种治疗,携带野生型Pip4k2c或Pip4k2c缺失的小鼠,它们的原位肿瘤生长情况都没有差异。
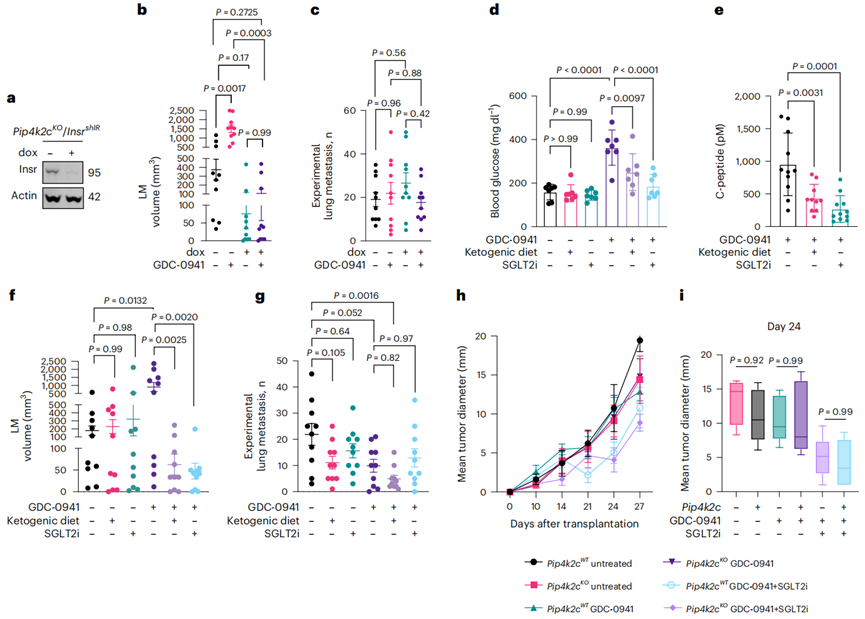
联合治疗效果
另外,与小鼠实验结果一致,研究者们对3511例黑色素瘤患者的样本进行分析,发现与患有原发性肿瘤和发生肺转移的患者相比,发生肝转移的患者Pip4k2c表达水平更低,且肿瘤细胞的TCA循环、氧化磷酸化等关键代谢途径强烈富集。
很好,这下我们专攻肝转移有了新的方向!
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


