Science子刊:揭示癌细胞多药耐药的新机制
来源:本站原创 2020-02-20 14:02
2020年2月20日讯 /生物谷BIOON /--韩国科学技术研究院(KAIST)的研究人员已经确定了对一线化疗的获得性耐药转移到二线靶向治疗的机制,这种机制导致了癌症耐药的"多米诺效应"。他们的研究发表在近日的《Science Advances》上,该研究提出了一种新策略,用于改善对抗癌药物产生耐药性的患者的癌症治疗的二线疗法。对癌症药物的耐药性通常是通过
2020年2月20日讯 /生物谷BIOON /--韩国科学技术研究院(KAIST)的研究人员已经确定了对一线化疗的获得性耐药转移到二线靶向治疗的机制,这种机制导致了癌症耐药的"多米诺效应"。他们的研究发表在近日的《Science Advances》上,该研究提出了一种新策略,用于改善对抗癌药物产生耐药性的患者的癌症治疗的二线疗法。
对癌症药物的耐药性通常是通过化疗和靶向治疗来控制的。与抑制快速增殖细胞的化疗不同,靶向治疗阻断了阻止肿瘤生长的单一致癌途径。在许多情况下,靶向治疗被作为一种维持治疗或在一线化疗后的二线使用。
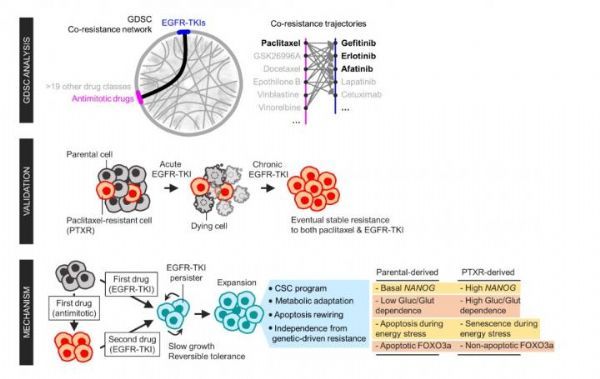
图片来源;KAIST
由来自KAIST化学与生物分子工程系和KAIST健康科技院的Yoosik Kim教授领导的一组研究人员发现了一个发生在化疗和靶向治疗之间的意想不到的耐药性特征。该团队进一步确定了一套促进这种序贯治疗耐药性的综合机制。
该论文的第一作者Mark Borris D. Aldonza说:"多个临床案例表明,在用尽了所有标准治疗方法的患者身上,靶向治疗往往最不成功。这些解释点燃了我们的假设,即对某些化疗的失败反应可能会加速对其他药物的耐药性的进化,特别是那些有特定靶点的药物。"
Aldonza和他的同事从开源数据库"癌症药物敏感性基因组学"(GDSC)中提取了大量的耐药性信息,该数据库包含了来自各种人类癌症细胞系的数千个药物反应数据条目。他们的大数据分析显示,对抗有丝分裂药物(AMDs)这类抑制细胞分裂过度的化疗具有耐药性的癌细胞株,也对一类名为表皮生长因子受体酪氨酸激酶抑制剂(EGFR-TKIs)的靶向治疗具有耐药性。
在所有被分析的癌症类型中,超过84%的抗AMDs(代表"紫杉醇")癌细胞同时也对至少9种EGFR-TKIs耐药。在肺癌、胰腺癌和乳腺癌中,紫杉醇常被用作一线的标准治疗方案,超过92%的患者表现出对EGFR-TKIs的耐药性。Kim教授说:"令人惊讶的是,这种间接耐药性可以在两种化学性质不同的药物之间发生。"
为了弄清对紫杉醇的失败反应是如何导致对EGFR-TKIs产生耐药性的,研究小组通过生成和分析一组称为"持续者"的紫杉醇耐药癌症模型,验证了他们在数据库中发现的共同耐药性特征。
结果表明,紫杉醇耐药的癌症通过首先变得更像干细胞,进化出自我更新的能力,以适应更大的压力条件,如药物暴露,从而重塑其应激反应。更令人惊讶的是,当研究人员研究细胞的代谢状态时,来自紫杉醇耐药癌细胞的EGFR-TKI持续耐药细胞表现出对能量产生过程的高度依赖,如糖酵解和谷氨酰胺分解。
"我们发现,如果没有葡萄糖这样的能量刺激,这些细胞会变得更衰老,这是细胞停止分裂的一个特征。然而,这种衰老是由干细胞因素控制的,这些干细胞因素是紫杉醇耐药的癌细胞用来摆脱这种停滞状态并重新生长的因素,"Aldonza说。
Kim教授解释说:"在这项研究之前,我们没有理由期望获得癌症干细胞表型会显着地导致影响新陈代谢和细胞死亡的细胞状态的级联变化与两类治疗之间的药物特异性序贯耐药性有关。"
他补充说:"我们的工作将扩展到更具有临床相关性的环境中(也许是在临床试验中)的其他耐药性工作模型,这将变得越来越重要,因为序贯治疗策略将继续适用于各种形式的抗癌治疗方案。"(生物谷Bioon.com)
参考资料:
Yoosik Kim et al. Prior acquired resistance to paclitaxel relays diverse EGFR-targeted therapy persistence mechanisms Science Advances 07 Feb 2020: Vol. 6, no. 6, eaav7416 DOI: 10.1126/sciadv.aav7416
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->