Nature Cancer:叶海峰团队开发光控溶瘤细菌,用于癌症精准治疗
来源:生物世界 2025-03-20 09:55
该研究开发了一种近红外光介导的治疗平台,实现了对溶瘤细菌的光控,具有可定制的输出和精确的剂量控制。
实体瘤通常具有低氧特性,一些厌氧菌或兼性厌氧菌能够选择性定植于肿瘤核心低氧区域,并在其中增殖。利用这一特点,研究人员提出了溶瘤细菌的概念,将细菌改造为生产抗肿瘤药物的细胞工程,实现癌症的精准靶向治疗。
然而,由于需要安全、精确的控制系统来调节局部治疗药物的表达和释放,溶瘤细菌疗法的临床应用受到了阻碍。
2025 年 3 月 17 日,华东师范大学生命科学学院、上海市调控生物学重点实验室、上海市基因编辑与细胞治疗前沿基地、医学合成生物学研究中心研究员叶海峰、管宁子团队与同济大学附属同济医院乳腺外科中心主任蔡丰丰团队合作(乔龙亮、牛灵雪、王智浩为共同第一作者),在 Nature 子刊 Nature Cancer 上发表了题为:Engineered bacteria for near-infrared light-inducible expression of cancer therapeutics 的研究论文。
该研究报道了一种能够响应近红外光的新型光遗传学工具——NETMAP系统,并将其上载到减毒沙门氏菌中,成功实现了对多种不同免疫原性肿瘤的光控治疗。

在这项最新研究中,研究团队开发了一种基于近红外(NIR)光介导的 PadC 光开关系统——NETMAP,该系统基于嵌合型光敏色素激活的环二鸟苷酸合成酶(PadC)和环二鸟苷酸依赖的转录激活因子 MrkH。
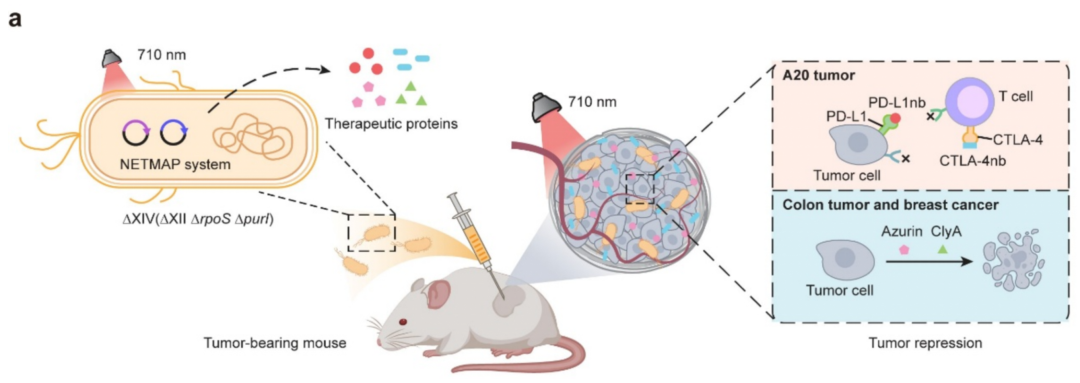
具体而言,在具有免疫原性的淋巴瘤肿瘤中,近红外光诱导的 PD-L1 和 CTLA-4 纳米抗体增强了适应性免疫的激活。在低免疫原性肿瘤中(包括源自小鼠的结肠癌模型、原位人乳腺癌细胞系来源的异种移植模型以及结直肠癌患者来源的异种移植模型),近红外光诱导(每天近红外光照射 2 小时,连续 9 天)的细胞杀伤蛋白(Azurin、Cytolysin A),显著抑制了肿瘤生长。
总的来说,该研究开发了一种近红外光介导的治疗平台,实现了对溶瘤细菌的光控,具有可定制的输出和精确的剂量控制。这种创新的治疗方式,为癌症治疗装上了一套智能导航系统,为癌症治疗领域带来了新希望,也指引着医学迈向更加精准和个性化的未来。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


