部分发作性癫痫新药!Briviact(布瓦西坦)亚洲3期研究成功:显著降低癫痫发作频率!
来源:生物谷原创 2022-10-25 10:54
癫痫是一种慢性神经系统疾病,影响全球约6500万人。

图片来源:摄图网
2022年10月25日讯 /生物谷BIOON/ --优时比(UCB)近日公布了抗癫痫药物Briviact(brivaracetam,布瓦西坦)最新的一项3期临床研究的阳性顶线结果。这是一项随机、双盲、安慰剂对照、多中心、平行组试验,在亚洲的部分发作性癫痫(partial seizure,有或无继发全身性发作)患者中开展(年龄:16岁至80岁),旨在评估Briviact辅助治疗的疗效和安全性。
这项研究是亚洲针对部分发作性癫痫患者进行的规模最大的3期临床研究,共入组了449名患者(日本=98;泰国=145;中国=91;菲律宾=62;马来西亚=47;新加坡=6)。在12周治疗期内,患者被随机分配接受Briviact 50mg/天、200mg/天、安慰剂。
对非盲数据的初步分析得出结论,该试验达到了主要疗效终点:与安慰剂组相比,2种剂量Briviact治疗组患者,28天部分发作性癫痫(POS)频率均显著降低【50mg/天组降低24.6%[p=0.0004],200mg/天组降低33.3%[p<0.0001])。
该试验还达到了所有关键次要终点:50mg/天组有41.1%、200mg/天组有49.3%的患者POS频率至少降低50%,安慰剂组仅为19.0%(均p<0.0001)。与安慰剂组相比,2种剂量Briviact治疗组患者POS频率与基线水平中位百分比均显著降低(50mg/天组中位数降低38.9%[p=0.0011],200mg/天组中位数降低46.7%[p<0.0001])。
研究的安全性数据表明,Briviact耐受性良好,未观察到新的安全信号。最常见的(≥5%)治疗期不良事件(TEAE)为嗜睡(14.4%)、头晕(12.7%)、头痛(6.0%)、上呼吸道感染(6.0%)和鼻咽炎(5.7%)。
该研究的疗效和安全性结果,将支持2023年第3季度在日本提交Briviact的监管申请。研究的详细数据将在即将召开的癫痫大会上公布,并在同行评审期刊上发表。
UCB日本负责人Kanako Kikuchi表示:“该试验的阳性数据表明,强健且临床相关的癫痫发作减少,与之前的Briviact试验一致。这项研究是亚洲针对部分发作性癫痫患者进行的规模最大的3期临床研究,我们期待与监管机构和科学界讨论数据。”
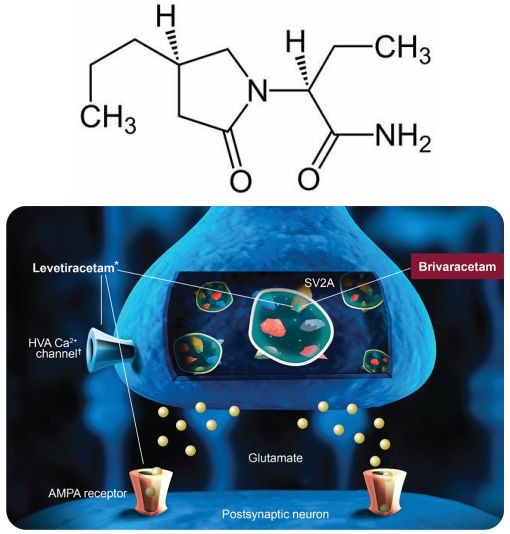
brivaracetam化学结构式及作用机制(图片来源:Wikipedia.org)
癫痫是一种慢性神经系统疾病,影响全球约6500万人。尽管癫痫可能与健康状况、种族和年龄等因素有关,但任何年龄段的人都可能患癫痫,大约每26人中就有1人会在一生中患癫痫。部分性癫痫发作亦称“局灶性或局限性发作”,始于大脑一个区域的神经元放电异常。有多种情况会导致部分性癫痫发作,例如头部损伤、脑感染、中风、肿瘤,以及出生前大脑某一区域形成方式的改变(称为皮质发育不良)。很多时候,没有发现已知的原因,但遗传因素可能在某些部分性癫痫发作中很重要。
Briviact是优时比所发现和开发的一类药物——突触囊泡蛋白2A(SV2A)抗癫痫药物(AED)家族中的药物。Briviact对大脑中的SV2A表现出高度的选择性亲和力并能被迅速完全吸收,这可能有助于其抗惊厥作用。不过,Briviact发挥抗惊厥作用的确切机制目前尚不清楚。
在欧盟,Briviact适应症为:作为一种辅助疗法,用于2岁及以上癫痫患者部分发作性癫痫(有或无继发性全身性发作)的治疗。在美国,Briviact适应症为:用于1个月及以上癫痫患者部分发作性癫痫(有或无继发性全身性发作)的治疗。Briviact有3种剂型:口服片剂、口服溶液和静脉(IV)注射剂。(生物谷Bioon.com)
原文出处:UCB announces positive preliminary results for major brivaracetam (Briviact[®]) study in Asia
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


