平衡抗癌效果和安全性:星锐医药开发肺靶向的mRNA-LNP疗法,开辟肺癌治疗新思路
来源:生物世界 2024-01-16 15:48
这些发现表明,mRNA-LNP的靶向递送为基于IL-15的癌症治疗提供另一种有前途的选择,特别是在肺癌或肺转移肿瘤中。
IL-15(白细胞介素-15)因在调节固有免疫和适应性免疫中的关键作用而成为肿瘤免疫治疗的有前途的候选者。然而,由于意外的毒性作用,其治疗效果仍未得到有效释放。
近几年,我们见证了mRNA技术的快速发展,尤其是在COVID-19疫苗中大获成功,这也让基于mRNA的新疗法得到了广泛关注。使用脂质纳米颗粒(LNP)来靶向递送mRNA,增加IL-15在肿瘤部位的浓度、减少其向循环系统的泄漏,是平衡IL-15疗效和毒性作用的一种有潜力的方法。
2024年1月12日,星锐医药(Starna Therapeutics)胡荣宽博士、北京大学未来技术程强研究员等在预印本平台 bioRxiv 上发表了题为:Targeted LNPs deliver mRNA encoding IL-15 superagonists to balance efficacy and toxicity in cancer therapy 的研究论文。
该研究使用结构驱动的靶向递送平台——STAR,获得了一系列具有自主知识产权的LNP在体,用于高效且选择性将mRNA递送至局部(LNPLocal)和肺部(LNPLung)。通过对mRNA的结构优化和序列筛选,该研究获得具有良好抗癌活性的IL-15超激动剂mRNA,分别使用LNPLocal和LNPLung进行瘤内注射和静脉注射,评估了IL-15超激动剂mRNA的抗肿瘤效果。结果显示,这些超级激动剂表现出比N-803(一种已提交上市申请的IL-15超级激动剂)更好的抗肿瘤活性,且具有更少的全身暴露和更少的细胞因子相关风险。
更重要的是,该研究还在非人类灵长类动物(NHP)中进一步验证了LNPLung的肺部选择性靶向递送效果和良好的安全性,证实了其临床应用潜力。这些结果为肺癌和肺转移肿瘤的治疗开辟了新的可能性。

IL-15(白细胞介素-15)在固有免疫和适应性免疫中的关键作用在免疫学领域具有深远的影响。IL-15的生物学效应通过由三个亚单位组成的受体复合物相互作用来介导:CD122(IL-2/IL-15Rβ),CD132(IL-2/IL-15Rγc),以及高亲和力特异性的IL-15Rα。
IL-15目前作为一种有前途的免疫治疗候选药物,在癌症治疗中获得了相当多的关注,例如IL-15超级激动剂N-803已获FDA批准的临床试验。
然而,由于IL-15超激动剂激活T细胞和NK细胞的机制,潜在毒性仍然存在。在治疗过程中,在所有剂量和给药途径下观察到CD8 T细胞、NK细胞和在某些情况下CD4 T细胞的治疗增强。值得注意的是,更高的剂量和更频繁的给药会导致更明显的反应,但也会引起临床毒性,如厌食、腹泻、体重减轻和短暂的3-4级的中性粒细胞减少。
N-803在提交新药上市申请时的初始适应症是通过膀胱内给药治疗膀胱癌,相较于全身性系统给药,这种局部给药可以相对平衡IL-15的治疗效果和潜在毒性。
胡荣宽/程强团队认为,可以通过靶向给药更好地实现疗效与毒性之间的平衡,让让靶组织实现最大的IL-15浓度,而尽量减少其向循环系统的泄漏。通过靶向递送和表达,mRNA技术成为实现上述目标的最具潜力的选项之一。
mRNA技术在COVID-19疫苗中的成功应用,使其在全世界范围内成为研究热点。除了用作传染病疫苗,通过序列设计,mRNA可以编码各种蛋白质,具有广阔的应用前景。目前,使用脂质纳米颗粒(LNP)递送的mRNA技术已经成功应用于多种疾病的防御和治疗。
然而,将mRNA-LNP靶向递送至特定器官/组织和细胞仍然具有挑战性,但这可以通过高通量筛选、LNP组分优化和抗体修饰来部分解决。
在这项研究中,研究团队通过理性设计,合成了数百种可电离的阳离子脂质,并建立了一种结构驱动的靶向递送平台——STAR(Structure-driven TARgeting platform),其器官/组织选择性靶向能力已得到充分验证并获得了专利授权。
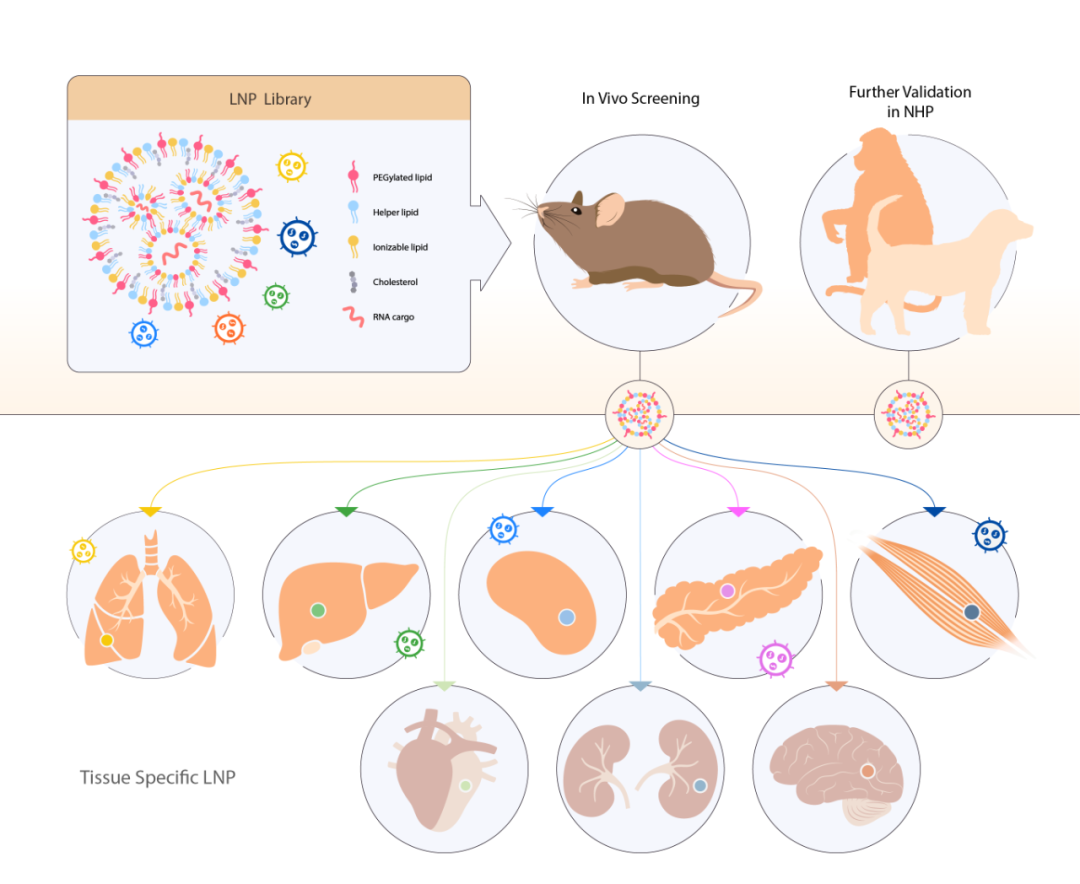
星锐医药开发的组织特异性LNP
值得注意的是,STAR LNPs库中的LNPLocal和LNPLung可以分别将mRNA特异性地递送到肌肉和肺部。因此,这两种LNP可以通过递送编码IL-15超激动剂的mRNA来满足肿瘤治疗的需求,特别是在特定的组织中。
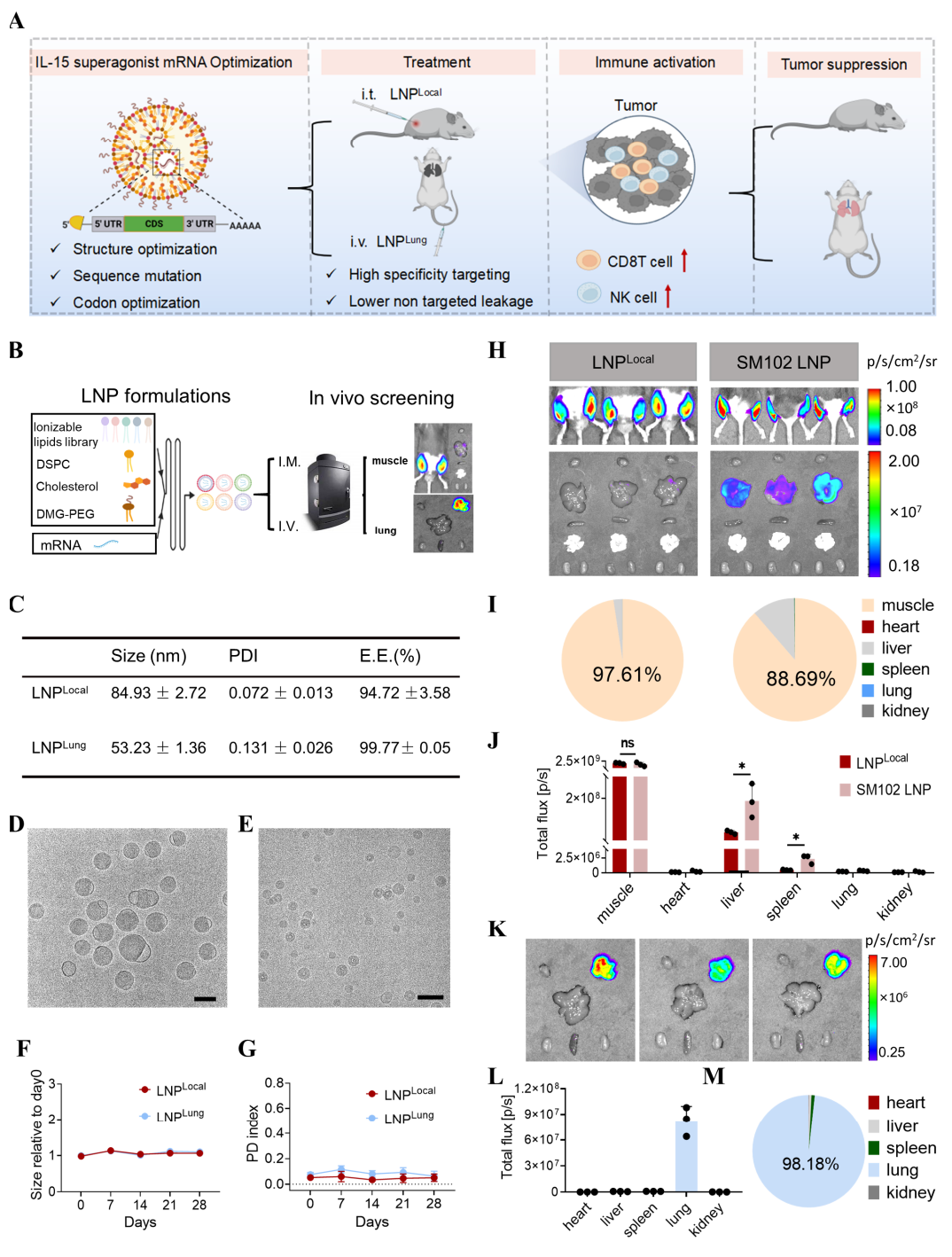
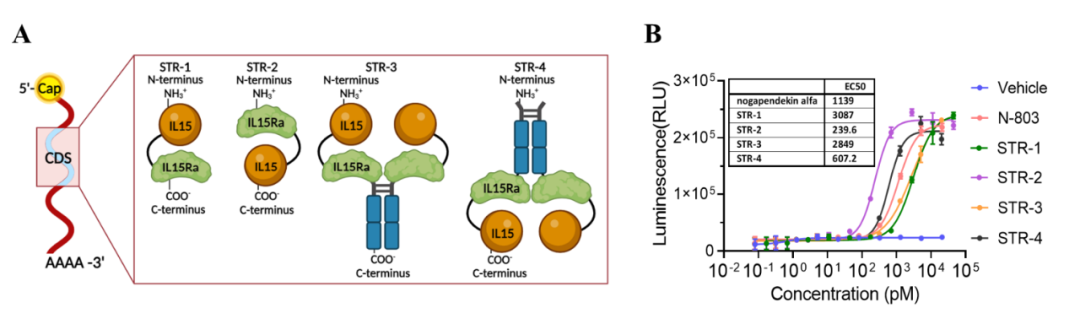
研究团队首先评估了几种IL-15超激动剂的mRNA形式的结构稳定性和活性。其中,具有IgG Fc片段-IL-15Rα sushi结构域的STR-4 mRNA表现出最佳疗效,甚至优于N-803。然后,研究团队对STR-4 mRNA序列进行了进一步优化,在特定位置引入天冬氨酸突变,获得了STR-4-D43和STR-4-D61 mRNA,并进行了皮下肿瘤模型和肺转移瘤模型的抗肿瘤实验。
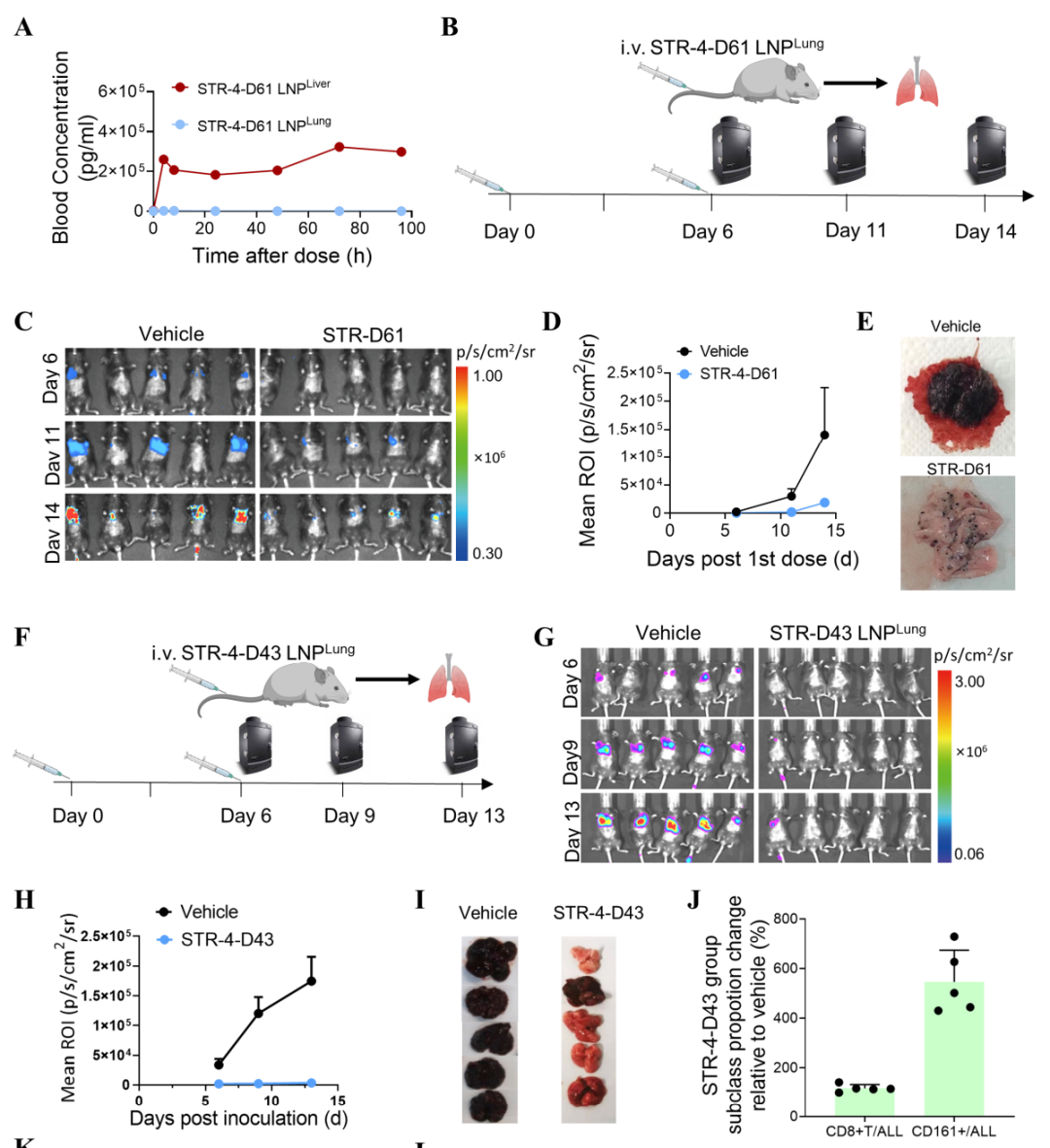
通过LNPLocal局部注射和LNPLung静脉注射两种方式递送上述mRNA,均表现出显著的肿瘤抑制作用。此外,这种mRNA-LNP方式通过最大限度地减少IL-15向主要器官的泄漏,从而减少了毒性作用,显示出良好的疗效和安全性之间的平衡。
为了验证该方法的临床转化潜力,研究团队在非人类灵长类动物(NHP)上测试了mRNA-LNPLung,结果显示了强健的肺部递送效率和良好的安全性。
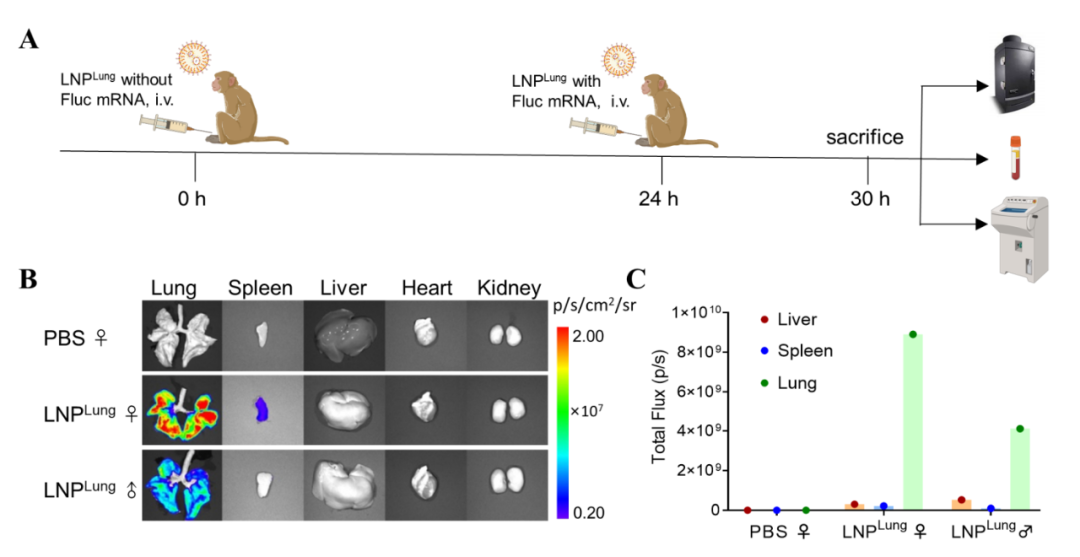
这些发现表明,mRNA-LNP的靶向递送为基于IL-15的癌症治疗提供另一种有前途的选择,特别是在肺癌或肺转移肿瘤中。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


