《自然·医学》:指导HER2阳性大肠癌靶向治疗,ctDNA能行
来源:奇点糕 2021-12-13 16:29
作为最常见的消化道恶性肿瘤之一,结直肠癌的发病率目前占所有恶性肿瘤第3位,而癌症相关病死率已跃居第2位,严重威胁着人类健康[1]。随着分子生物学研究的深入和驱动基因的发现,结直肠癌的治疗也逐渐向个体化、精准化方向发展。人表皮生长因子受体2(HER2)已初步被确认为结直肠癌治疗靶点[2],既往研究表明抗HER2治疗在HER2阳性转移性结
作为最常见的消化道恶性肿瘤之一,结直肠癌的发病率目前占所有恶性肿瘤第3位,而癌症相关病死率已跃居第2位,严重威胁着人类健康[1]。随着分子生物学研究的深入和驱动基因的发现,结直肠癌的治疗也逐渐向个体化、精准化方向发展。
人表皮生长因子受体2(HER2)已初步被确认为结直肠癌治疗靶点[2],既往研究表明抗HER2治疗在HER2阳性转移性结直肠癌患者(mCRC)中具有一定的疗效及良好的耐受性[3]。
然而,目前的研究显示HER2在结直肠癌中的总体阳性率不高,不同研究之间关于阳性率的报道差异巨大(1.6%~46.2%)[4]。这一现象可能与目前CRC组织中关于HER2阳性的评分标准不同,且HER2检测仍以免疫组化或荧光原位杂交为主有关。那么,是否还有其他更准确的方法能够协助检测肠癌患者的HER2表达吗?
答案是肯定的。
近日,来自日本国立癌症中心的Takayuki Yoshino教授团队在《自然·医学》期刊发表了团队最新的研究成果。
他们借助肿瘤组织学检测或血浆循环肿瘤DNA(ctDNA)分析,选择了伴有HER2扩增的mCRC患者作为受试者,用以评估帕妥珠单抗联合曲妥珠单抗靶向治疗的效果。
结果发现组织学HER2阳性的mCRC患者客观缓解率(ORR)可达30%,ctDNA阳性的mCRC患者ORR也达到了28%,均优于以往的真实世界研究中mCRC患者标准补救疗法的ORR(0%)。后续的探索性研究还发现,借助ctDNA检测患者靶向治疗前后HER2基因拷贝数的变化,还有助于评估患者对治疗的反应[5]。
这一结果表明, ctDNA对HER2 基因的检测效能不劣于肿瘤组织学检测,且ctDNA不仅可用于评估HER2基因靶向治疗能否适用于mCRC患者,也可用于动态监测患者对于靶向药物的治疗效果,有助于预测患者的预后。
作为近几年兴起的一种分子检测手段,液体活检技术不仅有助于肿瘤早期筛查,还可实时监测治疗疗效和耐药基因,评估复发转移风险,在肿瘤的精准治疗中具有重要的应用前景[6]。液体活检的对象包括循环肿瘤细胞(CTC)、ctDNA、外泌体、循环RNA等,其中ctDNA作为最重要的生物标志物,在进展期消化道肿瘤中的应用价值也逐渐被认可[7]。
Yoshino团队曾在日本开展了一项筛查型研究(GOZILA研究),对进展期消化道肿瘤患者行血浆ctDNA二代测序,并基于基因分型予以相应的靶向药物治疗。研究发现应用ctDNA检测可加快患者招募的进程,且其对患者基因分型的检测效能与组织学检测的结果持平[8]。然而目前应用ctDNA的临床研究仍较少,尤其是用ctDNA检测基因扩增情况。由此,Yoshino团队设计了这一项2期临床研究,并将其命名为TRIUMPH研究。
TRIUMPH研究借助日本的两个大规模筛查队列—SCRUM-Japan GI-SCREEN 以及 GOZILA,从中各选取部分mCRC患者入组,入组患者分别经组织学检测[免疫组化(IHC)及荧光原位杂交(FISH)]和/或血浆ctDNA检测为RAS野生型基因,并伴随HER2基因扩增表达。
对入组患者行帕妥珠单抗联合曲妥珠单抗靶向治疗后进行随访,随访的主要终点为客观缓解率(ORR)。此外,研究者选取SCRUM-Japan Registry队列中的RAS野生型基因并伴随HER2基因扩增,但接受了非靶向HER2的标准补救治疗方案的mCRC患者作为真实世界对照组。
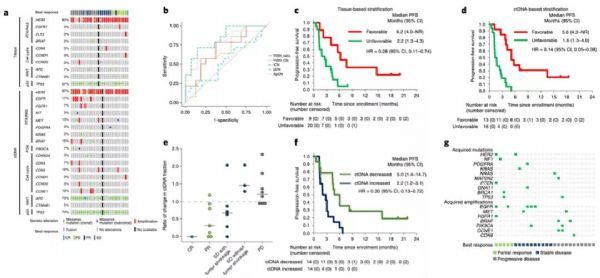
自2017年12月至2020年3月,在147名接受HER2组织学筛查(HER2-Screening组)的mCRC患者中,共有56名被证实为HER2基因扩增。自2018年1月至2020年3月,在1107名ctDNA检测(GOZILA组)的患者中,有66名被证实为HER2基因扩增。此外,研究者发现ctDNA测得的所有扩增基因中,HER2基因的中位血浆拷贝数(pCN)表达最高,提示HER2基因可能为mCRC进展的驱动基因及潜在靶基因。
在两组研究队列中,共有75名患者同时进行了HER2组织学及ctDNA检测,进一步分析发现,有7/39名(18%)患者表现为组织学阳性、ctDNA阴性(tissue+ctDNA-),而6/38名(16%)表现为ctDNA阳性、组织学阴性(tissue-ctDNA+)。由此可见,组织学与ctDNA法对HER2基因扩增检测结果的阳性一致率为82%,总体一致率为83%。
Yoshino团队最终选择了30名患者入组,其中组织学阳性(tissue+)组27名,ctDNA 阳性(ctDNA+)组25名,有22名患者同时接受了组织学及ctDNA检测。两组患者的中位随访时间为tissue+组9.2个月,ctDNA+组7.6个月。
此外,研究者另选了14名HER2基因扩增型mCRC患者作为真实世界数据对照,这些患者曾接受过一线氟尿嘧啶、奥沙利铂、伊立替康以及抗EGFR治疗,在疾病进展后,最常用的补救治疗是曲氟尿苷替匹嘧啶片联合或不联合贝伐珠单抗。
在随访过程中,两组患者均达到研究的主要随访终点,其中tissue+组的ORR达到30%,而ctDNA+组为28%,两组中均有一名患者达到完全缓解(CR)。相比而言,对照组人群的ORR为0%。
此外, tissue+组患者的中为无进展生存期(PFS)为4.0个月,而ctDNA+组中位PFS为3.1个月。而对于中位总生存期(OS)而言,tissue+组患者的中位OS为10.1个月,而ctDNA+组患者为8.8个月。
共有24名患者(80%)发生治疗相关的不良事件,最常见的是输液相关反应,腹泻、胃炎和不适感。有3名患者 (10%) 发生了治疗相关的 3 级不良事件,但没有治疗相关的死亡事件发生。
为评估患者基线组织学及ctDNA基因表达谱与治疗效果的相关性,Yoshino团队继续在TRIUMPH队列中开展探索性的研究。组织学二代测序(NGS)仅在少数无反应者中检测到癌基因的共同改变(如HER2和BRAF基因),而ctDNA基因分型显示,无反应患者中存在受体酪氨酸激酶 (RTK)/RAS 和 PI3K 相关基因的显着扩增或克隆突变,而这些基因已被报道与HER2 靶向治疗的耐药相关[9]。
总的来说,在21名靶向治疗无反应的患者中,组织学NGS共在4名患者(19%)检测到RTK/RAS/PI3K相关基因的共同突变,而ctDNA在14名(67%)患者中检测到该突变(p=0.004)。
此外,研究者还发现基于组织学NGS获取的HER2 拷贝数(CN)与患者临床预后的相关性明显优于HER2/CEP17比值或 HER2 CN-FISH组(p<0.001),而尽管血浆ctDNA CN的绝对计数与临床预后相关性不明显,但经肿瘤组分校准后的CN(ApCN)与预后的相关性与组织学NGS相似(p=0.009)。
Yoshino团队进一步依据患者RTK/RAS/PI3K相关基因的共同突变率,及tissue+组患者的组织学NGS 检测到的HER2 CN或ctDNA+组的ApCN,来评估患者的临床预后。结果表明,不带有共同突变且HER2 CN高于阈值的患者(即优势组患者)PFS及OS均显着升高。
除此之外,研究者还发现靶向治疗后3周检测ctDNA的组分变化可有助于评估患者疗效,达到客观缓解的患者在治疗前后ctDNA组分的中位百分比低于1.0,而肿瘤进展的患者ctDNA组分明显升高,治疗后ctDNA降低与患者较好的PFS及OS均显着相关。而通过对患者靶向治疗前后的血浆ctDNA进一步分析,发现在疾病进展的26名患者中,有16名(62%)检测到了至少1个基因的获得性突变或扩增。
总的来说,这项前瞻性的2 期临床试验表明,对于伴有HER2扩增的mCRC患者而言,帕妥珠单抗联合曲妥珠单抗的ORR接近30%,研究的有效性与安全性与既往研究一致,且ctDNA与组织学检测对于HER2扩增的检验效能相似。
此外,ctDNA在治疗前后的动态变化可有助于评估患者的疗效,且可根据治疗后基因突变及扩增情况预测患者的继发性耐药情况,这对于预测HER2阳性mCRC患者的预后具有重要的应用前景。当然,这项研究尚属于小样本量研究,未来还需要有更大规模的研究进行验证。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。