Science:揭示衰老的神经系统在遭受损伤后再生能力下降机制
来源:生物谷原创 2022-05-17 13:01
轴突再生和神经功能的恢复在老年人中极为有限。因此,神经系统受伤后通常会出现严重和长期的残疾。科学家们对因衰老出现再生失败的分子机制了解不多,阻碍了在开发有效的神经系统修复疗法方面取得进展。
轴突再生和神经功能的恢复在老年人中极为有限。因此,神经系统受伤后通常会出现严重和长期的残疾。科学家们对因衰老出现再生失败的分子机制了解不多,阻碍了在开发有效的神经系统修复疗法方面取得进展。为了促进神经系统修复策略的设计,人们迫切需要确定导致因衰老出现再生失败的关键分子机制和细胞机制。
衰老会导致细胞信号传导的广泛改变,包括代谢、免疫和整体组织平衡的变化,这在神经系统的生理学特性和损伤反应中起着关键作用。因此,在一项新的研究中,来自英国帝国理工学院的研究人员猜测衰老的神经系统在受伤后会出现独特的分子和细胞修饰,这将有助于促进因衰老而出现的再生能力下降。为此,他们通过对年轻小鼠和年老小鼠坐骨神经损伤的成熟模型中的背根神经节(dorsal root ganglia, DRG)进行RNA测序,系统性地研究了与衰老和神经系统损伤有关的分子和细胞特征。对这些机制的深入了解可能发现以前没有认识到的分子靶标,以对抗因衰老而出现的再生能力下降。相关研究结果发表在2022年5月13日的Science期刊上,论文标题为“Reversible CD8 T cell–neuron cross-talk causes aging-dependent neuronal regenerative decline”。

对RNA测序数据的初步分析发现,衰老主要与小鼠坐骨神经损伤后DRG中T细胞激活和信号传导的明显增加有关。随后的实验表明,衰老与坐骨神经损伤前后DRG中包括淋巴毒素在内的炎性细胞因子的增加有关。
具体来说,这些作者发现淋巴毒素β是NF-κB磷酸化所必需的,NF-κB磷酸化驱动趋化因子CXCL13在DRG感觉神经元中的表达。在坐骨神经损伤后,CXCL13在通过过表达主要组织相容性复合物I型(MHC I)作为抗原呈递细胞发挥作用的神经元附近吸引了表达CXCL13受体CXCR5的CD8+ T细胞。CXCR5+CD8+T细胞与表达MHC I的感觉神经元的结合激活了caspase 3,而激活的caspase 3破坏了pAKT和pS6信号传导,从而导致再生失败。利用药物拮抗caspase 3激活可以逆转年老小鼠的再生失败,并恢复pAKT和pS6的表达。
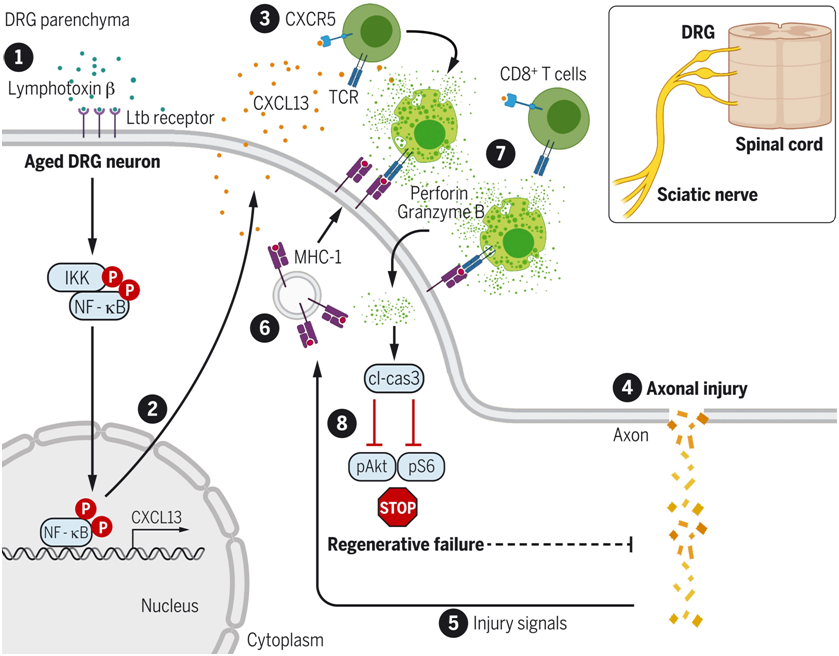
导致在感觉神经元受损后因衰老而出现再生失败的事件序列。图片来自Science, 2022, doi:10.1126/science.abd5926。
包括比较Cxcr5-/-细胞和野生型细胞的比较在内的过继转移实验直接表明CXCR5+CD8+T细胞限制了年老小鼠坐骨神经损伤后的轴突再生。最后,用单克隆抗体中和CXCL13可以拮抗CXCR5+CD8+T细胞招募到DRG,并使年老小鼠坐骨神经感觉轴突的再生能力恢复到与年轻小鼠相当的水平。中和CXCL13也明显促进了皮肤神经再支配和感觉功能的神经恢复。
综上所述,这些作者鉴定出一种衰老依赖性机制,该机制基于CXCL13依赖性地招募和激活感觉神经元附近的CXCR5+CD8+T细胞,这些T细胞在与呈递MHC I的DRG神经元沟通后限制了神经损伤后的轴突再生。用人源化单克隆抗体中和CXCL13可以逆转再生能力的下降,并促进年老小鼠的神经系统恢复,这表明一种可能在未来疗法中使用的途径。(生物谷 Bioon.com)
参考资料:
Luming Zhou et al. Reversible CD8 T cell–neuron cross-talk causes aging-dependent neuronal regenerative decline. Science, 2022, doi:10.1126/science.abd5926.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


