《JAMA·肿瘤学》:吴一龙/莫树锦深度综述!可手术EGFR突变阳性肺癌靶向辅助治疗的现在和未来
来源:奇点糕 2023-06-13 15:26
作为最早应用酪氨酸激酶抑制剂(TKI)类靶向药的癌症亚型之一,
作为最早应用酪氨酸激酶抑制剂(TKI)类靶向药的癌症亚型之一,EGFR突变阳性非小细胞肺癌(NSCLC)的靶向治疗,确实反映着精准治疗的航向。
在晚期患者的预后被EGFR-TKI显著改善后,2020年关键临床研究ADAURA的提前成功[1],则标志着以奥希替尼为代表的第三代EGFR-TKI,能够参与到围术期患者的辅助治疗中,开启“靶向辅助治疗”的全新治疗模式。
不知不觉,距离ADAURA研究的成功也有三年了,那么EGFR突变阳性NSCLC的辅助靶向治疗,还有哪些问题悬而未决,亟待科学家和医生们给出答案呢?近期发表在JAMA Oncology上的一篇综述,就深度剖析了这个问题[1]。

论文首页截图
当前临床研究提供的EGFR-TKI辅助治疗证据
较早使用第一代EGFR-TKI辅助治疗的临床研究,如BR19、RADIANT等均未达到阳性结果,我国学者吸取了早期研究未精准选择EGFR突变阳性人群的教训,主持并开展了多项关键研究,如EVAN(使用厄洛替尼)、ADJUVANT(吉非替尼)、EVIDENCE(埃克替尼)等,大多报告了无病生存期(DFS)显著获益。
不过,上述研究的DFS获益存在一定差异,且受到后线治疗等因素的影响,第一代EGFR-TKI均未能在研究中显著延长患者的总生存期(OS),长期DFS获益也仍不够明确(如ADJUVANT研究试验组/对照组5年DFS率无差异)。
而ADAURA研究中奥希替尼的疗效则全面超越了第一代EGFR-TKI:研究最新随访数据显示,对分期在IB-IIIA期的可手术患者,奥希替尼可使患者疾病进展或死亡风险下降73%(HR=0.27),4年DFS率接近翻倍(73%/38%)[2]。虽然目前研究随访时间尚不足以得到成熟OS结果,但奥希替尼已被国内外权威指南所推荐。
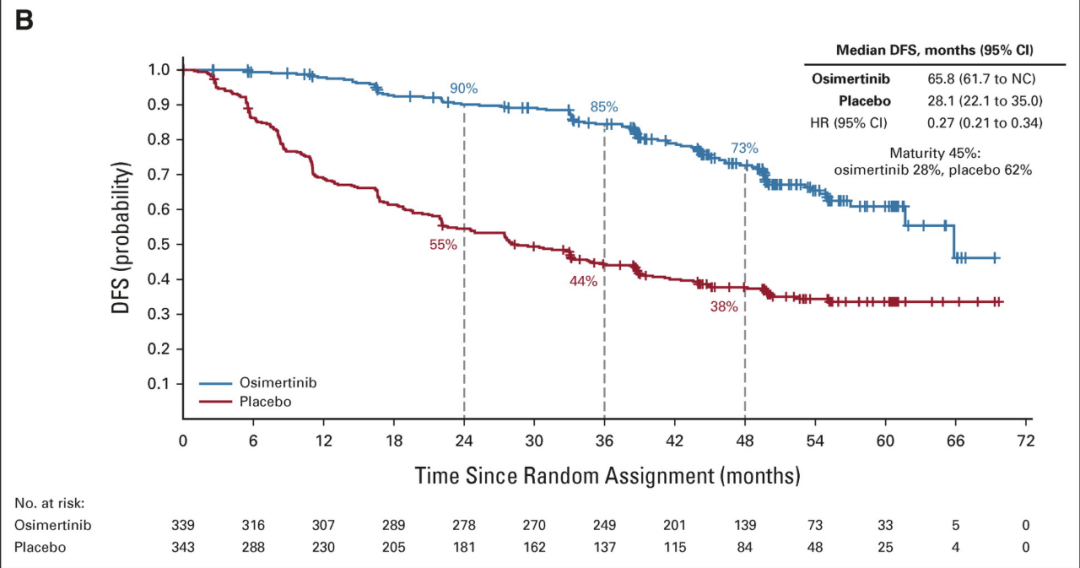
ADAURA研究4年随访数据图
值得注意的是,ADAURA研究在设计上“允许但不强制”入组患者使用奥希替尼前,接受传统的含铂双药辅助化疗,且无论患者是否接受化疗,均不显著影响奥希替尼的获益。但从历史数据来看,辅助化疗对EGFR突变阳性NSCLC是否有获益仍存在很大争议,ADAURA研究和权威指南也暂时无法回答这一问题。
EGFR突变阳性NSCLC复发模式及复发后的管理
有真实世界研究显示,EGFR突变阳性NSCLC患者接受根治性治疗后,存在更高的疾病复发/远处转移风险,而最常见的复发部位依次为脑、疾病原位(肺)、骨和肝[3-4]。使用吉非替尼的ADJUVANT研究中,脑转移也仍是患者最常见的远处转移,且第一代EGFR-TKI入脑能力有限,无法显著降低脑转移发生风险。
而ADAURA研究的复发模式数据则显示,奥希替尼可有效降低患者脑转移风险,36个月时仅2%患者新发脑转移(对照组为11%,相应HR=0.24),至于第三代EGFR-TKI对其它部位复发/转移风险的影响,还有待更多数据报告。
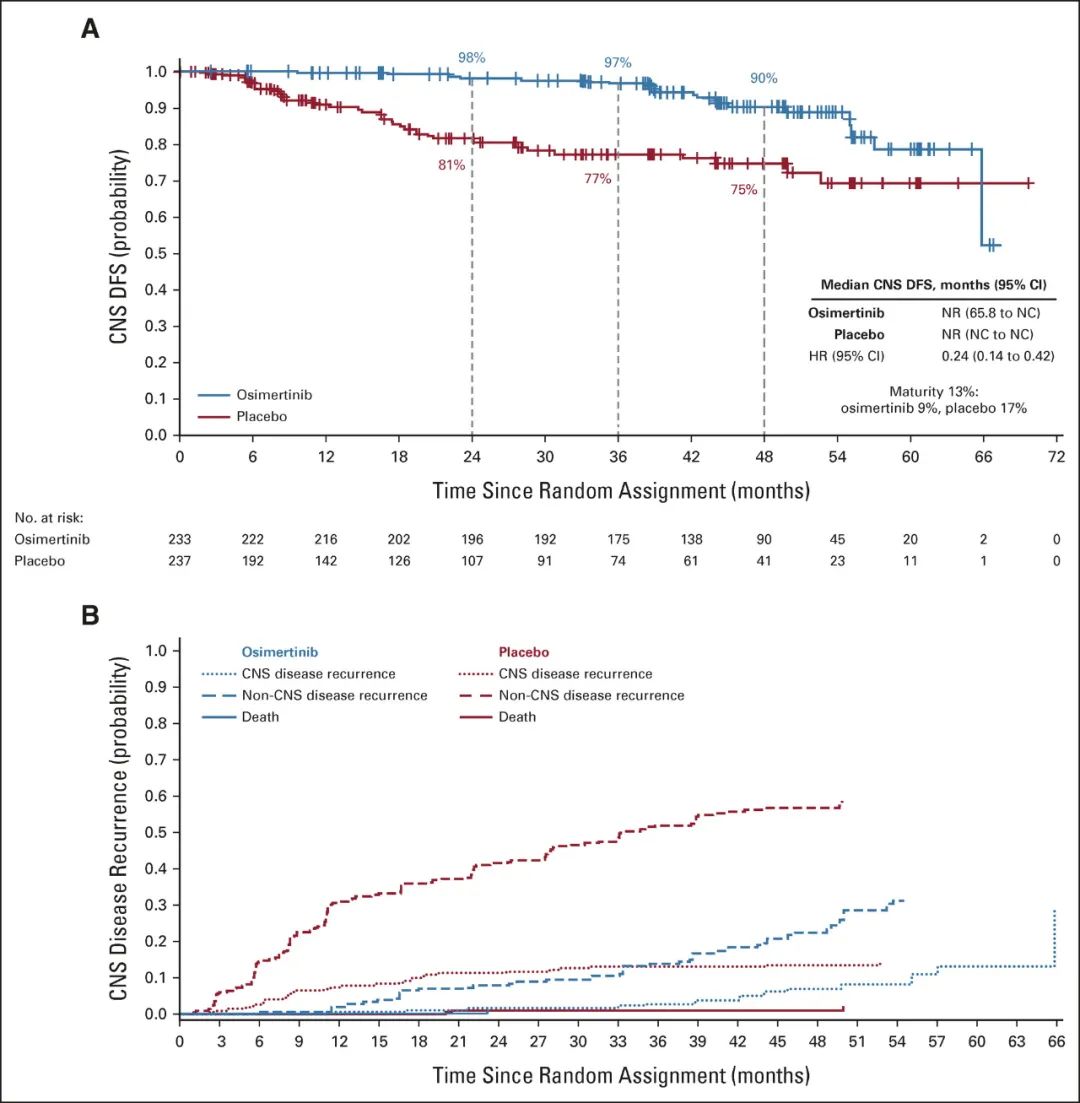
奥希替尼可有效降低患者脑转移风险
对出现疾病复发的患者,既往的ADJUVANT、SELECT等研究采用以一代EGFR-TKI再挑战的策略,能一定程度上延缓疾病再次进展,但这仅限于辅助治疗结束后的疾病复发;进入奥希替尼治疗时代后,也可考虑相似的TKI再挑战策略,但由于奥希替尼的耐药机制比第一代EGFR-TKI更复杂,应对策略仍需更多探索。
共突变和免疫微环境的影响
EGFR突变阳性NSCLC较常见的共突变有TP53、RB1等,且大量临床数据显示,TP53共突变与晚期患者不良预后有关,TP53/RB1同时存在则可能介导组织学类型转化(即NSCLC转化为小细胞肺癌);而可手术的早期肿瘤,也存在显著的瘤内异质性和基因组不稳定性,意味着共突变也将产生深远影响。
我国学者对ADJUVANT研究患者数据(n=171)进行分析后,将EGFR突变阳性可手术NSCLC患者分为三个亚组,而TP53 4/5号外显子突变、RB1突变及NKX2-1、CDK4、MYC基因的拷贝数变异均可作为预测性标志物[5],但样本量仍嫌不足。
目前ADAURA研究尚无此类分析结果报告,期待未来能看到相关信息,此外还应分析辅助化疗和EGFR-TKI治疗对免疫微环境的影响,寻找新的生物标志物,乃至为免疫治疗的应用铺路。
MRD和ctDNA的应用
液体活检ctDNA可评估可手术NSCLC患者是否仍存在分子残留病灶(MRD),以预测患者疾病复发和远处转移风险,但目前专门分析EGFR突变阳性患者MRD状况与预后关系的研究还很少,只有一项韩国研究显示,手术后4周时仍有MRD(基线ctDNA阳性)与患者较短的DFS有关[6],该研究也未使用EGFR-TKI治疗。
辅助治疗最优时长是多久?
早期使用一代EGFR-TKI的临床研究中,普遍将辅助治疗时长定为两年,但生存曲线的快速重合提示治疗时长仍有不足,因此ADAURA研究将奥希替尼辅助治疗的时长设定为3年,目前尚未观察到延长治疗期导致的明显毒性,近期启动的临床II期TARGET研究,则将探索奥希替尼辅助治疗5年的疗效和安全性。
总结
虽然ADAURA研究的OS结果必将受到诸多因素影响,还需要非常长期的随访观察,但奥希替尼即使只能显著延缓疾病复发、改善患者临床症状,也将带来巨大的治疗获益,因此奥希替尼辅助治疗3年(大多推荐在化疗后序贯使用),已成为目前国内外推荐的EGFR突变阳性可手术NSCLC标准辅助治疗方案。
参考文献:
[1]Passaro A, Mok T S K, Attili I, et al. Adjuvant Treatments for Surgically Resected Non–Small Cell Lung Cancer Harboring EGFR Mutations: A Review[J]. JAMA Oncology, 2023.
[2]Herbst R S, Wu Y L, John T, et al. Adjuvant osimertinib for resected EGFR-mutated stage IB-IIIA non–small-cell lung cancer: updated results from the phase III randomized adaura trial[J]. Journal of Clinical Oncology, 2023, 41(10): 1830-1840.
[3]Chouaid C, Danson S, Andreas S, et al. Adjuvant treatment patterns and outcomes in patients with stage IB-IIIA non-small cell lung cancer in France, Germany, and the United Kingdom based on the LuCaBIS burden of illness study[J]. Lung Cancer, 2018, 124: 310-316.
[4]Galvez C, Jacob S, Finkelman B S, et al. The role of EGFR mutations in predicting recurrence in early and locally advanced lung adenocarcinoma following definitive therapy[J]. Oncotarget, 2020, 11(21): 1953-1960.
[5]Liu S Y, Bao H, Wang Q, et al. Genomic signatures define three subtypes of EGFR-mutant stage II–III non-small-cell lung cancer with distinct adjuvant therapy outcomes[J]. Nature Communications, 2021, 12: 6450.
[6]Ahn M J, Jung H A, Ku B M, et al. 933MO Longitudinal monitoring of circulating tumor DNA from plasma in patients with curative resected stage IA-IIIA EGFR mutant non-small cell lung cancer[J]. Annals of Oncology, 2022, 33(Supplement 7): S974.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


