CAR-T,CAR-NK联合间充质干细胞,攻克实体瘤的新希望
来源:博雅生命 2022-09-30 21:33
谈及癌症,人人都十分惶恐,全球范围内癌症发病率与死亡率不断攀升,据统计[1],2020 年全球癌症发病率为 247.5/10 万,死亡率为 127.8/10 万。
谈及癌症,人人都十分惶恐,全球范围内癌症发病率与死亡率不断攀升,据统计[1],2020 年全球癌症发病率为 247.5/10 万,死亡率为 127.8/10 万。目前,对于癌症防治的治疗手段以外科手术,放化疗,靶向治疗及免疫治疗等,然而仍有相当比例的患者无法得到有效治疗。近年来,基于细胞的疗法给癌症治疗带来了变革。
近日《Biomedicines》杂志发表的综述[2],详细介绍了嵌合抗原受体细胞疗法(包括CAR-T,CAR-NK)在癌症治疗领域的研究进展及其在不同肿瘤中的应用;间充质干细胞(MSCs)作为肿瘤治疗载体的独特能力以及增强CAR免疫细胞活性的可能性。帮助大家了解不同类型细胞在癌症治疗领域的发展。

图1 研究成果(图源:[2])
细胞疗法,也被称为过继细胞疗法,是近年来癌症治疗领域的一大研究热点。其中最备受关注的便是CAR-T及CAR-NK细胞,该疗法首先采集患者/健康供体的T/NK细胞,在体外对其进行改造,使其带上能特异性瞄准肿瘤细胞表面抗原的受体,相当于给细胞装上了一个GPS,然后将这些改造后的细胞重新输注给患者,使其能够更加精准的狙击肿瘤细胞。
虽然CAR-T及CAR-NK细胞研究取得巨大进展,尤其在血液系统恶性肿瘤治疗中,但在实体肿瘤中由于毒性、脱靶、稳定性有限等挑战还有待解决。
为了解决上述问题,研究人员引入了间充质干细胞(MSCs)作为生物载体,借助其向肿瘤组织的归巢效应,可以增强CAR-细胞的靶向性及活性。
CAR-细胞临床研究进展
CAR-T细胞疗法大家想必都很熟悉了,约有1000项相关临床试验正在开展中,也有多款产品获批上市。目前,CAR-T细胞疗法的关注点旨在解决相关副作用,包括细胞因子释放综合征(CRS),免疫效应细胞相关神经毒性综合征(ICANS),和肿瘤靶外毒性等。
近年来,CAR-NK细胞的出现被认为有望解决上述难题,目前全球已开展29项CAR-NK细胞治疗研究。
相较于CAR-T细胞,CAR-NK细胞不受Tregs细胞的抑制,当CAR-NK细胞被激活时,它们可以在事先无肿瘤抗原刺激的情况下进行细胞毒活动;它的另一个优势是不会刺激移植物抗宿主病(GVHD),有望实现同种异体应用;此外,CAR-NK细胞也不会引起CRS等副作用。
对于CAR-T细胞,一项1期临床试验[3]对23例癌症患者(包括14例肝细胞癌,7例胰腺癌,2例结直肠癌)进行CAR-T细胞疗法。结果显示,接受治疗后,3例患者部分缓解,14例病情稳定。21名患者没有出现可检测到的新病灶,此外,活检组织显示表达特定抗原的癌细胞被消除了。
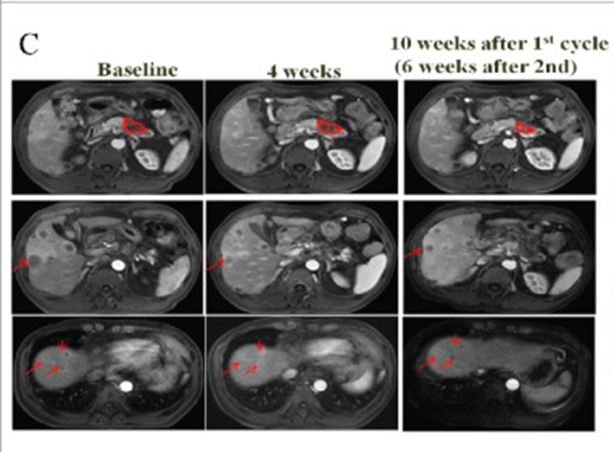
图2 患者治疗前后影像学变化(图源:[3])
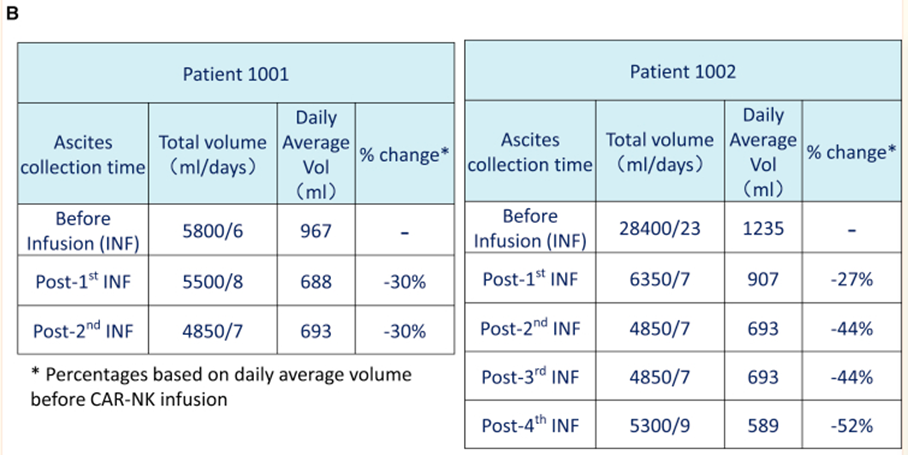
图3 患者治疗前后腹水量变化(图源:[4])
尽管CAR-T及CAR-NK细胞取得了瞩目的成果,但是其不足也是存在的,其中最有待解决的便是细胞的耗竭及治疗实体肿瘤疗效差,这导致需要探索其他新手段提高其疗效。
近年来,间充质干细胞(MSCs)逐渐被用来与CAR-细胞协同使用,以解决CAR-细胞不足的问题。
MSCs可分泌多种趋化因子和细胞因子,能够启动急性免疫反应,从而维持CAR-T细胞的活动;此外,MSCs可以作为载体向肿瘤组织输送生物活性蛋白(支持性细胞因子)和转基因免疫调节剂等,这会导致肿瘤床从最初的抑制状态转移到免疫刺激环境,从而支持CAR-T细胞活性和提高其抗肿瘤侵袭性。
小结与展望
随着CAR-细胞的不断研究,目前可通过确定最佳的肿瘤相关抗原,可以最大限度地发挥CAR-细胞的潜力。然而,其既有优势,也有局限性,如细胞靶向性低、持久性差及免疫抑制环境等。上述问题有望通过应用MSCs来克服,MSCs从提供多种抗肿瘤药物(包括溶瘤病毒和肿瘤特异性前体药物)到引入免疫调节蛋白(如趋化因子和白介素类),MSC的各种潜力不仅增强了CAR相关免疫治疗的疗效,而且为实体肿瘤治疗提供了一个充满希望的未来。未来,随着CAR-细胞和MSCs的联合应用,有望为实体肿瘤患者提供多一种治疗希望!
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


