研究揭秘CSN6如何调控肥胖人群肝细胞癌进展
来源:网络 2024-04-23 09:00
研究团队构建了患者来源的肿瘤异种移植模型,发现在CSN6高表达的肿瘤中, 靶向抑制HMGCS1提高了YAP1抑制剂的疗效。该研究确定了CSN6-HMGCS1-YAP1轴在介导HCC发生发展中的关键作用
近日,附属第六医院胃肠病学研究所李孟鸿教授及其合作团队在Advanced Science(2022IF=15.1)杂志上发表了题为 “CSN6-SPOP-HMGCS1 Axis Promotes Hepatocellular Carcinoma Progression via YAP1 Activation” 的研究论文。该研究发现COP9信号小体亚基6 (CSN6) 通过拮抗斑点型POZ蛋白 (SPOP) 泛素连接酶稳定HMGCS1,进而激活YAP1促进肿瘤的生长,为靶向肿瘤代谢异常的精准治疗提供了新思路。
目前,肝癌是一个全球性的健康问题,其发病率和死亡率在世界范围内不断上升,其中,肝细胞癌 (Hepatocellular carcinoma, HCC) 是最常见的肝癌形式,大约占肝癌总病例数的90%。超过90%的HCC病例发生在有慢性肝病的背景下,任何造成肝硬化的病因都是HCC的危险因素,主要包括乙肝或丙肝病毒感染、慢性饮酒、糖尿病或肥胖相关的非酒精性脂肪肝病(Non-alcoholic fatty liver diseases, NAFLD) 等。随着肥胖的流行,NAFLD预计将成为未来HCC的主要原因,而胆固醇升高是NAFLD相关癌症的重要指标之一,胆固醇由乙酰辅酶A经过30步酶促反应合成,即甲羟戊酸 (MVA) 合成途径。研究靶向胆固醇合成途径,有利于发现更加安全有效的NAFLD相关HCC的治疗方案与策略。
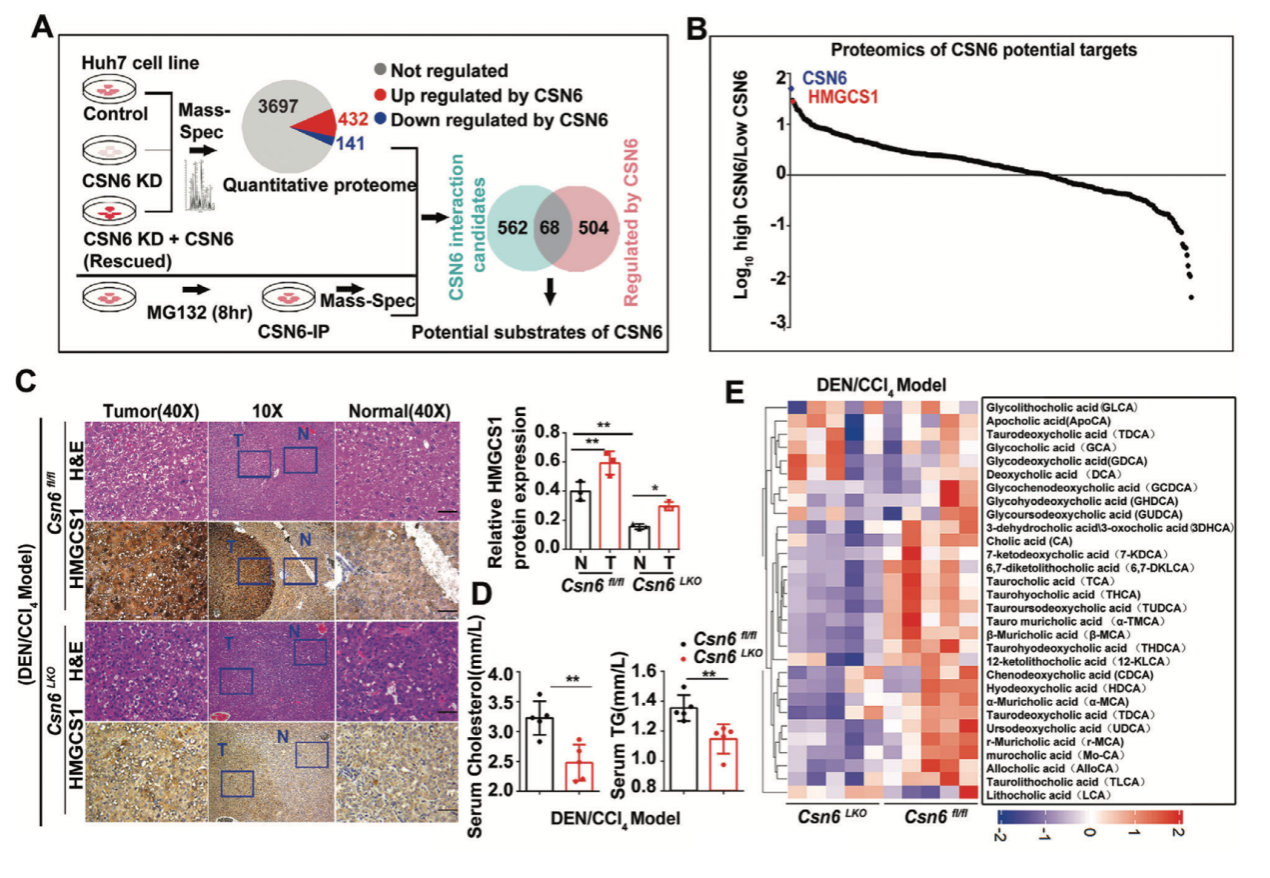
研究团队采用大数据进行联合肝癌组织微阵列免疫组化分析,发现CSN6在肿瘤组织中表达上调且与病人生存率低显著相关。进一步,采用CRISPR-Cas9基因编辑系统构建肝脏特异性CSN6基因敲除小鼠,通过构建原位肝癌自发模型,研究团队发现肝脏特异性敲除CSN6可抑制肝脏肿瘤生长,并降低小鼠血液胆固醇水平,这提示CSN6在肝癌发生发展中发挥重要作用。
为了阐明CSN6在肝癌中的作用机制,研究团队通过免疫共沉淀质谱和定量蛋白质组学分析,确定了68个潜在的CSN6直接作用靶点,并发现CSN6直接结合并调控HMGCS1(MVA合成相关途径关键酶,催化乙酰乙酰辅酶A,生成β-羟基-β-甲基戊二酰辅酶A(HMG-CoA))的蛋白质水平。进一步,发现CSN6可以调节MDM2的稳定性,从而破坏E3连接酶SPOP的稳定性,对抗SPOP介导的HMGCS1的泛素化和降解过程。因此,CSN6调控HMGCS1蛋白的稳定性,进而促进MVA途径和YAP1的转录激活,从而促进肿瘤的恶性进展。本研究第一次鉴定两个知名E3连接酶MDM2和SPOP之间存在相互调控,发现MDM2为知名抑癌基因SPOP的E3连接酶,提示SPOP除了在肿瘤突变之外,其低表达也是诱发肿瘤的重要因素之一。
最后,研究团队构建了患者来源的肿瘤异种移植模型,发现在CSN6高表达的肿瘤中, 靶向抑制HMGCS1提高了YAP1抑制剂的疗效。该研究确定了CSN6-HMGCS1-YAP1轴在介导HCC发生发展中的关键作用。
综上,该研究通过临床组织芯片,基因敲除小鼠和蛋白质组学等手段,鉴定了肥胖以及NAFLD相关肝癌发生发展的分子机制,解释了脂代谢异常与肝癌进展的潜在原因,为NAFLD相关HCC患者的临床治疗提供了潜在的指导策略与方法。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


