Hepatology:揭示乙肝病毒和丁肝病毒如何在肝细胞中建立感染
来源:本站原创 2019-06-25 15:01
2019年6月25日讯/生物谷BIOON/---在一项新的研究中,来自美国普林斯顿大学的研究人员开发出一种新的可扩展的细胞培养系统,它允许对宿主细胞如何应对乙型肝炎病毒(HBV,又称乙肝病毒)和丁型肝炎病毒(HDV,又称丁肝病毒)感染进行了详细调查。相关研究结果于2019年6月17日在线发表在Hepatology期刊上,论文标题为“Analysis of host responses to hep
2019年6月25日讯/生物谷BIOON/---在一项新的研究中,来自美国普林斯顿大学的研究人员开发出一种新的可扩展的细胞培养系统,它允许对宿主细胞如何应对乙型肝炎病毒(HBV,又称乙肝病毒)和丁型肝炎病毒(HDV,又称丁肝病毒)感染进行了详细调查。相关研究结果于2019年6月17日在线发表在Hepatology期刊上,论文标题为“Analysis of host responses to hepatitis B and delta viral infections in a micro‐scalable hepatic co‐culture system”。
HBV引起的急性疾病通常可由具有完整免疫系统的成年人迅速清除,但是幼儿和HIV患者特别容易患上慢性HBV感染,这可能导致肝硬化或肝癌。 HBV感染也让人容易感染HDV,这可能导致急性肝衰竭和/或加速进展为肝硬化或肝癌。幸运的是,HBV存在有效的疫苗,并且鉴于HDV需要HBV才能复制,因此这两者都可以被认为是可预防的疾病。然而,疫苗的费用和有限的可用性让全世界有数百万人面临感染风险。
更好地了解病毒HBV和HDV如何影响它们感染的细胞将有助于开发抗击甚至治愈感染的药物,但是这两种病毒仅感染来自人类和黑猩猩的肝细胞(hepatocyte, 译者注:也可译为肝实质细胞,在本文中未特地说明时,肝细胞指的是肝实质细胞)。这些细胞很难获得,并且当在体外的细胞培养液中培养时,它们经历一种称为去分化(de-differentiation)的过程:在短短几天的过程中,它们失去它们特有的特征和功能。当这种情况发生时,它们也失去了被HBV和HDV感染的能力,从而成为研究慢性病毒感染的重大障碍。
论文通讯作者、普林斯顿大学分子生物学系副教授兼领导人Alexander Ploss说道,“自20世纪80年代中期以来,人们已经尝试在原代人肝细胞(PHH)中建立稳健且重要的持续性感染,但效果有限。”
对其他组织的研究已表明特殊的细胞类型有时需要其他细胞类型的支持来维持它们的分化状态。肝实质细胞构成肝脏中的大部分细胞,但是肝脏组织也含有许多其他的细胞类型,它们统称为“肝非实质细胞(non-parenchymal cell)”。最近,研究生Benjamin Winer与Ploss实验室和胡日勒公司(Hurel Corporation)的同事们已证实新鲜分离的人肝细胞能够与肝非实质细胞一起生长在由胶原蛋白制成的支撑表面上。在这种他们称为原代人肝细胞自组装共培养物(self-assembling co-culture of primary human hepatocytes, SACC-PHH)的细胞培养系统中,肝细胞保持它们的分化状态,并能够支持慢性HBV感染长达40天。
Ploss说道,“这种系统为研究宿主对肝炎病毒的反应创造了前所未有的机会,特别是在持续感染的情况下。”
在这项新的研究中,Winer及其同事们研究了肝细胞如何应对HBV和HDV感染。首先,他们测试了SACC-PHH是否能够支持这两种病毒的感染。HBV劫持肝细胞的蛋白制造机器来制造病毒蛋白,HDV利用HBV蛋白进行自我组装。因此,HDV仅能在与HBV同时感染(co-infection, 共感染)的肝细胞中或者在已遭受HBV慢性感染(super-infection, 重叠感染)的肝细胞中复制。这些研究人员发现这两种情况都可能发生在SACC-PHH中,即使这种细胞培养系统已经缩小到很小的384微孔培养板---这一进展使得这种系统非常适合候选药物的高通量筛选。因此,他们发现使用两种候选抗病毒药物恩替卡韦(entecavir)和Myrcludex B进行预防性治疗能够降低SACC-PHH中这两种肝炎病毒的水平。
病毒感染引起宿主细胞的许多变化,从代谢适应到能够识别和破坏细胞内病毒的先天免疫防御的激活。为了探究肝细胞在遭受HBV/HDV感染时经历的变化,这些研究人员通过使用RNA-Seq分析技术来研究哪些基因表达。这些数据显示受到HBV感染的肝细胞表现出参与氧化磷酸化和与细胞外环境相互作用的基因表达升高。相反,进一步受到HDV感染的肝细胞具有与未受到感染的肝细胞相似的基因表达模式。
有趣的是,尽管这些肝细胞的先天免疫信号转导通路是完整的并且可以通过添加聚肌胞苷酸(poly(I:C))化学物来加以刺激,但是HBV感染并未激活这些防御。另一方面,用聚肌胞苷酸治疗有助于抑制HBV生长,这表明这种病毒在细胞防御的监视下建立持续感染。
先天免疫防御如何影响HBV/HDV共感染似乎显得更加微妙。用聚肌胞苷酸刺激先天免疫通路对HDV几乎没有影响。HBV/HDV共感染也未能激活所研究的大多数人类供者的肝细胞中的防御途径,但是有些人类供者在这种共感染时显示出先天免疫激活,这表明人的基因构成可能影响他们抵抗感染的能力。
Ploss说,“我们相信,我们的经过优化的高通量SACC-PHH平台是研究嗜肝性病原体的独特资源,而且我们的数据将有助于推进对HBV和HDV持续感染的了解。” (生物谷 Bioon.com)
参考资料:
Benjamin Y. Winer et al, Analysis of host responses to hepatitis B and delta viral infections in a micro-scalable hepatic co-culture system, Hepatology (2019). DOI: 10.1002/hep.30815.

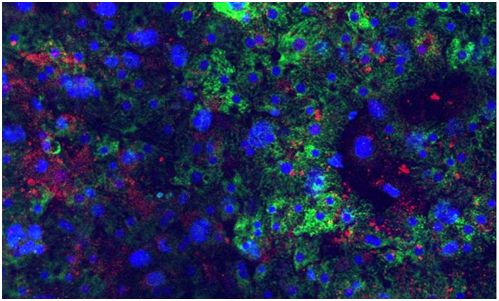
图片来自Winer et al., Princeton University。
HBV引起的急性疾病通常可由具有完整免疫系统的成年人迅速清除,但是幼儿和HIV患者特别容易患上慢性HBV感染,这可能导致肝硬化或肝癌。 HBV感染也让人容易感染HDV,这可能导致急性肝衰竭和/或加速进展为肝硬化或肝癌。幸运的是,HBV存在有效的疫苗,并且鉴于HDV需要HBV才能复制,因此这两者都可以被认为是可预防的疾病。然而,疫苗的费用和有限的可用性让全世界有数百万人面临感染风险。
更好地了解病毒HBV和HDV如何影响它们感染的细胞将有助于开发抗击甚至治愈感染的药物,但是这两种病毒仅感染来自人类和黑猩猩的肝细胞(hepatocyte, 译者注:也可译为肝实质细胞,在本文中未特地说明时,肝细胞指的是肝实质细胞)。这些细胞很难获得,并且当在体外的细胞培养液中培养时,它们经历一种称为去分化(de-differentiation)的过程:在短短几天的过程中,它们失去它们特有的特征和功能。当这种情况发生时,它们也失去了被HBV和HDV感染的能力,从而成为研究慢性病毒感染的重大障碍。
论文通讯作者、普林斯顿大学分子生物学系副教授兼领导人Alexander Ploss说道,“自20世纪80年代中期以来,人们已经尝试在原代人肝细胞(PHH)中建立稳健且重要的持续性感染,但效果有限。”
对其他组织的研究已表明特殊的细胞类型有时需要其他细胞类型的支持来维持它们的分化状态。肝实质细胞构成肝脏中的大部分细胞,但是肝脏组织也含有许多其他的细胞类型,它们统称为“肝非实质细胞(non-parenchymal cell)”。最近,研究生Benjamin Winer与Ploss实验室和胡日勒公司(Hurel Corporation)的同事们已证实新鲜分离的人肝细胞能够与肝非实质细胞一起生长在由胶原蛋白制成的支撑表面上。在这种他们称为原代人肝细胞自组装共培养物(self-assembling co-culture of primary human hepatocytes, SACC-PHH)的细胞培养系统中,肝细胞保持它们的分化状态,并能够支持慢性HBV感染长达40天。
Ploss说道,“这种系统为研究宿主对肝炎病毒的反应创造了前所未有的机会,特别是在持续感染的情况下。”
在这项新的研究中,Winer及其同事们研究了肝细胞如何应对HBV和HDV感染。首先,他们测试了SACC-PHH是否能够支持这两种病毒的感染。HBV劫持肝细胞的蛋白制造机器来制造病毒蛋白,HDV利用HBV蛋白进行自我组装。因此,HDV仅能在与HBV同时感染(co-infection, 共感染)的肝细胞中或者在已遭受HBV慢性感染(super-infection, 重叠感染)的肝细胞中复制。这些研究人员发现这两种情况都可能发生在SACC-PHH中,即使这种细胞培养系统已经缩小到很小的384微孔培养板---这一进展使得这种系统非常适合候选药物的高通量筛选。因此,他们发现使用两种候选抗病毒药物恩替卡韦(entecavir)和Myrcludex B进行预防性治疗能够降低SACC-PHH中这两种肝炎病毒的水平。
病毒感染引起宿主细胞的许多变化,从代谢适应到能够识别和破坏细胞内病毒的先天免疫防御的激活。为了探究肝细胞在遭受HBV/HDV感染时经历的变化,这些研究人员通过使用RNA-Seq分析技术来研究哪些基因表达。这些数据显示受到HBV感染的肝细胞表现出参与氧化磷酸化和与细胞外环境相互作用的基因表达升高。相反,进一步受到HDV感染的肝细胞具有与未受到感染的肝细胞相似的基因表达模式。
有趣的是,尽管这些肝细胞的先天免疫信号转导通路是完整的并且可以通过添加聚肌胞苷酸(poly(I:C))化学物来加以刺激,但是HBV感染并未激活这些防御。另一方面,用聚肌胞苷酸治疗有助于抑制HBV生长,这表明这种病毒在细胞防御的监视下建立持续感染。
先天免疫防御如何影响HBV/HDV共感染似乎显得更加微妙。用聚肌胞苷酸刺激先天免疫通路对HDV几乎没有影响。HBV/HDV共感染也未能激活所研究的大多数人类供者的肝细胞中的防御途径,但是有些人类供者在这种共感染时显示出先天免疫激活,这表明人的基因构成可能影响他们抵抗感染的能力。
Ploss说,“我们相信,我们的经过优化的高通量SACC-PHH平台是研究嗜肝性病原体的独特资源,而且我们的数据将有助于推进对HBV和HDV持续感染的了解。” (生物谷 Bioon.com)
参考资料:
Benjamin Y. Winer et al, Analysis of host responses to hepatitis B and delta viral infections in a micro-scalable hepatic co-culture system, Hepatology (2019). DOI: 10.1002/hep.30815.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


