Nat Commun | 高平/杨显珠/张华凤/钟秀颖发现HKDC1促进肝细胞癌的肿瘤免疫逃逸
来源:生物探索 2024-02-20 10:06
该研究揭示了HKDC1通过募集胞质内的STAT1到细胞质膜上的IFNGR1来促进肿瘤免疫逃避的作用,从而揭示了HCC的治疗脆弱性。
华南理工大学高平、杨显珠、中国科学技术大学张华凤和南方医科大学钟秀颖共同通讯在Nature Communications 发表题为“HKDC1 promotes tumor immune evasion in hepatocellular carcinoma by coupling cytoskeleton to STAT1 activation and PD-L1 expression”的研究论文,本研究表明己糖激酶结构域组1(HKDC1) 通过激活肿瘤细胞中的STAT1/PD-L1以CD8+T细胞依赖性方式促进肿瘤免疫逃避。
从机制上讲,HKDC1 通过与细胞骨架蛋白ACTA2结合,在IFNγ刺激后将胞质上的STAT1与IFNGR1结合并呈现在细胞膜上,导致STAT1磷酸化和核转。在雄性小鼠肝癌模型中,抑制HKDC1与抗PD-1/PD-L1联合增强体内T细胞抗肿瘤反应。临床样本分析表明,在接受阿替利珠单抗(抗PPD-L1)治疗的肝细胞癌患者中,HKDC1表达、STAT1磷酸化和生存期之间存在相关性。这些发现揭示了HKDC1通过耦联细胞骨架与STAT1激活来调节免疫逃避的作用,提供了一种潜在的联合策略来增强抗肿瘤免疫应答。

癌细胞采用多种策略来逃避免疫检测并克服免疫反应,统称为适应性免疫抵抗(AIR)。第一个经过实验定义和治疗验证的 AIR 机制是通过干扰素-γ(IFNγ)在肿瘤中选择性诱导程序性细胞死亡1配体1(PD-L1)。尽管目前通过ICB破坏肿瘤免疫逃逸的疗法在15-20% 的患者中显示出强大的抗肿瘤功效,但在大多数患者中,免疫逃逸和治疗耐药导致较弱的临床应答,其机制基本上未知。因此,联合疗法为克服PD-1/PD-L1耐药性和提高反应率提供了一种潜在的有效方法。不幸的是在没有强有力的机制基础的情况下,抗PD-1/PD-L1与其他抗肿瘤药物联合的临床试验,未能显示出协同作用。因此,迫切需要将抗PD-1/PD-L1 ICB与疗效预测标志物相结合的新型联合疗法。
癌细胞中的代谢重编程不仅为维持肿瘤发生和癌症发展提供生物能量和生物合成前体,而且还通过消耗TME中的有效营养物质,促进免疫抑制代谢物分泌和调节免疫信号分子表达来调节抗肿瘤免疫反应。然而,许多在肿瘤细胞中被激活的代谢通路也是抗肿瘤免疫细胞活性所必需的,因此很难在患者获益的同时阻断这些通路。因此,特异性抑制或改变肿瘤代谢的靶点有可能产生有效的抗肿瘤免疫应答。有趣的是,代谢酶最近被发现具有直接调节癌细胞基因表达的功能。然而,由于肿瘤发展是一个复杂的过程,涉及许多代谢酶和调节分子,目前尚不清楚其他代谢酶是否以及哪些其他代谢酶也可以调节肿瘤免疫,如果可以,通过什么调节机制。
己糖激酶(HK)依赖性葡萄糖磷酸化是糖酵解的限速步骤。在哺乳动物细胞中已鉴定出五种HK同工酶(包括HK1-4和HKDC1),每种同工酶都具有不同的亚细胞定位、动力学、底物特异性和生理功能。在巨噬细胞中,抑制HK1依赖性糖酵解会抑制LPS和ATP诱导的il -1β前体成熟和caspase-1活化,表明HK1依赖性糖酵解在调节NLRP3炎症小体激活中起重要作用。HK2可作为模式识别受体检测N-乙酰氨基葡萄糖的释放并激活巨噬细胞中 NLRP3炎症小体的形成。
胶质母细胞瘤细胞中异常增强的有氧糖酵解促进HK2从线粒体解离到磷酸化IκBα作为蛋白激酶。IκBα磷酸化导致其降解和NF-κB激活依赖的PD-L1表达肿瘤免疫逃逸。HKDC1是最近发现的一种人类己糖激酶,其异常表达与癌症患者的总生存率密切相关。然而,通过RNAi或CRISPR敲低或敲除HKDC1表明,在混合筛选中,HKDC1对细胞活力不是必需的。此外,HKDC1在肝细胞中表现出较低的葡萄糖磷酸化活性,这表明HKDC1可能具有超越其经典己糖激酶活性的“兼职”功能。
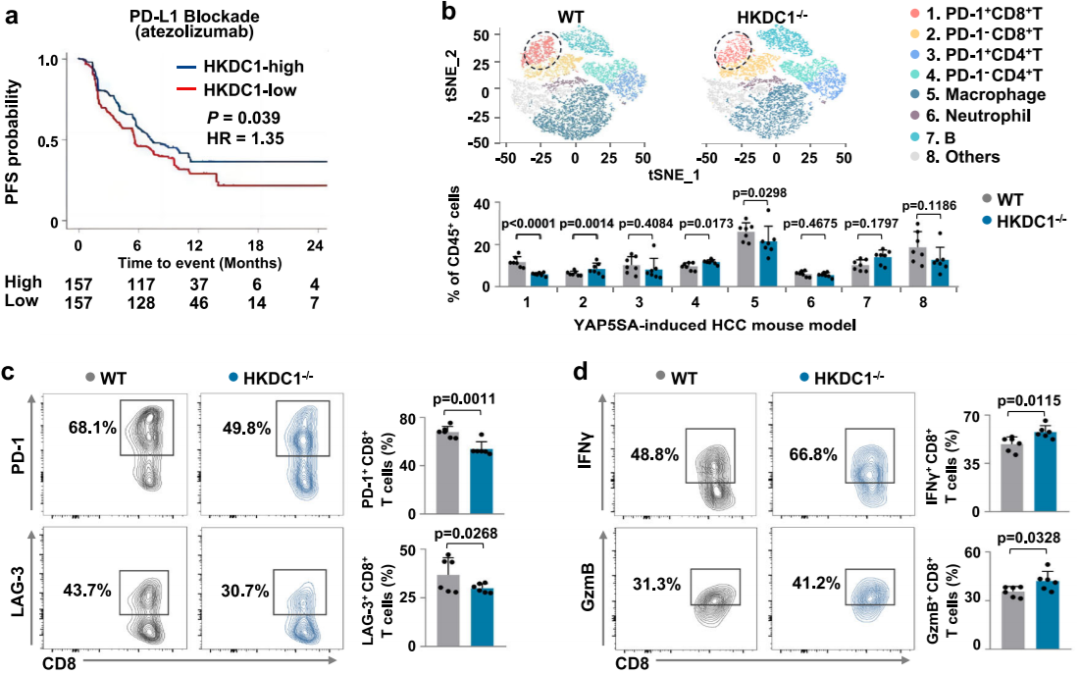
HKDC1表达与HCC进展和肿瘤浸润CD8+ T细胞耗竭相关(Credit: Nature Communications)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


