上海交通大学:WWP1靶向MUC1泛素介导的溶酶体降解抑制癌变
来源:本站原创 2021-08-28 16:54
2021年8月28日讯/生物谷BIOON/---粘蛋白1(MUC1)含有N-和C-亚基,在腔上皮细胞的顶端表面形成异源二聚体。然而,MUC1在多种癌症中异常过表达,如乳腺癌、肺癌和前列腺癌,这对肿瘤的发生和不良的临床结果起着至关重要的作用。
2021年8月28日讯/生物谷BIOON/---粘蛋白1(MUC1)含有N-和C-亚基,在腔上皮细胞的顶端表面形成异源二聚体。然而,MUC1在多种癌症中异常过表达,如乳腺癌、肺癌和前列腺癌,这对肿瘤的发生和不良的临床结果起着至关重要的作用。针对MUC1的靶向抑制已经开发了几种策略,包括疫苗、单克隆抗体(MAb)和多肽。疫苗通常识别MUC1-N的VNTR中的异常糖基化区域,单抗主要针对MUC1-N,但收效甚微,多肽抑制剂被应用于通过MUC1-C的CQC基序阻断二聚化,其中多肽抑制剂GO203已进入临床试验。然而,目前没有一种针对MUC1的靶向疗法在临床治疗中是可行的。MUC1在肿瘤中的过度表达部分是由于基因扩增和转录增加所致。但人们对MUC1蛋白是如何维持的知之甚少。破译MUC1降解的机制将为减少癌症中MUC1的丰度提供一种新的策略。
图片来源:https://doi.org/10.1038/s41392-021-00660-x
为了发现MUC1的新调控因子,作者进行了LC-MS/MS分析,并鉴定了与MUC1相互作用的WW结构域的泛素E3连接酶1(WWP1)。在乳腺癌、肝癌和非小细胞肺癌细胞系中检测到MUC1和WWP1的蛋白水平呈负相关。一致地,使用互补的遗传方法,作者发现WWP1在蛋白质水平而不是在mRNA水平负调控MUC1。WWP1以剂量依赖性的方式降低MUC1丰度。WWP1的过表达显著缩短了MUC1蛋白的半衰期。这些结果表明WWP1触发了MUC1蛋白的周转。
此外,溶酶体抑制剂氯喹(CQ)而不是蛋白酶体抑制剂MG132显著抑制了WWP1介导的MUC1的降解,提示WWP1通过溶酶体途径诱导MUC1的降解。WWP1诱导的MUC1和LAMP2的共定位进一步证实了这一结果。使用抑制剂来检测WWP1降解MUC1的亚细胞位置。结果证实,只有CPZ(一种依赖于笼蛋白的内吞作用的抑制剂)显著阻止WWP1介导的MUC1降解,这表明依赖于笼蛋白的内吞作用起着至关重要的作用。免疫荧光染色显示WWP1增加了早、晚期内体MUC1的水平,降低了循环内小体的MUC1水平。雷帕霉素激活自噬促进BT549细胞WWP1依赖的MUC1降解。综上所述,这些结果表明WWP1通过网囊酶介导的内切酶/溶酶体途径降解MUC1。
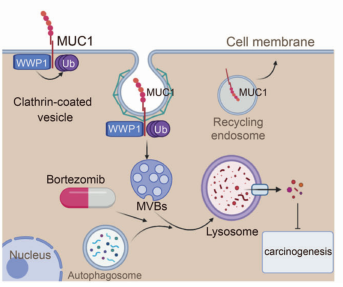
该示意图描述了WWP1介导的MUC1在癌症中的溶酶体降解模型
图片来源:https://doi.org/10.1038/s41392-021-00660-x
MUC1在细胞膜上过表达,参与多种致癌信号通路(如EGFR和β-catenin等),促进肿瘤的发生。该研究表明WWP1可以通过溶酶体途径降解膜MUC1,从而抑制肿瘤生长。重要的是,作者验证了蛋白酶体抑制剂bortezomib在促进WWP1介导的MUC1降解中的作用,为WWP1/MUC1阳性肿瘤的治疗提供了一种新的策略。(生物谷 Bioon.com)
参考文献
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。



