Molecular Therapy Nucleic Acids: CDR1as通过控制miR-7的可获得性调节α-突触核蛋白介导的缺血性脑损伤
来源:生物谷原创 2023-01-30 14:57
局灶性脑缺血迅速改变了几类非编码RNA(NcRNAs)的表达,包括环状RNAs(CircRNAs)、微小RNAs(MiRNAs)和长ncRNAs(LncRNAs)。
局灶性脑缺血迅速改变了几类非编码RNA(NcRNAs)的表达,包括环状RNAs(CircRNAs)、微小RNAs(MiRNAs)和长ncRNAs(LncRNAs)。它们可以通过影响染色质结构、RNA/蛋白质支架、增强子功能、选择性剪接、RNA稳定性、转录和翻译来影响缺血后的功能结果。
ncRNA相互调节,这对它们在细胞环境中的功能和稳定性至关重要。通过5‘端和3’端的反向剪接和共价连接形成的CircRNA对消化线性RNA的核酸外切酶具有抗性。许多CircRNAs海绵miRNAs或蛋白质,从而调节转录和翻译。

图片来源:https://doi.org/10.1016/j.omtn.2022.11.022.
近日,来自威斯康星大学麦迪逊分校的研究者们在Molecular Therapy: Nucleic Acids杂志上发表了题为“CDR1as regulates a-synuclein-mediated ischemic brain damage by controlling miR-7 availability”的文章,该研究的发现表明,CDR1as重建对中风后的神经具有保护作用,可能是通过保护miR-7和防止a-Syn介导的神经元死亡。
短暂性局灶性脑缺血降低了microRNA-7(miR-7)水平,导致其主要靶标α-突触核蛋白(a-Syn)表达下降,从而促进继发性脑损伤。已知环状RNA CDR1as调节miR-7的丰度和功能。因此,研究者评估了它在局灶性脑缺血后的功能意义。
成年小鼠大脑中动脉短暂性闭塞(MCAO)后,再灌流3h~72h,梗死灶周围皮质CDR1as和miR-7水平显著降低。有趣的是,在缺血脑中,pri-miR-7a和7b都没有改变。脑内注射含有CDR1as基因的AAV9载体后,在假手术组和MCAO组,CDR1as水平在21天内显著升高,并持续到4个月,没有引起任何明显的毒性。
短暂性脑缺血再灌注1d,AAV9-CDR1AS组梗死灶周围皮质miR-7水平及与Ago2/miR-7结合的CDR1as均显著高于AAV9-对照组。与AAV9对照治疗组相比,CDR1as过表达显著抑制了卒中后α-Syn蛋白的诱导,促进了运动功能的恢复,缩小了梗塞面积,并减少了卒中后脑内细胞凋亡、自噬、线粒体碎裂和炎症的标志物。
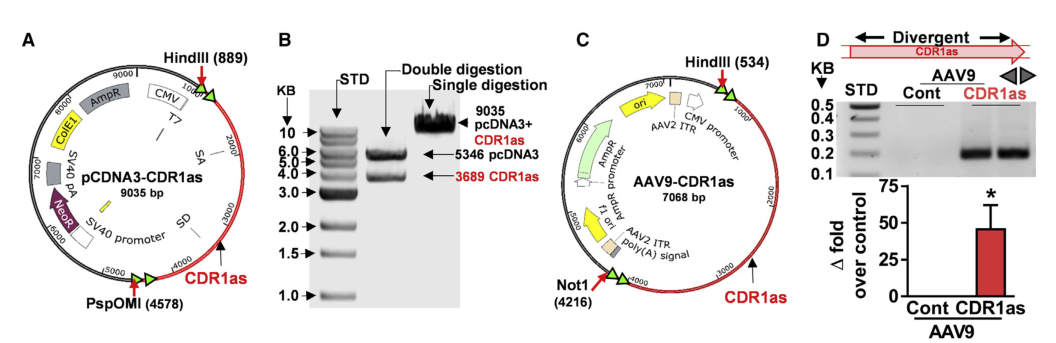
CDR1as过表达可提高CDR1as水平,但不影响正常生理功能
图片来源:https://doi.org/10.1016/j.omtn.2022.11.022
CDR1as可以被包装在细胞外小泡(EV)和/或脂质体中,并可以在体内传递(IV)以增加翻译潜力。虽然研究者将在未来的研究中对此进行测试,但其他研究者们最近验证了一种类似的RNA药物输送方法,以使用EVS在小鼠和猴子中靶向功能恢复的卒中后给予CircRNA CircSCMH1(IV)。
总体而言,目前的发现表明,靶向CircRNA CDR1as是一种新的治疗策略,可以有效地控制miR-7/a-Syn,将中风后的脑损伤降至最低。(生物谷 Bioon.com)
参考文献
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


