中国首例!士泽生物成功实施临床级iPS衍生细胞移植治疗帕金森病给药
来源:士泽生物 2024-02-11 11:19
士泽生物的治疗成本不及美国同类治疗成本的三十分之一,对追求个性化治疗帕金森病有实质需求的中国及全球帕金森病患者更加经济可及,具有明确的市场化竞争优势。
士泽生物医药(苏州/上海)有限公司(Roche Accelerator Member;以下简称“士泽生物”)临床级自体iPSC衍生多巴胺能神经前体细胞注射液经颅内立体定位注射微创手术方式移植治疗帕金森病在上海市东方医院(同济大学附属东方医院)(以下简称”东方医院“)成功完成。据悉,这是中国首例临床级iPS衍生细胞移植治疗帕金森病,也是中国首例、世界第二例自体iPS衍生细胞替代性移植治疗帕金森病。
此次士泽生物与合作医院完成的中国首例、世界第二例临床级自体iPS衍生细胞治疗帕金森病的神经外科微创手术移植在两小时以内完成:首例受试者接受临床级iPS衍生细胞移植后,无手术及围术期的并发症或其他不良安全事件,各项检测指标正常且已顺利出院,平稳度过观察期并进入正式随访期。

此次已成功实施的中国首例iPS衍生细胞治疗帕金森病移植给药,由国家卫生健康委员会和国家药品监督管理局(简称两委)正式批准开展临床:是我国首个经国家两委局批准开展的iPS衍生细胞治疗帕金森病的临床研究,也是我国迄今为止唯一一个正式获批的iPS衍生细胞治疗神经系统疾病的国家级干细胞备案临床研究项目(批准开展临床号:MR-31-24-001927)。

帕金森病(Parkinson's disease,PD)是全球第二大神经退行性疾病,我国是全球帕金森病第一大国,帕金森病主要致病原因为中脑黑质区多巴胺能神经元发生了退行性病变和死亡,进而引起震颤、运动迟缓、肢体僵硬、步态异常等运动功能的逐步退化,直至病人死亡。我国65岁以上人群中,帕金森病发病率约为1.7%,预计至2030年,我国帕金森病患者人数将达到500万左右,现有的传统药物治疗或手术治疗不能再生多巴胺能神经元或解决神经元退行性病变和死亡的问题,尚不能改变帕金森病的疾病发展进程。
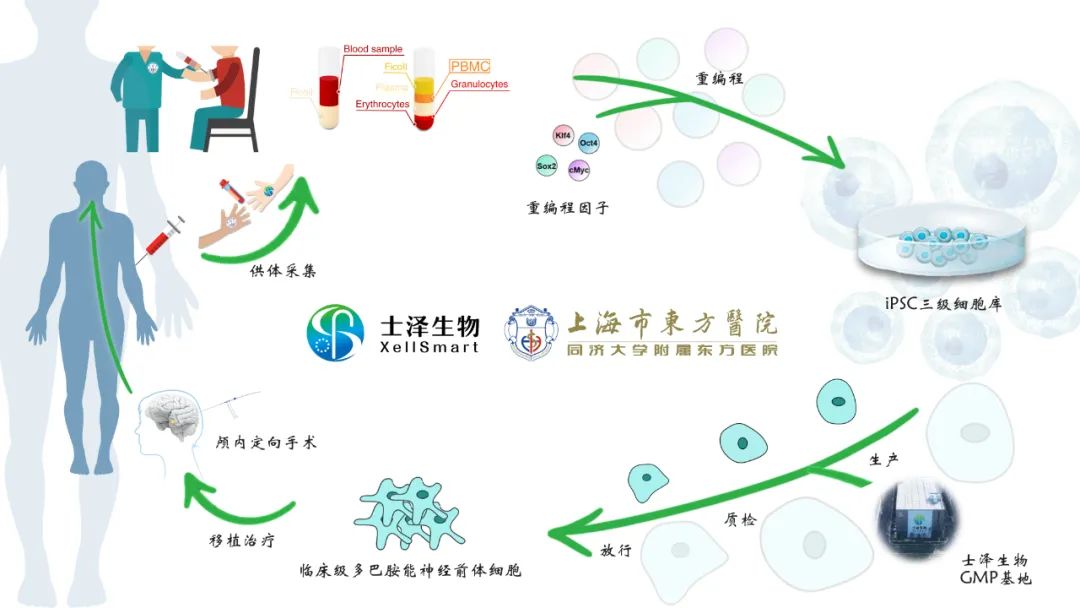
本次士泽生物与上海市东方医院合作完成的中国首例、世界第二例自体iPS衍生细胞替代性移植治疗中重度帕金森病,依托士泽生物已建立的一站式全流程的临床级iPS衍生亚型多巴胺能神经前体细胞注射液的制备工艺流程、质量控制及制剂放行体系:
对患者自体来源的供体细胞建系的临床级iPS细胞库进行临床级亚型多巴胺能神经前体细胞的诱导分化,在克服异体细胞移植可能产生免疫排斥影响细胞存留及功能活性的同时,通过颅内立体定位注射神经外科微创手术方式进行神经再生性移植治疗,对中国首例式临床研究再生多巴胺能神经细胞移植治疗帕金森病的安全性并分析对帕金森病患者疗效的影响具有重要的标杆意义。
士泽生物诱导制备的高纯度亚型特化多巴胺能神经前体神经细胞产品质量标准已达国际领先水平,并已在临床前帕金森病小动物模型及中重度帕金森病非人灵长类模型上进行了系统的评估和验证,成药性优异,论证了士泽生物iPS衍生多巴胺能神经前体细胞移植治疗安全有效。士泽生物已建设完成的>5000平方米的研发中心、GMP中试基地及质控中心可充分保障获国家两委局正式批准开展的中国首个iPS衍生细胞药治疗帕金森病临床研究项目的临床级iPS衍生多巴胺能神经前体细胞制剂的生产、质控和放行。

李翔博士
士泽生物创始人李翔博士表示:士泽生物此次顺利完成的临床给药:为中国首例临床级iPS衍生细胞移植治疗帕金森病,也是中国首例、世界第二例个性化自体iPS衍生细胞替代性移植治疗帕金森病,为中国iPS衍生细胞治疗帕金森病留下了中国“首个及首例”的行业记忆!
士泽生物此次开展的临床研究项目由国家卫生健康委员会和国家药品监督管理局正式批准开展:是我国首个iPS衍生细胞治疗帕金森病的国家级备案干细胞临床研究项目,也是我国迄今为止唯一一个获得国家两委局正式批准开展的iPS衍生细胞治疗神经系统疾病的国家级临床研究项目。
士泽生物获得两委局正式批准开展中国首个临床研究及已经顺利完成个性化自体iPS衍生多巴胺能神经前体细胞的临床级注射液的生产、质检、放行及与合作医院完成的临床微创移植,是对士泽生物自主运营和已经建立的临床级iPS衍生细胞注射液治疗帕金森病的整体产品及管理体系,和GMP规范下的临床级iPS衍生细胞的“生产-制备-放行”的一站式平台能力的重要验证和论证。
相对美国已经完成全世界第一例的实验室级别自体iPS衍生细胞移植治疗帕金森病,中国士泽生物自研及国产的临床级iPS衍生细胞注射液,具有多方面的显著对比优势,其中,士泽生物的治疗成本不及美国同类治疗成本的三十分之一,对追求个性化治疗帕金森病有实质需求的中国及全球帕金森病患者更加经济可及,具有明确的市场化竞争优势。
自士泽生物在合作医院发起临床招募以来,全国帕金森病患者报名意愿强烈,更加凸显出作为全世界帕金森病第一大国,中重度帕金森病未被满足的重大临床刚需。士泽生物团队将严格遵守医学及伦理要求,与合作医院临床及管理团队一起,以科学严谨的态度推进后续国家级干细胞备案临床研究工作,不忘初心,不懈进取。
期待最终能够为帕金森病患者开发出安全、有效、可控及经济可及的,或实现高价值个性化医疗的,具有实质临床获益的细胞药物和解决方案!
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


