Cell:解析出蛋白LRP2的三维低温电镜结构
来源:生物谷原创 2023-02-21 17:09
在一项新的研究中,来自美国哥伦比亚大学等研究机构的研究人员首次揭示了一种生死攸关的蛋白---LRP2---的三维结构,其清晰度足以最终揭示它是如何起作用的。
细节往往是决定成败的关键。对于协调生命分子业务的蛋白来说,它们的细节中存在着魔鬼和天使,小到组成蛋白的原子。正是在这种结构性的细枝末节上,健康和疾病,甚至生命和死亡的平衡可能会发生转折。
在一项新的研究中,来自美国哥伦比亚大学等研究机构的研究人员首次揭示了一种生死攸关的蛋白的三维结构,其清晰度足以最终揭示它是如何起作用的:就像一艘载着分子乘客的微型渡轮,它必须穿越从肾脏和大脑到内耳和肺泡等组织和器官中近万亿个细胞的细胞膜。相关研究结果发表在2023年2月16日的Cell期刊上,论文标题为“Structures of LRP2 reveal a molecular machine for endocytosis”。

论文共同通讯作者、哥伦比亚大学瓦格洛斯内外科医生学院的Jonathan Barasch博士说,“随着对这一关键蛋白的新的机理理解,以及它的突变如何使它关闭,我们希望后续研究将发现治疗肾脏和大脑疾病的新靶标。我在哥伦比亚大学的同事Andrew Beenken、Anthony Fitzpatrick和Lawrence Shapiro发现了令人惊奇的这些蛋白结构,这是开发新疗法的突破口。”
Barasch博士和他的合作者们设想,这些新的高分辨率蛋白结构将指向治疗疾病的线索,如急性肾损伤(每年影响美国400多万患者)、慢性肾脏病(影响全球约8亿人)和阿尔茨海默病(估计影响全球3200万人)等流行疾病,以及像唐奈-巴罗综合征(Donnai-Barrow syndrome,影响不到1000名美国人)这样罕见的、具有多种身体和认知后果的遗传疾病。
这种称为LRP2的蛋白是在从线虫到人类的多种生物中发现的LRP蛋白质家族的成员。与细胞膜上的大多数蛋白相比,LRP是巨大的,以至于在20世纪80年代初发现LRP2的科学家Marilyn Farquhar和Dontscho Kerjaschki将它称为megalin。一些LRP是由4600多个氨基酸构建而成的。
在肾细胞中,LRP2对于从体液中过滤的代谢废物中回收可重复使用的分子至关重要,因此身体不必花费能量和资源来再次制造这些分子。对于每个细胞来说,可能有数以万计的LRP2蛋白,像草莓上的种子一样分布在细胞的表面上。
Barasch博士说,“肾脏面临着回收人体通过该器官过滤器的99%的盐和水,还面临着回收100%的小蛋白,否则这些小蛋白会流入尿液并排出体外。关于这种回收是如何进行的,人们已经有了一般的想法,但它的特异性如今得到了解决。”
这就是Barasch博士的同事们发挥作用的地方。其中的一位是论文第一作者Andrew Beenken博士。像LRP家族中的那些膜蛋白是出了名的难以分离,更不用说详细绘制它们的结构了。Beenken博士在这个僵局中迈出了一大步,他在这个过程中使用了大量的生物化学技术。
Shapiro博士说,“当我第一次听说Jonathan和Andrew打算做什么时,我认为这是不可能的。”Shapiro博士在研究蛋白的复杂结构如何产生它们的生物功能方面的专长对破译LRP2的运输机制至关重要。
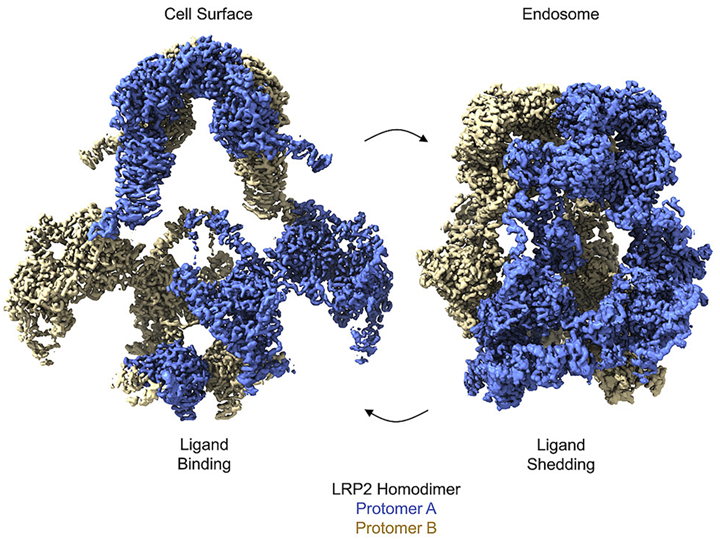
图片来自Cell, 2023, doi:10.1016/j.cell.2023.01.016。
凭借台式技术、创造力和决心,Beenken博士从500个小鼠肾脏中收获了足够的LRP2蛋白,将这种蛋白凝固成足够大小和纯度的样本,以便用高级显微镜技术进行分析。在收集LRP2分子的过程中,Beenken博士完成了一次生化之旅:捕捉到锁定在两种关键构象中的LRP2蛋白,这是揭开该蛋白在细胞中的作用的一个关键实验室壮举。
随后,论文共同通讯作者Anthony Fitzpatrick博士领导的第二个研究步骤。Fitzpatrick是低温电子显微镜领域的领导者,特别适合研究大型蛋白质和其他生物分子。
通过一台两层楼高的液氮冷却的低温电镜,Fitzpatrick博士和Beenken博士利用Beenken博士来之不易的LRP2样本获得了大量的结构数据。然后,通过巧妙地使用强大的计算工具来理解这些数据,他们构建出它的接近原子细节的三维蛋白结构。
Fitzpatrick博士说,“我们如今拥有迄今为止最好的LRP2蛋白三维结构图。有了这些结构图,Shapiro博士(也是这篇论文的通讯作者之一)可以开始弄清LRP2在细胞中发挥作用的非凡机制。”
其中的一种构象捕捉到了LRP2在细胞膜上和细胞内的形状。这就是该蛋白从细胞外的液体---无论是从肾脏中产生的尿液还是从脑细胞周围的液体---获取分子乘客的地方。在这些分子乘客中,有一些小的蛋白,包括tau和β淀粉样蛋白(两者都与阿尔茨海默病有关)、胰岛素和那些在细胞周围穿梭的维生素A和D。
另一种LRP2构象是该蛋白在被一点细胞膜包裹并被运送到细胞内的位置后的构象。正是在这些小囊---内体(endosome)---中,这种改变形状的蛋白要么使得它的分子乘客完整地被回收以进一步使用,要么让它们被分解成可重复使用或一次性的组分。
从这两种LRP2结构中,这些作者能够确定这种蛋白在它们的乘客上船形式和乘客下船形式之间经历了一种类似机器的切换。当LRP2蛋白没有突变时,它们成功地维持了血液和脑组织中的分子平衡。但是,当LRP巨大的分子解剖结构发生微小调整时,这些蛋白就会导致疾病。
例如,在肾细胞中,有缺陷的LRP2蛋白背弃了其正常的任务,即检索否则会在尿液中丢失的蛋白质。这可能导致各种疾病,包括慢性肾脏病、唐奈-巴罗综合征和在新生儿阶段致命的疾病。
在大脑中,LRP2(和相关的LRP1)通常帮助清除多种有毒物质,其中包括长期以来与阿尔茨海默病有关的tau蛋白片段。但是LRP家族的蛋白也被证明可以在脑细胞之间转移这些片段,可能会促成这种疾病的发生。Shapiro博士说,“你可以想象,试图用一种药物来抑制这种情况的发生可能会有帮助。”
这就是低温电镜的强大力量所在。Fitzpatrick博士说,“如果你确切地知道tau蛋白在哪里结合的原子细节,你可能会使用抗体或小分子来阻止它。低温电镜可以让你达到你所需要的细节水平,以便研究潜在的新疗法。”(生物谷 Bioon.com)
参考资料:
Andrew Beenken et al. Structures of LRP2 reveal a molecular machine for endocytosis. Cell, 2023, doi:10.1016/j.cell.2023.01.016.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


