J Hepatol :武汉大学程晓明等团队全基因组siRNA筛选鉴定HBV感染中以前未知的原病毒和抗病毒宿主因子
来源:iNature 2025-12-03 11:21
研究结果不仅揭示了HBV对宿主的高度依赖性,阐明了涉及HNF4A、cccDNA表观遗传调控及细胞周期等具体分子机制,更为针对HBV感染的潜在治疗策略提供了经过验证的宿主靶点。
乙型肝炎病毒(HBV)广泛利用宿主细胞机制完成其感染过程。
2025年11月26日,武汉大学程晓明和美国国立卫生研究院T.Jake Liang共同通讯在Journal of Hepatology 在线发表题为A genome-wide siRNA screen identifies previously unknown proviral and antiviral host factors in HBV infection的研究论文。该研究验证了核受体共激活因子5(NCOA5)和染色质域解旋酶DNA结合蛋白4(CHD4)为关键的前病毒宿主因子,其敲低显著抑制HBV复制。相反,神经母细胞瘤RAS病毒癌基因同源物(NRAS)被鉴定为抗病毒因子。
机制研究表明,NCOA5可能通过雌激素受体与肝细胞核因子4α(HNF4α)轴发挥作用,而CHD4则调控共价闭合环状DNA(cccDNA)的组蛋白修饰。NRAS敲低通过提升HNF4A表达并诱导细胞周期阻滞,进而增强HBV转录活性。这一发现可能解释在RAS信号频繁过度活化的HBV相关HCC组织中观察到的HBV复制受限现象。
综上,本研究明确了NCOA5与CHD4作为关键的前病毒辅助因子,以及NRAS作为重要抗病毒因子在HBV复制调控中的作用。研究结果不仅揭示了HBV对宿主的高度依赖性,阐明了涉及HNF4A、cccDNA表观遗传调控及细胞周期等具体分子机制,更为针对HBV感染的潜在治疗策略提供了经过验证的宿主靶点。

乙型肝炎病毒(HBV)在全球范围内慢性感染约2.96亿人,并引起一系列肝脏疾病。作为一种致癌病毒,HBV可诱导肝细胞发生基因组及功能改变,从而驱动恶性转化。当前治疗手段仅限于核苷(酸)类似物(NUCs)和干扰素(IFN)。虽然NUCs可抑制病毒复制,但极少实现功能性治愈(即乙型肝炎表面抗原[HBsAg]清除),且需终身治疗。干扰素治疗仅能使3%–8%的患者获得HBsAg清除,同时会引发显著不良反应。因此,HBV相关肝病仍是全球重大健康挑战,亟需开发新型治疗策略。
HBV是一种包膜嗜肝DNA病毒,其3.2 kb的部分双链环状(rc)DNA基因组编码六种蛋白。这种极简编码能力导致其在完整生命周期中需广泛利用宿主因子。病毒入侵需要通过网格蛋白介导的内吞作用与多种宿主受体结合,包括硫酸乙酰肝素蛋白聚糖(如磷脂酰肌醇蛋白聚糖5)、牛磺胆酸钠共转运多肽(NTCP)及表皮生长因子受体(EGFR)。入侵后,衣壳运输涉及Rab5A/Rab7A GTP酶及微管系统,最终实现rcDNA的核输入并通过宿主DNA修复机制转化为共价闭合环状DNA(cccDNA)。
染色质化的cccDNA微型染色体可招募肝细胞核因子4α(HNF4α、HNF4A)、视黄醇X受体α(RXRα、RXRA)、过氧化物酶体增殖物激活受体α(PPARα、PPARA)等肝源性转录因子,并受表观遗传调控以转录病毒RNA。宿主机制将其翻译为e抗原(HBeAg)、HBsAg、核心蛋白(HBc)、聚合酶及X蛋白(HBx)。3.5 kb的前基因组RNA(pgRNA)同时作为翻译与逆转录的模板。成熟核衣壳可循环至核内扩增cccDNA,或在内质网膜处获得包膜。子代病毒粒子通过多泡体途径排出。
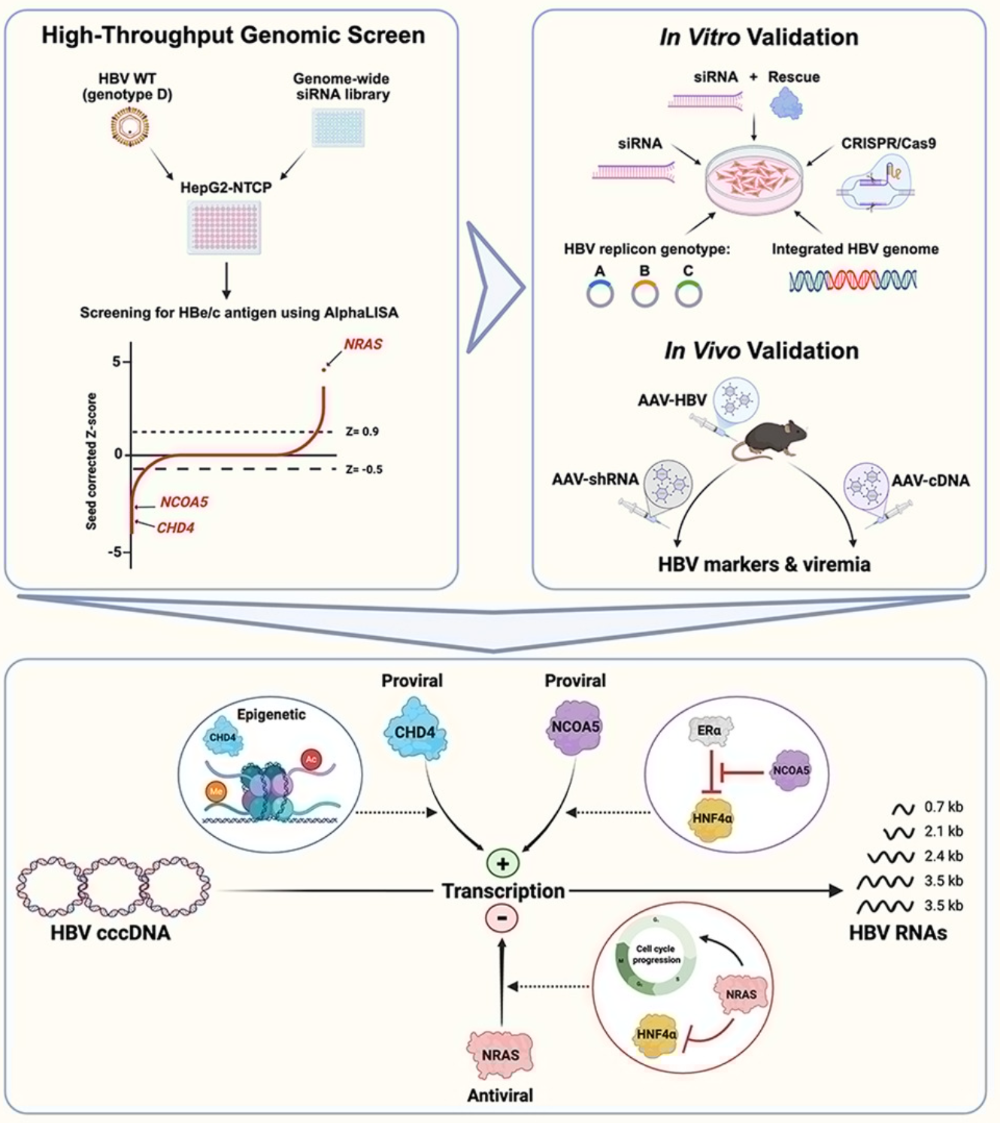
模式机理图(图片源自Journal of Hepatology )
目前对HBV与宿主因子交互作用的全谱认知仍不完整。高通量功能基因组学与HBV受体鉴定的最新进展,使得系统绘制病毒在整个生命周期中与宿主的交互作用图谱成为可能。本研究报道了在HBV感染的HepG2-NTCP细胞中进行的全基因组siRNA筛选,同步评估了病毒抗原表达与细胞活性。该方法鉴定了数千个候选调控因子,其中大多数此前未发现与HBV相关,经后续验证后为HBV-宿主交互作用机制提供了新见解,并可能为治疗策略开发提供新方向。
原文链接:
https://doi.org/10.1016/j.jhep.2025.11.017
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


