Cell:遗传进化和微环境相互作用导致胶质瘤进展
来源:生物谷原创 2022-06-13 11:11
浸润性胶质瘤(infiltrating glioma)是由其遗传进化和微环境决定的,这一发现可能导致更有针对性的治疗。
在一项新的研究中,来自荷兰阿姆斯特丹大学、美国杰克逊基因组医学实验室和哥伦比亚大学医学中心等研究机构的研究人员发现作为一种常见的大脑和脊髓肿瘤,浸润性胶质瘤(infiltrating glioma)是由其遗传进化和微环境决定的,这一发现可能导致更有针对性的治疗。相关研究结果发表在2022年6月9日的Cell期刊上,论文标题为“Glioma progression is shaped by genetic evolution and microenvironment interactions”。
论文共同作者、科罗拉多大学癌症中心成员D.Ryan Ormond博士说,“我们确定了复发时的表观遗传学改变,这些改变不仅在某些病例中具有预后作用,而且可能导致针对不同亚型的不同治疗方案,从而改善长期生存。”
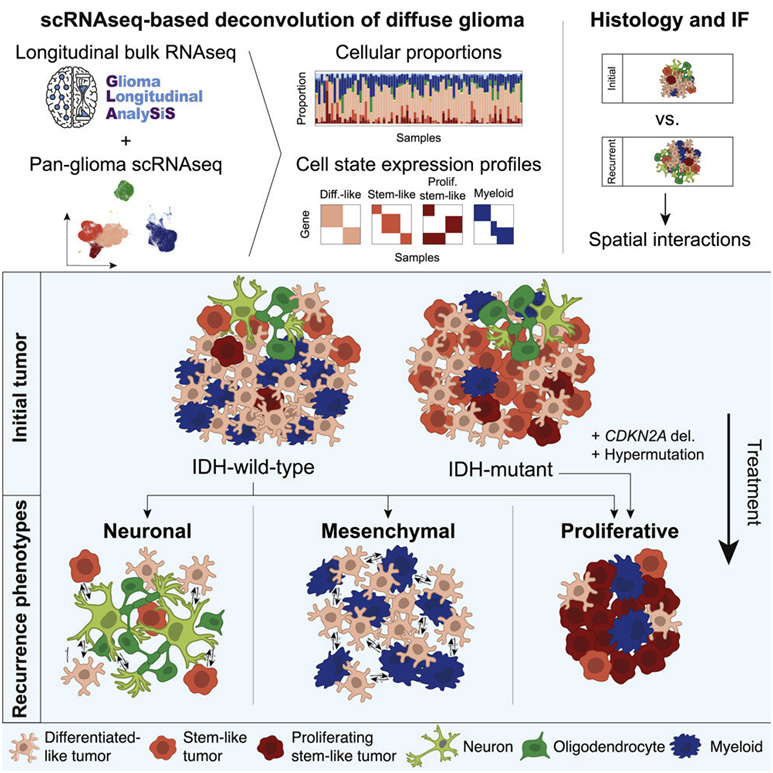
这些作者观察了胶质瘤如何与大脑相互作用,随着时间的推移发生变化,产生治疗抵抗性并变得更具侵袭性。他们确定了胶质瘤复发时的三种不同表型,或者说可观察到的特征---神经元型、间充质型和增殖型。它们中的每一种都细胞、遗传和组织学特征,这些特征在复发时会显现出来。其的一些特征与不太有利的结果有关。
在这项新的研究中,这些作者使用了胶质瘤纵向分析联盟(Glioma Longitudinal Analysis Consortium, GLASS)的参与者样本,该联盟是为了确定胶质瘤治疗抵抗性的驱动因素而成立的。
他们分析了来自304名患有异柠檬酸脱氢酶(IDH)野生型胶质瘤和IDH突变型胶质瘤的成年患者的肿瘤样本的RNA和/或DNA测序数据。肿瘤复发的方式取决于IDH突变状态。它们在复发过程中发生的变化取决于它们与它们所居住的微环境的相互作用方式。
图片来自Cell, 2022, doi:10.1016/j.cell.2022.04.038。
这些作者发现,许多IDH野生型胶质瘤在复发时更具侵入性。他们的肿瘤细胞显示出神经元信号程序的增加,这表明神经元的相互作用在引发这种肿瘤的进展中可能发挥了作用。他们还发现通常由替莫唑胺(temozolomide)等药物治疗诱发的高突变(hypermutation),以及产生肿瘤抑制蛋白的CDKN2A基因的缺失,与这两种胶质瘤亚型复发时肿瘤细胞的增殖有关。
在IDH野生型和IDH突变型胶质瘤中,这种高突变与干细胞样肿瘤细胞(stem-like neoplastic cell)的数量增加有关。这些细胞的生长降低了患者的总体生存率。
这些作者指出,“总的来说,这些结果表明,复发时的遗传进化可以改变胶质瘤细胞,使其朝着与预后不良有关的更多增殖表型发展。”
Ormond说,“治疗抵抗性仍然是胶质瘤患者的一个严重障碍,为了提高生活质量和生存率,需要克服它。”他说,这些发现将使医生能够以新的药物和治疗方法更好地治疗这种癌症。(生物谷 Bioon.com)
参考资料:
Frederick S. Varn et al. Glioma progression is shaped by genetic evolution and microenvironment interactions. Cell, 2022, doi:10.1016/j.cell.2022.04.038.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


