Nat Cancer:癌症真地存在交叉抵抗性,至少对黑色素瘤就是如此
来源:本站原创 2021-07-28 12:16
2021年7月28日讯/生物谷BIOON/---靶向治疗和免疫治疗经常被作为一种组合拳来治疗某些癌症,但有时这种方法并不奏效。在一项新的研究中,来自奥地利、英国、瑞士、美国和澳大利亚的研究人员发现作为免疫治疗期间激活免疫系统的关键细胞,树突细胞在对靶向治疗产生抵抗性的黑色素瘤小鼠模型中,具有较少的活性和较少的数量,这解释了为什么这些肿瘤对免疫治疗不太敏感。刺
2021年7月28日讯/生物谷BIOON/---靶向治疗和免疫治疗经常被作为一种组合拳来治疗某些癌症,但有时这种方法并不奏效。在一项新的研究中,来自奥地利、英国、瑞士、美国和澳大利亚的研究人员发现作为免疫治疗期间激活免疫系统的关键细胞,树突细胞在对靶向治疗产生抵抗性的黑色素瘤小鼠模型中,具有较少的活性和较少的数量,这解释了为什么这些肿瘤对免疫治疗不太敏感。刺激树突细胞可恢复这些肿瘤对免疫疗法的反应。相关研究结果发表在2021年7月的Nature Cancer期刊上,论文标题为“Acquired resistance to anti-MAPK targeted therapy confers an immune-evasive tumor microenvironment and cross-resistance to immunotherapy in melanoma”。论文通讯作者为奥地利维也纳分子病理学研究所研究员Anna Obenauf博士。

美国杜克大学肿瘤内科医生Brent Hanks(未参与这项研究)在发送给《科学家》网站的一封电子邮件中说道,“这项研究为许多黑色素瘤专家在临床上亲身观察到的、最近在回顾性研究中描述的一种现象提供了机理上的新见解:在对[靶向]疗法产生抵抗性之后,对免疫疗法的反应不佳。总的来说,这是对黑色素瘤研究的一个重要贡献,可能对其他癌症的治疗也有影响。”
事实上,正是早期的临床数据引发了Obenauf的兴趣。“这在某种程度上是一个临床难题,因为这两种不同类型的疗法如何能够相互联系,这种对一种疗法的抵抗性导致对另一种疗法的交叉抵抗性(即交叉耐药性)?”靶向治疗阻断了癌细胞内的特定分子通路以阻止增殖,而免疫疗法则通过刺激免疫细胞来根除肿瘤细胞。
Obenauf和她的同事们首先在小鼠模型中重现了这些临床观察。他们利用两种小鼠黑色素瘤细胞系,在小鼠体内建立了肿瘤,并用达拉菲尼(dabrafenib)治疗它们,其中达拉菲尼是一种被批准用于治疗携带BRAF基因突变的黑色素瘤患者的靶向疗法。达拉菲尼通过抑制B-Raf酶来打断MAP激酶(MAPK)通路。虽然这些肿瘤最初对该药物有反应,但癌症最终复发并产生了抵抗性,或者说耐药性。他们从治疗敏感的肿瘤和治疗抵抗性的肿瘤中提取癌细胞,建立了细胞系。这些细胞系再次被注射到小鼠体内,随后用抗PD-1或抗CTL-4免疫检查点抑制剂---旨在解除对免疫系统抑制的免疫疗法---治疗它们。抗PD-1和抗CTL-4免疫检查点抑制剂也被批准用于治疗某些黑色素瘤患者。
利用这种方法,Obenauf团队可以将治疗抵抗性肿瘤植入事先没有接触过靶向疗法的小鼠体内。这使得他们能够评估靶向疗法是否对可能导致免疫疗法抵抗性的免疫细胞有直接影响,或者是否在肿瘤内发生了其他事情。结果发现是后者。Obenauf说,“靶向治疗抵抗性肿瘤确实对免疫检查点抑制剂有交叉抵抗性。”
免疫疗法通常通过促进T细胞反应来发挥作用,因此Obenauf团队更仔细地研究了小鼠的T细胞是如何表现的。虽然T细胞能够在体外杀死治疗抵抗性的肿瘤细胞,但是当他们使用缺乏内源性T细胞的小鼠模型,并加入他们可以用荧光素酶追踪的T细胞时,他们看到T细胞无法渗透到治疗抵抗性的肿瘤中,结果就是肿瘤继续生长。Obenauf回忆说,“这使我们想到了一个问题:肿瘤微环境是否介导抵抗性。”
因此Obenauf团队培育出混合匹配的黑色素瘤小鼠。当他们把治疗抵抗性的肿瘤细胞放在较大的治疗敏感性的肿瘤内时,治疗抵抗性的肿瘤细胞被杀死。Obenauf解释说,似乎治疗敏感性的肿瘤有一种“免疫允许的肿瘤微环境”。相反,当他们将治疗敏感性的肿瘤细胞放在较大的治疗抵抗性肿瘤内时,这些肿瘤细胞存活下来,显然没有受到T细胞介导的杀伤。
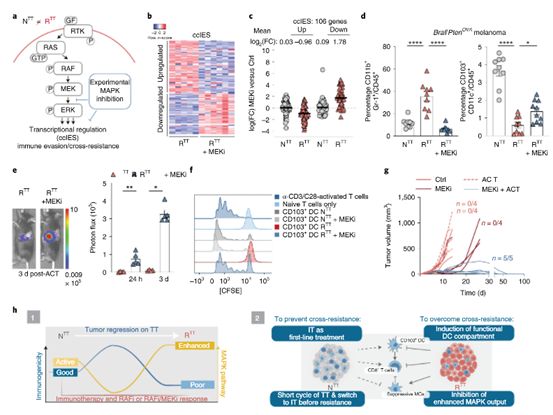
抑制重新激活的MAPK通路可恢复靶向治疗抵抗性肿瘤对免疫治疗的敏感性。图片来自Nature Cancer, 2021, doi:10.1038/s43018-021-00221-9。
RNA测序和流式细胞仪分析显示,作为一种在免疫疗法中激活免疫系统的关键细胞类型,树突细胞在具有治疗抵抗性肿瘤的小鼠中含量较少。当他们将树突细胞与T细胞共同培养时,他们观察到来自治疗抵抗性肿瘤的树突细胞没有激活T细胞,也没有像来自治疗敏感性肿瘤的树突细胞那样刺激它们增殖。Obenauf团队与澳大利亚悉尼大学的一个研究团队合作,从接受靶向治疗的黑色素瘤患者那里获得了活组织样本。一旦患者对这种靶向治疗产生抵抗性,他们体内的肿瘤中的树突细胞就会比以前少。
Hanks解释说,这些结果表明,树突细胞的减少“产生了一种对后续免疫检查点抑制剂免疫疗法反应不佳的免疫破坏性肿瘤微环境”。值得注意的是,这种影响是可逆的。在用实验性免疫刺激剂治疗这些小鼠模型而使树突细胞池成熟和扩大后,这些作者看到更多的T细胞浸润这些小鼠体内的肿瘤,肿瘤因此而缩小。美国莫菲特癌症中心癌症免疫学家Brian Ruffell(未参与这项研究)告诉《科学家》网站,“他们的研究表明,可以通过加入这些树突细胞刺激剂来逆转表型,这是一个很好的原理论证,表明确实是这些细胞受到了限制。”Ruffell补充说,“我认为这项[研究]真正打破了一些生物学上的难题,即为什么要在进入医院和允许治疗抵抗性肿瘤细胞克隆在靶向治疗后产生之前进行免疫治疗。从基础科学的角度来看,我们需要在免疫治疗或免疫系统的背景下研究所有的治疗方法,这确实有助于增加越来越多的这方面的研究。”
为了了解肿瘤细胞如何产生交叉抵抗性,Obenauf及其同事们分析了来自对靶向MAP激酶信号通路的疗法产生了抵抗性的小鼠和患者样本的肿瘤细胞的转录组。过度活跃的MAP激酶通路会导致细胞不受控制的增殖,但会被这种通路的抑制剂所抑制,肿瘤也会随之缩小。当肿瘤复发并对抑制剂产生抵抗性时,MAP激酶通路经常被重新激活。
在他们的样本中,Obenauf团队确定了在靶向治疗抵抗性肿瘤与敏感性肿瘤中存在不同表达的基因的特征。他们通过计算分析来寻找支配这一基因特征的调节因子,发现MAP激酶信号通路在治疗抵抗性肿瘤中再次被激活,明显在促进免疫逃避。 Obenauf说,“令人惊讶的是,[治疗敏感性]和[治疗抵抗性]肿瘤之间的差异被预测为由MAP[激酶]通路导致,这是因为[治疗敏感性]肿瘤虽然存在已经过度活跃的MAPK通路,但是对免疫疗法如此敏感,而[治疗抵抗性]肿瘤因它们的MAPK通路被重新激活,对免疫疗法极具抵抗性。”
事实证明,治疗抵抗性肿瘤中的MAP激酶通路比敏感性肿瘤中的MAP激酶通路更有力地推动了靶基因表达。该通路的组成部分还可以进入新的基因调控位点,这意味着它们可以驱动不同基因的表达。Obenauf说,“MAP激酶通路,也就是对肿瘤起始非常重要的通路,在这种治疗抵抗性过程中被重新连接并增强,从而建立一种非常不同的免疫表型。”
美国汉普顿-悉尼学院生物学家Kristian Hargadon(未参与这项研究)说,“我们可以非常强烈地得出结论,该通路的重新激活是驱动免疫疗法抵抗性的原因。这是人们在此之前不会想到的事情,然而现在这解释了很多以前的观察。”
将所有这些线索拉到一起,这些作者用一种MEK抑制剂治疗具有靶向治疗抵抗性的肿瘤的小鼠,其中与最初的靶向治疗抑制剂不同的是,MEK抑制剂在不同的节点上抑制MAP激酶通路。在体外,这种抑制作用使80%的形成这种治疗抵抗性特征的基因的表达恢复到对治疗敏感的表达特征。当对具有治疗抵抗性的肿瘤的小鼠给予MEK抑制剂时,树突细胞变得更多和更活跃,从而诱导T细胞增殖。当他们对这些小鼠进行免疫治疗时,T细胞能够控制住肿瘤,而且它们可以存活更长时间。Obenauf说,“效果非常显著,表明MAP激酶通路与树突细胞一起确实负责介导交叉抵抗性。”
Hargadon总结道,“这是一项非常优雅、复杂、深入的研究。研究了几种不同的肿瘤模型,评估了几种不同的治疗方案,所有这些都指向了同一现象。”(生物谷 Bioon.com)
参考资料:
Lisa Haas et al. Acquired resistance to anti-MAPK targeted therapy confers an immune-evasive tumor microenvironment and cross-resistance to immunotherapy in melanoma. Nature Cancer, 2021, doi:10.1038/s43018-021-00221-9.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


