《自然》:科学家首次在体内破解上皮-间质转化促进癌症对化疗耐药的机制!
来源:奇点糕 2023-04-14 13:46
这一研究发现,RHOJ在EMT相关肿瘤化疗耐药方面发挥着重要的作用,靶向RHOJ以及核内肌动蛋白纤维重塑的疗法可能具有一定的治疗潜力。
干细胞和间质细胞拥有分化成不同细胞的魔法,而通常情况下,「平民」上皮细胞,就不具备这种超能力。
但在有些情况下,上皮细胞也会获得这种超级魔法,「返祖」重获多能性。比如,在伤口愈合过程中,部分上皮细胞就会通过上皮-间质转化(EMT)过程,成为间质细胞。这些间质细胞具有高度的迁移和增殖能力,能够向伤口方向迁移,分化成不同的细胞,填补受损组织缺陷。
这种超炫的魔法,癌细胞一定不会错过。毕竟,绝大部分的实体瘤都是上皮细胞来源的。事实上,大量的研究发现,肿瘤组织中存在大量的EMT过程,EMT可以使癌细胞具有更强的迁移和侵袭能力,从而促进肿瘤的形成和转移【1】。同时,EMT还可以使肿瘤细胞从肿瘤组织中脱落,进入循环系统并定居到远处的器官,从而形成转移瘤。魔法就此变成了魔咒。
在这个过程中,肿瘤的代谢和转录特性也会发生显著的变化。许多研究表明,这种由EMT驱动的重编程可以促进肿瘤的耐药。
那么,EMT促进癌症耐药的具体机制究竟是什么呢?以往的一些研究,已经提出了几种机制,来解释体外癌细胞系中与EMT相关的治疗抗性【2】。但这些机制还没有在体内原发性肿瘤中获得验证。
近期,由比利时布鲁塞尔自由大学领衔的一项研究,发表在了顶级期刊《自然》上,首次通过体内研究揭示了EMT促进癌症对化疗耐药的机制。

论文首页截图
研究发现,一种叫RHOJ的酶在EMT相关化疗耐药中发挥着重要的作用。这种酶可以使受损的癌细胞获得强大的DNA修复能力,必要时还会启动「休眠起源」这个备胎,来促进DNA的复制,从而在化疗的围剿中死里逃生。简单点说,RHOJ就像一个DNA快修公司的领导,组织各种资源,拯救受损的DNA【3】。
在这项研究中,研究人员首先使用顺铂和5-氟尿嘧啶两种化疗药物,治疗经基因工程诱发皮肤鳞状细胞癌(SCC)的小鼠。这种药物组合目前是晚期皮肤癌的标准化疗方法,其作用机制是诱导癌细胞的DNA损伤。
研究发现,约14%的SCC对化疗非常敏感,在治疗4周后实现完全应答;大多数SCC(54%)为部分应答,此外,还有约32%完全没有应答。进一步研究发现,没有应答的肿瘤里富集了EMT肿瘤细胞,占比达到70%。看来EMT的确和肿瘤的抗药性有重要的关联。
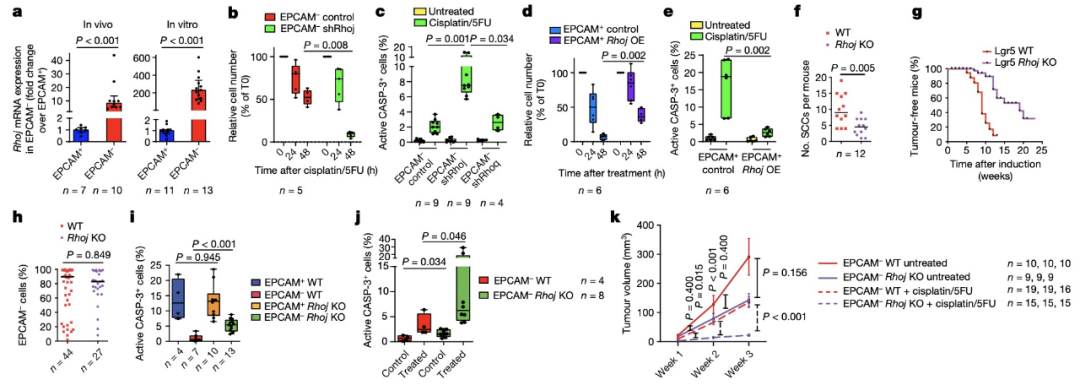
不同SCC对化疗的应答情况,以及EMT与应答的关联
随后的体外研究发现,EMT肿瘤细胞在没有肿瘤微环境的情况下也对化疗具有显著的抵抗力。这说明这股抵抗的势力并不依赖于肿瘤微环境。
继续深挖之后,科学家发现,EMT肿瘤细胞表达了较高水平的凋亡抑制因子以及与谷胱甘肽代谢相关的基因。更重要的发现是,有一种叫RHOJ的小GTP酶,在EMT肿瘤细胞中高度表达。
当然,RHOJ对于科学家来说也不算陌生,此前的研究就发现,RHOJ在黑色素瘤中就可以介导治疗抵抗。
为了进一步研究RHOJ是否在SCC中也介导了EMT相关的治疗抗性,研究人员采用了经典的功能丧失/增益方法。结果发现,Rhoj敲低后,EMT肿瘤细胞在顺铂/5-氟尿嘧啶处理后凋亡增加,化疗48小时后活细胞数量也显著减少。但在没有经过EMT过程的肿瘤细胞中,Rhoj敲低并没有改变它们对化疗的反应。
看来在EMT肿瘤细胞中,RHOJ的确具有大法护体的功效。
接下来,研究人员评估了RHOJ过表达是否能使上皮肿瘤细胞对化疗产生抵抗。结果表明,RHOJ在没有经过EMT的肿瘤细胞中过表达,显著降低了顺铂/5FU处理24小时后的凋亡细胞比例。
其次,为了确定RHOJ是否在体内也能介导EMT对治疗的抵抗,研究人员使用了Rhoj条件性敲除小鼠肿瘤模型。Rhoj基因缺失后,EMT与未EMT的肿瘤细胞比例没有变化,说明RHOJ本身并不控制EMT。
给小鼠注射顺铂/5FU化疗后,Rhoj敲除的EMT肿瘤细胞死亡率增加。进一步研究发现,Rhoj基因缺失后,肿瘤对化疗的短期和长期敏感性均有所提高。那么,RHOJ具体是通过什么方法给肿瘤加上金钟罩的呢?
研究人员继续挖掘发现,EMT肿瘤细胞和未EMT细胞相比,DNA复制(POLD,PCNA)和修复(pRPA2)以及肌动蛋白骨架(N-WASP)相关蛋白具有较高的表达;而在Rhoj敲除的细胞中,观察到了这些蛋白的下调。据此推测,RHOJ可能是通过影响DNA修复以及肌动蛋白骨架相关蛋白来提高肿瘤抗药性的。
接下来的研究结果,就得让大家直呼RHOJ「大拿」了!研究发现,RHOJ对DNA损伤修复的调节,不是通过特定的DNA修复途径,而是控制不同DNA损伤应答(DDR)途径和抵抗复制应激机制共享的通用机制。蛋白质组学分析显示,RHOJ可以调节许多促进DNA复制和DNA修复的蛋白质的表达。
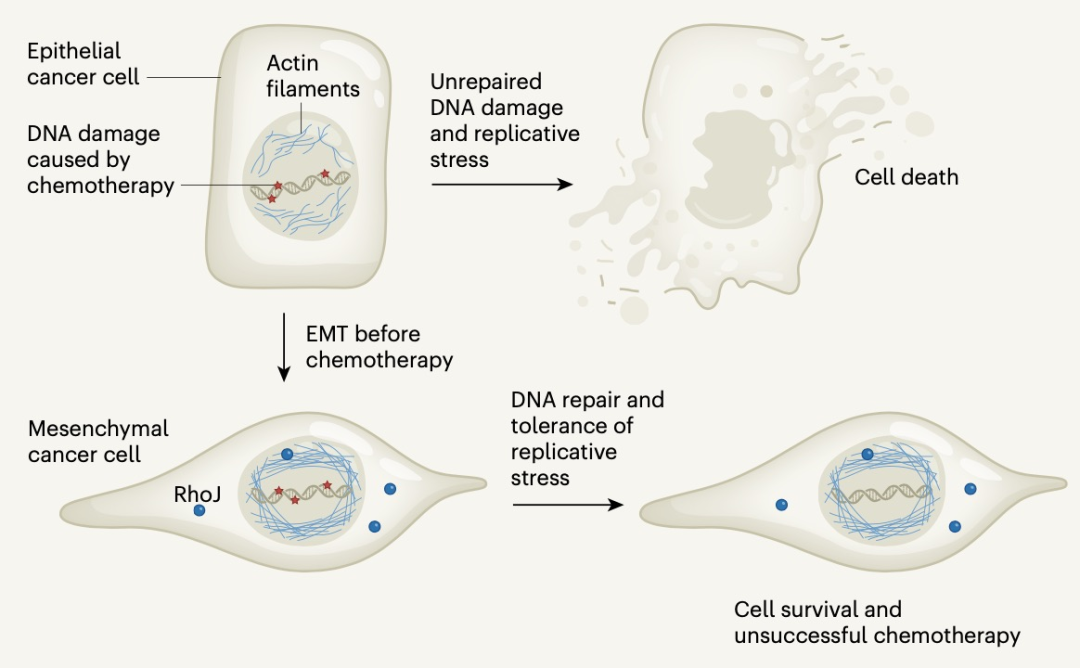
一图看懂RHOJ整体的调控作用
同时,RHOJ还可以激活DNA复制的「休眠起源」。「休眠起源」是DNA复制的备用起始点,当DNA复制因各种原因受阻时,有助于确保成功复制。
到这里,大家可能要问,RHOJ发挥这些神功的媒介是什么呢?以往的研究显示,RHOJ可以控制肌动蛋白纤维的动态重组(改变聚合的形态),那么肿瘤的化疗抗性和肌动蛋白纤维重塑之间有没有关联呢?
其实,以往大量研究已经暗示,核内肌动蛋白纤维在指导DNA修复动态中发挥一定的作用。而在这项研究中,科学家也发现,RHOJ介导的DNA修复和复制应激耐受,的确依赖于RHOJ诱导核内肌动蛋白纤维重塑的能力。但这一过程究竟是如何实现的,目前还没有定论。
总之,这一研究发现,RHOJ在EMT相关肿瘤化疗耐药方面发挥着重要的作用,靶向RHOJ以及核内肌动蛋白纤维重塑的疗法可能具有一定的治疗潜力。
参考文献:
【1】Yang, Jing, et al. "Guidelines and definitions for research on epithelial–mesenchymal transition." Nature reviews Molecular cell biology 21.6 (2020): 341-352.
【2】De Las Rivas, Javier, et al. "Cancer drug resistance induced by EMT: Novel therapeutic strategies." Archives of toxicology 95.7 (2021): 2279-2297.
【3】Debaugnies, M., Rodríguez-Acebes, S., Blondeau, J. et al. RHOJ controls EMT-associated resistance to chemotherapy. Nature (2023).
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


