《细胞》:给T细胞充能!科学家开发给T细胞输送线粒体的方法,“满电”T细胞抗肿瘤免疫能力更强、更不易耗竭
来源:代丝雨 2024-10-08 09:09
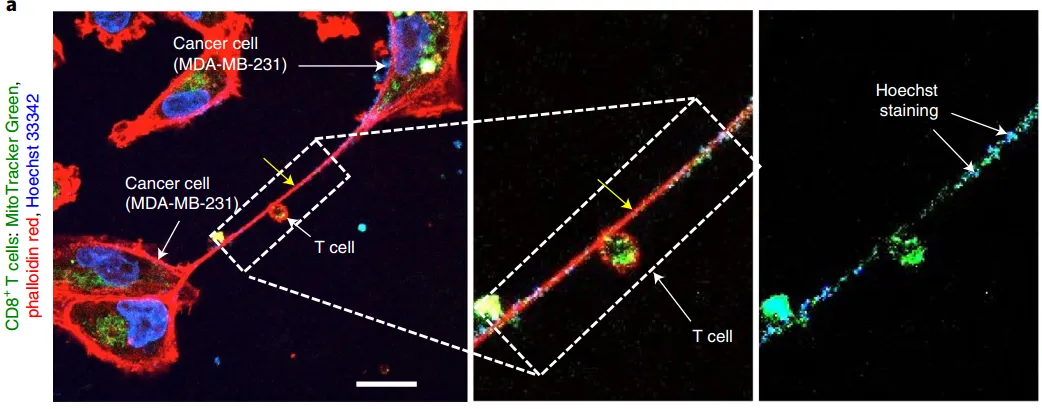
研究者们发现,骨髓基质细胞(BMSC)可以与CD8+T细胞建立纳米管连接,为T细胞输送线粒体。
《自然·纳米技术》发表的一篇论文发现,癌细胞竟然会通过细胞间的纳米管“偷走”免疫细胞的线粒体,一手加强自己、一手削弱免疫。
右一为转移中的线粒体
这手儿可太狠了,癌细胞空手套白狼,生意做得无本万利,外国学者都在评论里打下四个中文大字儿——“釜底抽薪”!

感慨癌细胞狠辣之余,咱们也得为T细胞发声,就没有人,能够救救T细胞吗?
3年后的今天,同一科研团队在《细胞》杂志发文,研究者们发现,骨髓基质细胞(BMSC)可以与CD8+T细胞建立纳米管连接,为T细胞输送线粒体。
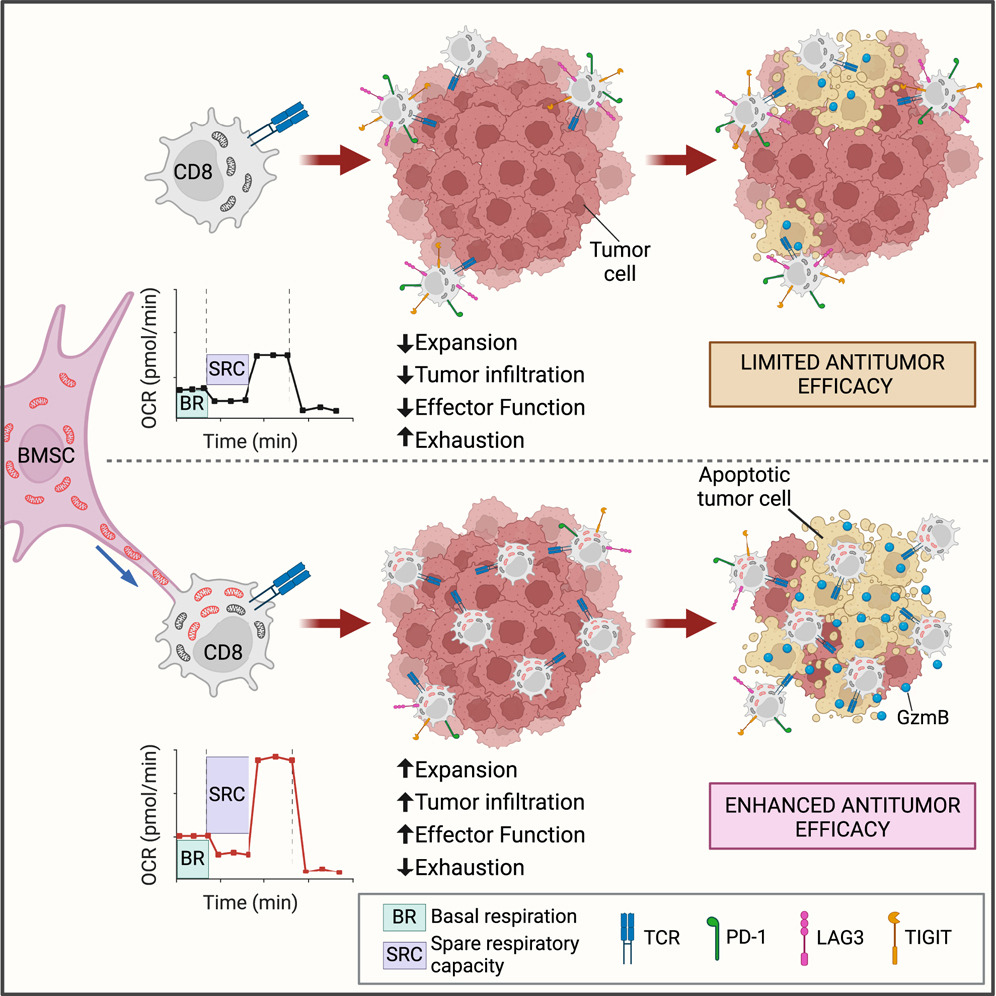
获得了外援线粒体超级充能(supercharging)的T细胞,能源大足、精神大振,在肿瘤微环境中表现出了更稳定的增殖特性和浸润效率,也更不容易耗竭。研究者认为,这一充能思路可以为强化CAR-T等细胞疗法提供新的方案。
不知道这次有没有老外秀中文,我看这招可以叫做“师夷长技以制夷”!
论文题图
肿瘤之难对付,很多时候来自严苛的肿瘤微环境。对T细胞等免疫细胞来说,肿瘤微环境可真不是个适合生存的地方,有各种不利因素会造成线粒体受损、并导致T细胞耗竭。而线粒体本身也比较脆弱,线粒体DNA相较核DNA更容易积累损伤,其功能也更容易受到年龄和各种治疗因素的影响。
缺乏了关键的能量工厂线粒体,也怪不得T细胞干不好活儿。
那么我们是否有方法可以给T细胞重新充能呢?谁又能当好这个超级充电桩?
研究者想到的是骨髓基质细胞(BMSC)。以前就有研究发现,BMSC能够调节T细胞功能和分化,研究者猜想,从二者的相互作用中,我们或许可以找到一些端倪。
研究者将人或小鼠的BMSC和匹配的CD8+T细胞共培养24小时后,固定细胞用场发射扫描电子显微镜(FESEM)检查。对的,2021年的研究他们也是用的这个超级高清的显微镜。
显微镜下,研究者们观察到,BMSC和T细胞之间果然存在复杂的纳米管桥接结构,平均每个细胞都有1个。考虑到固定细胞时对超细结构的破坏,研究者认为实际的纳米管数量应该更多。
有趣的是,纳米管的平均宽度仅有不足1μm(小鼠)和2μm(人类),但在其中可以观察到部分膨大的结构,好像有什么东西裹在里面。
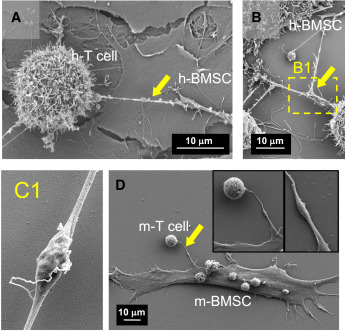
纳米管中可观察到膨大的结构
使用荧光蛋白标记线粒体,果然,这段膨大部分裹的就是正从BMSC运往T细胞的线粒体。
获得能量补给的T细胞显然变得更强了。
研究者首先检测了T细胞的有氧呼吸水平,发现获得线粒体补给后,T细胞的代谢能力变得更强了,代谢活性显著增加。
这显著增加了CD8+T细胞的抗肿瘤免疫能力。研究者将T细胞转移到黑色素瘤B16荷瘤小鼠体内,发现充过能的T细胞(Mito细胞)具有更强的抗肿瘤效应,小鼠的生存期显著延长。
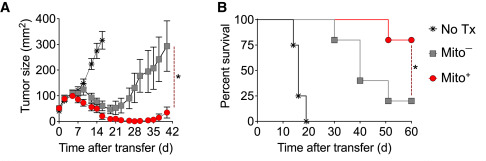
Mito细胞有更强的抗肿瘤作用
Mito细胞也更不容易被肿瘤微环境打败,在转移7天后,Mito细胞仍然能够保持较高的代谢优势,代谢特征没有显著改变。
在转移完成1个月后,研究者分析了Mito细胞扩增的子代细胞,发现来自BMSC的线粒体可以通过重复分裂传递给子代,而且子代细胞的线粒体含量仍旧保持着较高的水平,说明这一超级充能策略有效期还挺长的。
什么叫充电五分钟,通话一小时啊。
最后,研究者在CD19-CAR-T细胞中测试了超级充能的效果。从图中可以看出,在针对NALM6-GL白血病细胞的全6轮测试中,Mito细胞直到最后一轮都保持着强大的杀伤力,而没充电的T细胞(Mito-)第三轮开始就有点不行了。
在荷瘤小鼠中进行的实验也观察到了类似的结果。
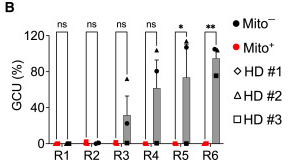
超级充能T细胞针对NALM6-GL白血病细胞的杀伤力测试
实验中,研究者们采用的充电方法是将T细胞与BMSC共培养。研究者们发现,要有效地转移线粒体,需要供体受体细胞都表达一种细胞骨架蛋白Talin2,或许这能够帮助研究者们设计出更有靶向性、更高效率的充电方案。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


