内皮细胞miR-22的抑制介导非小细胞肺癌细胞诱导的血管生成
来源:本站原创 2021-11-18 14:15
在内皮细胞(ECs)中表达的microrna (mirna)是强大的血管生成调控因子,而血管生成是肿瘤生长和转移的关键。
在内皮细胞(ECs)中表达的microrna (mirna)是强大的血管生成调控因子,而血管生成是肿瘤生长和转移的关键。在这里,作者证明了miR-22在ECs中优先和高表达,而与匹配的非肿瘤肺组织相比,其内皮水平在人类非小细胞肺癌(NSCLC)组织中显著下调。这种内皮 miR-22 的减少可能是由 NSCLC 细胞分泌的白细胞介素-1b 和随后激活的转录因子核因子-kB 诱导的。
内皮细胞miR-22作为一种有效的血管生成抑制剂,通过直接靶向ECs中的sirtuin 1和成纤维细胞生长因子受体1,抑制所有关键的血管生成活性,从而抑制NSCLC的生长,导致AKT/哺乳动物雷帕霉素信号靶点的失活。这些发现为了解非小细胞肺癌血管生成的分子机制提供了思路,并表明内皮细胞miR-22是未来非小细胞肺癌抗血管生成治疗的潜在靶点。
图片来源:https://doi.org/10.1016/j.omtn.2021.10.003
血管生成,即从已有的血管形成新的血管,是肿瘤生长和转移的必要条件。因此,过度的血管生成是不同类型癌症侵袭性的不良预后指标,如非小细胞肺癌(NSCLC)。肿瘤血管生成受促血管生成因子和抗血管生成因子之间的平衡密切调控,这涉及到肿瘤细胞与内皮细胞之间的动态通信。
肿瘤细胞能够释放不同的促血管生成因子,如血管内皮生长因子(VEGF)、碱性成纤维细胞生长因子(bFGF, FGF2)、表皮生长因子(EGF)、肿瘤坏死因子(TNF)-a、白细胞介素(IL)-1b、IL-6和IL-8。这些因子与位于ECs上的受体结合可激活关键的下游血管生成相关信号通路,如磷酸肌醇3激酶(PI3K)/v-akt鼠胸腺瘤病毒癌基因同源物(AKT)/雷帕霉素靶蛋白(mTOR)信号通路。因此,内皮细胞被刺激降解其基底膜、增殖、向肿瘤细胞迁移并相互连接以形成新的微血管网络。
既往研究表明,sirtuin (SIRT) 1在调控血管生成中起着至关重要的作用。SIRT1是烟酰胺腺嘌呤二核苷酸依赖性III类组蛋白去乙酰化酶sirtuin家族的原型成员。SIRT1的缺失导致EC发芽和分枝活性的显著降低。此外,内皮细胞SIRT1缺失会损害缺血后肢和肾脏内的血管生成。
SIRT1的促血管生成作用很可能是由它的一些底物介导的。事实上,有报道称SIRT1使AKT脱乙酰,AKT与磷脂酰肌醇(3,4,5)-三磷酸结合,导致AKT/mTOR通路的激活。此外,SIRT1还能使forkhead转录因子FOXO1去乙酰化,从而抑制其抗血管生成活性。SIRT1还可以通过上调雷帕霉素复合物2的机制靶点Rictor的转录来促进AKT的磷酸化。
MicroRNAs (miRNAs)是短的,内源性非编码RNA(~22核苷酸),主要通过结合信使RNA
(mRNA)的3’非翻译区(UTR)来调节基因表达,导致mRNA降解和翻译抑制。在过去的十年中,越来越多的证据表明,microrna是血管生成的强大调节因子。此外,miRNA 失调与肿瘤的发展和进展有关。有趣的是,miR-22在不同体液和肿瘤组织中的表达变化被认为对NSCLC等多种癌症的诊断、监测和预后具有重要意义。miR-22,又称miR-22-3p,位于染色体17p13上,在后生动物中高度保守。据报道,它在不同类型的ECs中表达。然而,其在调节肿瘤血管生成中的作用尚不明确。
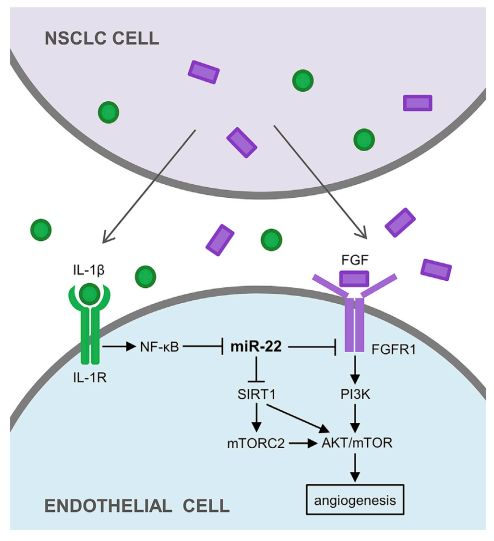
NSCLC 细胞通过下调靶向
SIRT1 和 FGFR1 的内皮 miR-22 来刺激血管生成。
图片来源:https://doi.org/10.1016/j.omtn.2021.10.003
在本研究中,作者分析了NSCLC细胞对内皮细胞miR-22的调控。然后,作者系统地研究了miR-22在基础血管生成过程中的作用,包括EC增殖、迁移和管形成。miR-22的抗血管生成作用在小鼠主动脉环实验和体内Matrigel堵塞实验中得到进一步证实。此外,作者在小鼠侧翼肿瘤模型中研究了内皮细胞miR-22对NSCLC血管生成和生长的影响。最后,机制分析确定SIRT1和FGF受体(FGFR)1是miR-22在ECs中的功能靶点。(生物谷 Bioon.com)
参考文献
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。




