2022 ASH:血液瘤新进展:4家巨头,10款双抗
来源:医药魔方 2022-11-25 12:00
2022年,似乎可以被称为双特异性抗体(双抗)药物的“爆发之年”,4款新产品在全球获批上市,直接超过了历年上市的双抗药物总和。康方生物卡度尼利单抗(CTLA-4/PD-1)的获
2022年,似乎可以被称为双特异性抗体(双抗)药物的“爆发之年”,4款新产品在全球获批上市,直接超过了历年上市的双抗药物总和。康方生物卡度尼利单抗(CTLA-4/PD-1)的获批诞生了首个中国本土双抗药物,罗氏2款双抗产品的相继上市也拉开了巨头药企在这一领域的新进展序幕。
2022年12月,在第64届美国血液学会年会 (2022 ASH)上,罗氏、强生、艾伯维和辉瑞将分别在多发性骨髓瘤(MM)、滤泡性淋巴瘤(FL)和弥漫性大B细胞淋巴瘤(DLBCL)等血液瘤领域公布多项双抗产品的临床数据和研究进展。
FL and DLBCL:罗氏率先进场,艾伯维紧随其后
2022年6月,罗氏CD20/CD3双抗mosunetuzumab(Lunsumio)获批用于治疗3线及以上复发难治滤泡性淋巴瘤,成为该疾病领域的首个双抗药物。Glofitamab紧随其后,凭借II期NP30179的扩展研究数据提交了治疗复发或难治性 (R/R) 弥漫性大B细胞淋巴瘤的上市申请。
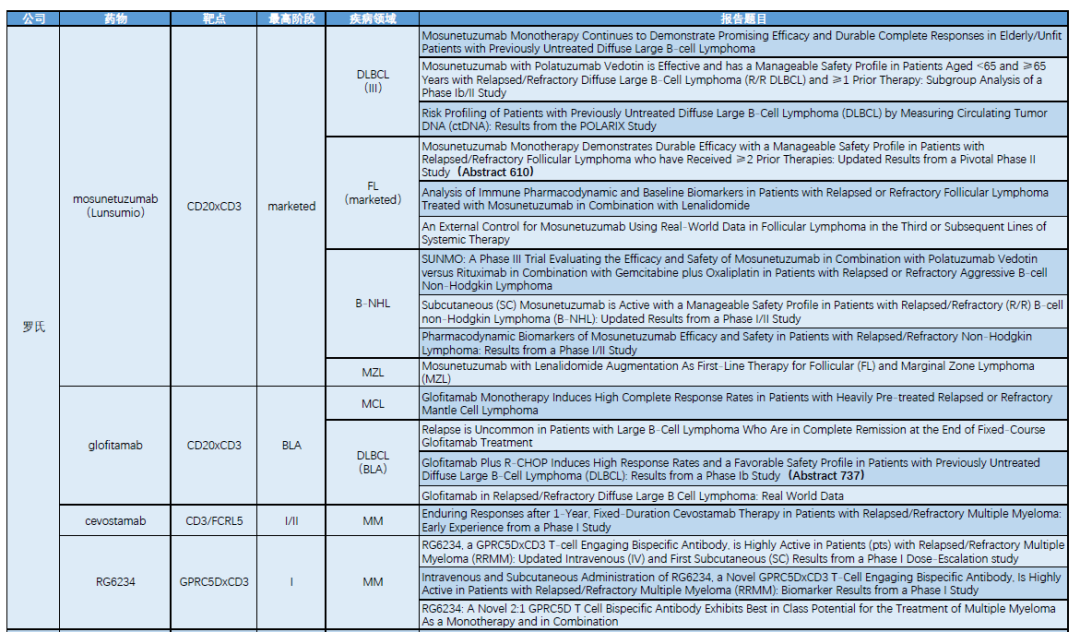
罗氏双抗产品的部分ASH报告题目
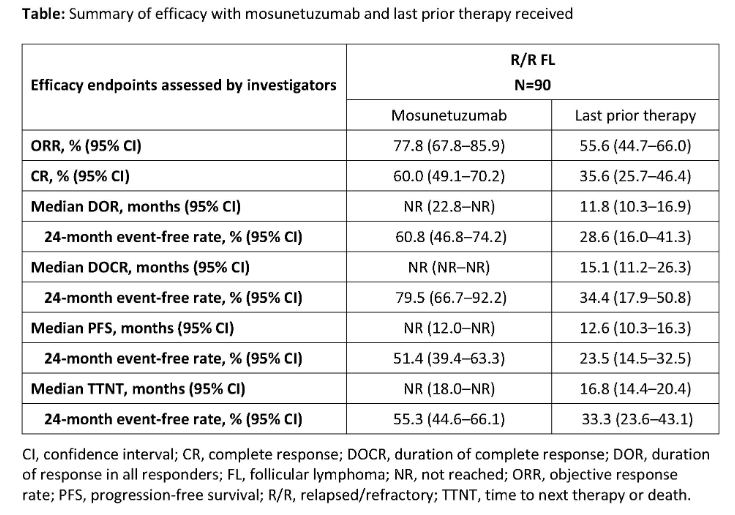
Mosunetuzumab将在本届会议上公布复发难治FL的更新数据(Abstract 610)。结果显示,在所有90例患者中,研究者 (INV) 评估的ORR和CR率分别为77.8%和60.0%,尚未达到中位缓解持续时间(DOR)、中位无进展生存期 (mPFS)和完全缓解持续时间(DOCR)。根据Kaplan-Meier估计,79.5%的完全缓解者至少在24个月内保持缓解状态,研究者评估的24个月PFS率为51.4%。
在DLBCL领域,罗氏的Glofitamab也开展了一线疗法的布局(Abstract 737)。在中位5.6个月的随访期内,56例患者中46例可评估疗效,CR率为76.1%,ORR为93.5%,1-2级细胞因子释放综合症(CRS)为10.7%。此前公布的复发或难治性DLBCL研究(NP30179),中位随访12.6个月后,独立审查委员会评估的CR为39.4% (n=61/155,主要疗效终点),其中一半(51.6%;n=80/155)达到总体反应的次要疗效终点。
然而,即使罗氏在CD20/CD3双抗赛道布局了2款产品,恐怕也难在这两项血液瘤领域独占鳌头。毕竟,艾伯维和Genmab已经分别向EMA和FDA提交了CD20xCD3双抗epcoritamab针对复发/难治性弥漫性大B细胞淋巴瘤(DLBCL)和大B细胞淋巴瘤 (LBCL)的上市申请,而滤泡型淋巴瘤也已经处于临床后期,或将与罗氏率先展开竞争。
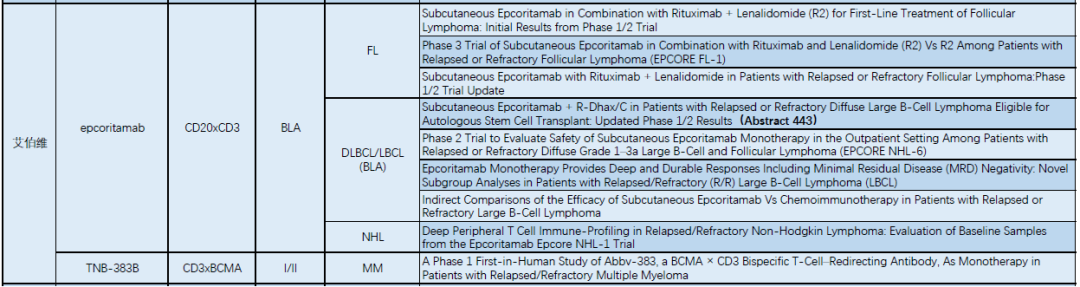
艾伯维双抗产品的部分ASH报告题目
Epcoritamab联合R-DHAX/C(利妥昔单抗/地塞米松/阿糖胞苷/卡铂)治疗复发难治适合移植的DLBCL数据在ASCO之后再次更新(Abstract 443),29例患者中ORR为100%、CR实现80%,虽然患者基数略少但也是不俗的表现。而在FL领域,epcoritamab同样开展了后线和前线治疗资格的双布局。
当然,罗氏和艾伯维也不会孤单,再生元的CD20xCD3双抗odronextamab将公布注册性II期ELM-2研究数据(Abstract 444,949)。在121例≥3线的DLBCL患者,90例符合有效性分析,随访17.1个月时ORR和CR分别为53%和37%,而且疗效持久性较好,9个月时持续CR率为73%。同样,在96例3线及以上FL患者中,85例患者评估的ORR和CR分别为81%和75%,两项研究结果也是被SVB证券的分析师认为均具有“竞争力”。

再生元双抗产品的部分ASH报告题目
强生在CD20xCD3赛道也不甘寂寞,虽plamotamab的开发速度有所落后,但在血液瘤领域却有着独特优势。
MM:强生壁垒高筑,辉瑞执剑入局
强生在多发性骨髓瘤(MM)领域可谓“老谋深算”、壁垒深厚,不仅拥用老牌的多发性骨髓瘤药物硼替佐米和达雷妥尤单抗两款成功的血液肿瘤产品,如今还手握着明星BCMA CAR T产品西达基奥仑赛,而近期获批上市的CD3xBCMA双抗teclistamab(Tecvayli)再次拉高了强生的领域壁垒。
推荐阅读:在BCMA靶点上,强生是如何深远布局的?
在本届ASH会议上,强生将继续公布teclistamab多项临床数据,包括上市研究的相关分析(MajesTEC‑1,Abstract 97)和新诊断患者的研究进展(Abstract 3242,4558)等。
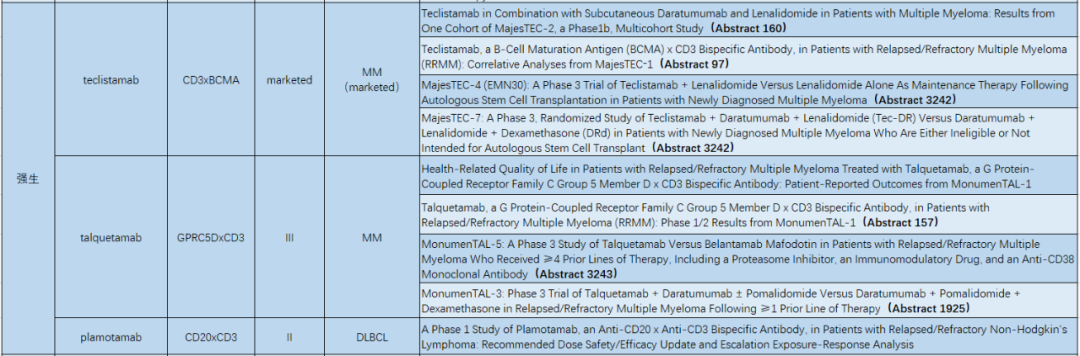
强生双抗产品的部分ASH报告题目
MajesTEC-1考察的是teclistamab在先前接受过≥3线治疗的复发/难治性多发性骨髓瘤 (RRMM) 患者中的安全性/有效性,MajesTEC-2则是将患者群拉到了接受过包括蛋白酶体抑制剂和免疫调节药物的1-3 线治疗 (LOT)上,MajesTEC-7和MajesTEC-4更进一步,直接到了新诊断患者群体。不难看出,teclistamab一款产品,让强生又完成了一项MM全疾病进程的治疗布局。
BCMA在MM领域是明星和热门靶点,辉瑞、再生元和BMS等也有CD3/BCMA双抗药物的临床数据披露,其中辉瑞的开发速度更为迅速。Elranatamab (PF-06863135) 是辉瑞开发的一种皮下双特异性抗体,靶向BCMA和T细胞上的CD3,可激活和重定向T细胞介导的针对MM的免疫反应。

辉瑞双抗产品的部分ASH报告题目
55例既往治疗方案的中位数为5的患者接受单药elranatamab SC,推荐剂量(1000µg/kg或76mg)的CRS总发生率为67%,仅限于1级 (33%) 或2级(33%),没有3级或更高级别的事件。中位随访12.0个月(范围 0.3-29.0),根据国际骨髓瘤工作组(IMWG)确认的客观反应率 (ORR) 为 64%,56%的患者达到非常好的部分缓解 (VGPR) 或更好,38%的患者(21/55)达到完全缓解(CR)或更好。即使之前接受过BCMA靶向治疗(抗体药物偶联物、嵌合抗原受体T细胞治疗或两者)的13名患者中,也获得54% (7/13) 的缓解,其中46% (6/13)获得了VGPR或更好,初步证明了elranatamab仍具备了抢夺BCMA靶向疗法治疗后患者的潜力。
而在MM领域,强生还有一款更受关注的GPRC5DxCD3双抗talquetamab,目前已经进展至临床III期。采取0.4 mg/kg QW治疗的143名患者中,ORR为73%(≥VGPR:58%;≥CR:29%),且随着时间的推移,反应持久并加深。中位反应时间为1.2 个月,达到CR的中位时间为2.1个月,中位DOR为9.3个月,中位PFS为7.5 个月。难得的是三类药物难治性 (72% [76/106]) 和五类药物难治性 (71% [30/42]) 患者的ORR与总人群相当,而0.8 mg/kg Q2W的疗效将在会议上公布。
可以说,罗氏和强生在多发性骨髓瘤(MM)、滤泡性淋巴瘤(FL)和弥漫性大B细胞淋巴瘤(DLBCL)等血液瘤领域存在一定的竞争优势,包括利妥昔单抗和硼替佐米等非专利药物打造的渠道优势和品牌,以及专利药达雷妥尤单抗、CAR T产品、维泊妥珠单抗等药物的继续渗透。
随着4家巨头双抗产品在血液瘤领域中的相继触线,新一轮的竞逐或将开幕。对于MM、FL和DLBCL并不是传统优势领域的艾伯维和辉瑞而言,能否执剑双抗杀入新的领域,我们拭目以待。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


