Cell子刊:孙洁/钱鹏旭/裴善赡/黄河团队开发CRISPR基因编辑增强的CAR-T细胞疗法,治疗急性髓系白血病
来源:生物世界 2025-05-30 17:00
这项研究支持 CD97 作为急性髓系白血病(AML)的 CAR-T 细胞疗法的一个有前景的靶点。
急性髓系白血病(AML)是成年人中常见的急性白血病,其特征是未成熟的髓系细胞分化受阻和异常增殖,导致造血功能紊乱和危及生命的血细胞减少症。AML 的发病率往往随着年龄的增长而逐渐上升,同时总体生存率则下降。例如,超过三分之二的 AML 诊断在 55 岁以上,与此同时,65 岁以下患者的总体生存率约为 40%-45%,而 65 岁以上患者仅为 10%-15%。此外,超过半数的 AML 患者在一年内病情复发,实现持久缓解的成年患者不到三分之一。急性髓系白血病(AML)原始细胞的固有异质性,再加上白血病干细胞(LSC)对化疗的耐药性,给 AML 的有效治疗带来了巨大障碍。
CAR-T 细胞疗法在治疗难治性或复发性 B 细胞恶性肿瘤及多发性骨髓瘤方面取得了显著成功。然而,其在急性髓系白血病(AML)患者中的疗效未达预期,一个主要挑战是在于缺乏像 B 细胞中 CD19 这样的靶点。AML 原始细胞和白血病干细胞(LSC)上表达的大多数抗原也在正常细胞中表达,尤其是造血干细胞(HSC),因此,以这些抗原为靶点的 CAR-T 细胞疗法会对正常造血功能产生脱靶毒性,从而导致粒细胞减少症、贫血、血小板减少症等。
2025 年 5 月 26 日,浙江大学医学院附属第一医院孙洁、钱鹏旭、裴善赡、黄河团队合作,在 Cell 子刊 Cell Reports Medicine 上发表了题为:CD97-directed CAR-T cells with enhanced persistence eradicate acute myeloid leukemia in diverse xenograft models 的研究论文。
该研究表明,CD97 是 CAR-T 细胞治疗急性髓系白血病(AML)的理想靶点,使用 CRISPR-Cas9 敲除 T 细胞中的 CD97,并将 CD97 CAR 定向插入 TRAC 位点,由此构建的 CAR-T 细胞能够避免自相残杀,增强持久效果,在多种异种移植肿瘤小鼠模型中根除急性髓系白血病。

CD97 由 ADGRE5 基因编码,属于黏附性 G 蛋白偶联受体(aGPCR)家族。大量研究显示,CD97 发挥着促进多种癌细胞侵袭的作用,包括结直肠癌、甲状腺癌、肝癌、胃癌、脑癌和前列腺癌等。
与正常骨髓细胞相比,原发性 AML 细胞和白血病干细胞中 CD97 的表达水平升高。值得注意的是,CD97 在造血干细胞中的表达水平极低。此外,AML 中 CD97 的高表达与不良预后相关。CD97 在 AML 原始细胞和白血病干细胞的增殖和存活中发挥着关键作用,维持其未分化状态。所有这些证据都表明,CD97 可能是治疗急性髓系白血病(AML)的一个合适靶点。
然而,T 细胞上也表达 CD97,这就导致 CD97 靶向的 CAR-T 细胞不仅会杀伤癌细胞,也会自相残杀。
为了让解决 T 细胞表达 CD97 导致自相残杀的问题,研究团队利用 CRISPR-Cas9 基因编辑技术敲除了 CAR-T 细胞中的 CD97,同时将 CD97 CAR 插入 TRAC 基因位点,从而构建了 CD97 敲除的 CD97 靶向的 CAR-T 细胞(CD97KO CAR-T cell)。
结果显示,CD97 敲除的 CD97 靶向的 CAR-T 细胞(CD97KO CAR-T cell)能有效清除 AML 细胞系和原发性 AML 细胞,同时对造血干细胞/祖细胞(HSPC)表现出可耐受的毒性。此外,研究团队对 CAR 的 CD3ζ 结构域进行了突变,发现优化后的 CD97KO-9728z-1XX CAR-T 细胞在体外以及多种异种移植小鼠肿瘤模型中均表现出持久的抗肿瘤活性。从机制上来说,转录谱显示优化后的 CAR-T 细胞延缓了分化并具有抗耗竭能力。
该研究的核心发现:
CD97 是治疗急性髓系白血病(AML)的 CAR-T 细胞疗法的一个合适靶点;
CD97 基因敲除策略减轻了 CD97 靶向的 CAR-T 细胞的自相残杀;
CD97KO CAR-T 细胞对造血干细胞/祖细胞(HSPC)表现出可耐受的细胞毒性;
CD97KO-9728z-1XX CAR-T 细胞在体外和体内均表现出卓越的功能。
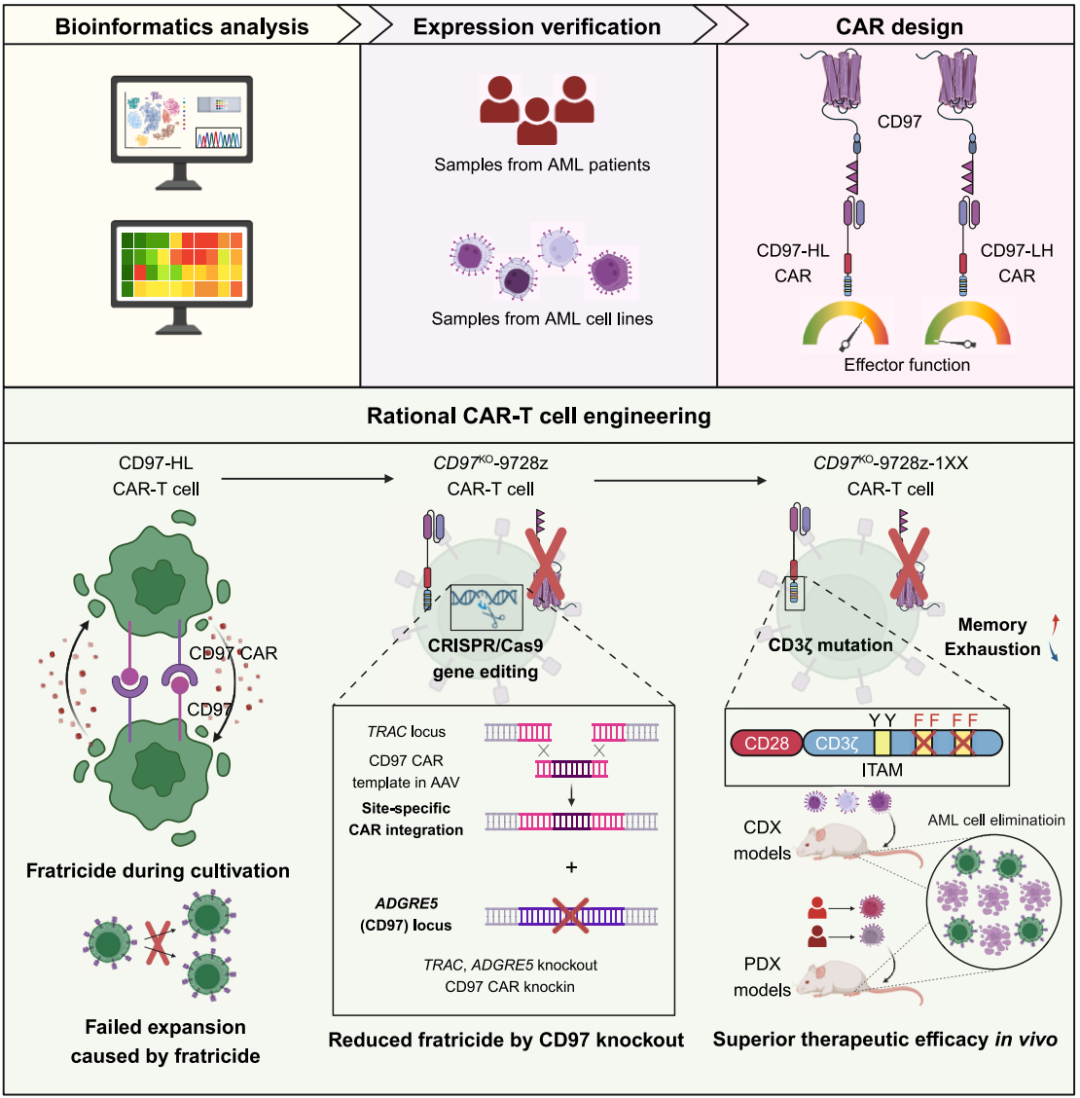
总的来说,这项研究支持 CD97 作为急性髓系白血病(AML)的 CAR-T 细胞疗法的一个有前景的靶点。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


