Nature 子刊: DAP5/eIF3d交替mRNA翻译机制促进人调节性T细胞分化和免疫抑制
来源:本站原创 2021-12-08 16:05
调节性T细胞(Treg细胞)抑制效应性T细胞,维持免疫系统的动态平衡。周围部位的Treg细胞成熟需要抑制蛋白激酶mTORC1和TGF-β-1(TGF-β)。
调节性T细胞(Treg细胞)抑制效应性T细胞,维持免疫系统的动态平衡。周围部位的Treg细胞成熟需要抑制蛋白激酶mTORC1和TGF-β-1(TGF-β)。虽然Treg细胞成熟需要蛋白质合成,但mTORC1抑制会下调它,使Treg细胞如何实现发育和免疫抑制活动所必需的mRNA翻译没有答案。
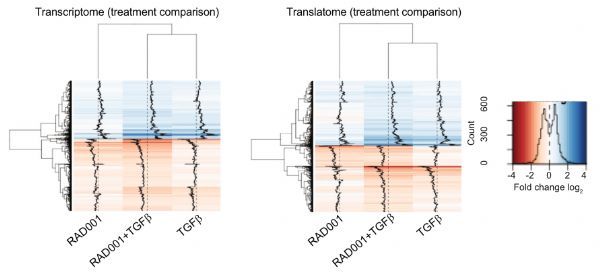
利用在培养中分化的人CD4+T细胞和全基因组转录和翻译图谱,作者报道了TGF-β在转录上重新编程初始T细胞以表达Treg细胞分化和免疫抑制mRNA,而mTORC1抑制则削弱T细胞mRNA的翻译,但不影响TGF-β诱导的翻译。与规范的mTORC1/eIF4E/eIF4G翻译不同,Treg细胞mRNAs利用eIF4G同源DAP5和启动因子eIF3d,这是一种非规范的翻译机制,需要由Treg细胞mRNA 5‘非编码区指导的eIF3d的帽依赖结合。
图片来源:https://doi.org/10.1038/s41467-021-27087-w
T细胞约占CD4+T淋巴细胞的5%,对活化的免疫细胞具有抗增殖作用。它们通过接触依赖和独立的机制发挥作用,从而维持免疫系统的动态平衡,抑制外周的效应性T细胞,控制对外来抗原的过度反应,并预防自身免疫性疾病。
Treg细胞可分为三个亚群:胸腺来源的Treg细胞(tTreg细胞),又称天然Treg细胞,外周来源的Treg细胞(pTreg细胞)和体外诱导的Treg细胞(iTreg细胞)3.tTreg细胞和pTreg细胞在动物体内自然存在,具有不同的功能。TTreg细胞主要参与抑制全身自身免疫,而pTreg细胞则抑制局部炎症反应。
抗原激活的初始CD4+T细胞分化为效应性T细胞或Treg细胞,部分受局部代谢参数和细胞因子的控制,尽管谱系表现出相当大的表型可塑性。MTOR复合物1(MTORC1)的抑制作用是产生和扩增Treg细胞所必需的,这是由维甲酸、短链脂肪酸、代谢应激或阻断mTORC1活性的药物抑制剂自然产生的。
MTOR是PI3K-Akt途径中的一种蛋白激酶,形成mTORC1和mTORC2两种复合物。MTORC1通过PI3K-AKT轴和MAPK通路被生长因子信号激活,并被低氧、低能量状态和营养水平降低等应激抑制。激活的mTORC1促进核糖体生物发生、mRNA翻译、DNA复制和修复,并抑制自噬。MTORC2由PI3K激活,调节肌动蛋白组织、细胞运动、Akt活性和其他激酶。
关于翻译调控在免疫细胞发育和功能中的作用,我们知之甚少。事实上,虽然只有一小部分哺乳动物mRNA实际参与翻译,特别是在细胞应激和发育细胞命运决定过程中,但全基因组翻译签名或翻译组的特征往往被忽视。
MTORC1部分通过4E-bps的磷酸化(失活)刺激翻译启动,4E-bps是帽结合蛋白eIF4E的负调控因子。抑制mTORC1导致4E-BPs的低磷酸化(激活),然后结合和隔离eIF4E,阻止它们与帽依赖的预启动复合物的相互作用,从而阻止核糖体向mRNAs募集。
MTORC1抑制和TGF-β治疗选择性促进规范Treg细胞mRNAs翻译
图片来源:https://doi.org/10.1038/s41467-021-27087-w
在这里,作者发现,在激活的人类CD4+初始T细胞中,mTORC1 mRNA翻译下调,与TGF-β转录重编程相结合,介导了强免疫抑制Treg细胞的发展。转录学和翻译学的比较研究表明,决定Treg细胞命运的mRNAs在翻译上具有特权,可以利用另一种帽依赖的mRNA翻译机制,该机制不依赖于mTORC1/eIF4E,由DAP5/eIF3d复合体指导,对于人类iTreg细胞从未承诺的CD4+T细胞发育是必不可少的。(生物谷 Bioon.com)
参考文献
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。