直击耐药性,中国**第三代BCR-ABL抑制剂奥雷巴替尼获批上市!
来源:生物谷 2021-12-19 12:23
奥雷巴替尼未来可期!
2021年11月25日,中国国家药品监督管理局(NMPA)宣布批准由亚盛医药全资子公司广州顺健生物医药科技有限公司研发的第三代BCR-ABL抑制剂奥雷巴替尼(商品名:耐立克®),用于治疗任何酪氨酸激酶抑制剂(TKI)耐药,并采用经充分验证的检测方法诊断为伴有T315I突变的慢性髓细胞白血病(CML)慢性期或加速期的成年患者。
奥雷巴替尼是我国自主研发并拥有自主知识产权的创新药,并获得国家“重大新药创制”专项支持。这也就意味着,奥雷巴替尼成为中国第一个、也是唯一一个第三代BCR-ABL抑制剂,解决了耐药慢粒白血病患者无药可医的重大问题。
CML是骨髓造血干细胞克隆性增值形成的恶性肿瘤,据数据显示,全球发病率为1.6/10万~2/10万,而我国发病率不容乐观为0.39/10万~0.55/10万,且中国CML患者较西方患者更为年轻化,中位发病年龄为45~50岁,西方为67岁。一代TKI作为一线治疗药物使CML患者的10年生存率达85%~90%,二代TKI一线治疗使CML患者能够获得更快更深的分子学反应,尽管如此,获得性耐药一直是CML治疗的主要挑战,仍有部分患者因耐药导致疾病进展甚至死亡。
根据亚盛医药早前公布的数据显示,中国的1期临床研究共入组100例CML患者,包括86例慢性期(CML-CP)患者,15例加速期(CML-AP)患者。奥雷巴替尼的使用方式为口服、隔天给药、28天为一个周期,总共探索的剂量范围从1mg至60 mg共11个剂量组。
结果显示,在CML-CP受试者中,基线未获得缓解的可评估受试者中,完全血液学缓解率(CHR)为100%,完全细胞遗传学缓解率(CCyR)为70%,主要分子学缓解率(MMR)为55%。携带仅T315I突变的可评估的CP受试者中CHR率为100%, MCyR率为90%,CCyR率为84%,MMR率为78%, MMR4.0率为68%,MR4.5率为58%。
在CML-AP受试者中,基线未获得缓解的可评估受试者中, CHR为92%, CCyR为43%,主要分子学缓解率(MMR)为43%。携带仅T315I突变的可评估的AP受试者中CHR率为67%, MCyR率为60%的,CCyR率 为60%,MMR率为60%,MMR4.0率为60%,MR4.5率为40%。
在安全性方面,大部分与治疗相关的不良事件为1级或2级,且不良事件经过暂停给药、降低治疗剂量或给予支持治疗后均可恢复正常。因此,奥雷巴替尼对TKI耐药的CML-CP或CML-AP受试者均有良好的耐受性和较强、较持续的抗肿瘤作用。值得一提的是,作为亚盛医药上市进度最快的重磅产品,奥雷巴替尼的临床进展已连续第四年入选ASH年会口头报告,充分显示了国际血液学界对其疗效和安全性的认可。
亚盛医药董事长、CEO杨大俊博士表示,“亚盛首款获批上市的核心产品奥雷巴替尼是填补国内空白、临床上不可或缺的急需产品,有效地解决了中国携T315I突变的耐药慢粒白血病患者无药可医的这一重大社会需求问题,让电影“我不是药神”里的社会之痛不再发生。未来,我们将继续坚守「解决中国乃至全球患者尚未满足的临床需求」的使命,带来更多满足临床急需的原创新药。希望在不远的将来,奥雷巴替尼这一中国原创、全球领先的创新药能惠及更多的患者。”
为了提升奥雷巴替尼的可及性和可负担性,据了解亚盛医药于今年7月已经与信达生物达成一项高达2.45亿美元的战略合作,合作内容之一就是双方将在中国联合开发及商业化奥雷巴替尼。另外,亚盛医药与基因检测公司、互联网医疗企业等合作伙伴达成合作,期待借助精准检测、互联网医院平台、商业保险等。
随着第三代BCR-ABL抑制剂的上市,期待中国本土创新力量实现弯道超车,让世界知道中国并没有落后。无论如何,CML治疗即将迎来全新的变革,奥雷巴替尼的上市,将惠及全球患者。据悉,奥雷巴替尼将进一步全球化。目前,正在美国开展开放性的桥接试验,旨在评估奥雷巴替尼对伴有或不伴有T315I突变的慢性期、加速期或急变期CML和Ph+ ALL的成人受试者的药代动力学、安全性和有效性。奥雷巴替尼的使用方式为口服、隔天给药。
参考资料
1.NCCN Clinical Practice Guidelines in Oncology: Chronic Myeloid Leukemia (Version 3.2021) available at www.nccn.org/patients
2.Hochhaus A, Breccia M. Leukemia. 2020 Jun;34(6):1495-1502.
3.慢性髓性白血病中国诊断与治疗指南(2020年版). 中华血液学杂志. 2020, 41(5): 353-364.
正如奥雷巴替尼中国临床试验主要研究者、北京大学血液病研究所所长、北京大学人民医院血液科主任黄晓军教授在由中国医药创新促进会主办、亚盛医药承办的国家“重大新药创制”专项成果发布暨奥雷巴替尼全球首发上市会上表示,“过往临床研究的有效性和安全性数据不断向我们显示,奥雷巴替尼在耐药慢性髓细胞白血病这个尚未满足的临床需求领域潜力巨大,极有希望成为该领域治疗的’Best-in-Class’药物。很高兴能见证奥雷巴替尼成功上市,因为这意味着中国CML治疗原有的耐药困境被打破,迎来了全新的里程碑药物,对临床医生和患者的意义巨大。”
CML是骨髓造血干细胞克隆性增值形成的恶性肿瘤,据数据显示,全球发病率为1.6/10万~2/10万,而我国发病率不容乐观为0.39/10万~0.55/10万,且中国CML患者较西方患者更为年轻化,中位发病年龄为45~50岁,西方为67岁。一代TKI作为一线治疗药物使CML患者的10年生存率达85%~90%,二代TKI一线治疗使CML患者能够获得更快更深的分子学反应,尽管如此,获得性耐药一直是CML治疗的主要挑战,仍有部分患者因耐药导致疾病进展甚至死亡。
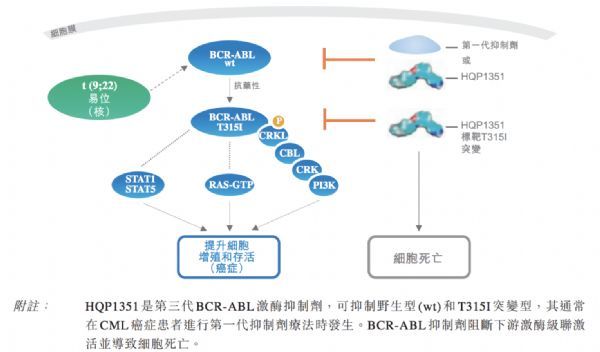
BCR-ABL激酶区突变是获得性耐药的重要机制之一,其中T315I突变是常见的耐药突变类型之一,在耐药CML中的发生率高达25%左右。伴有T315I突变的耐药CML患者对目前所有一代、二代BCR-ABL抑制剂均耐药。而第三代BCR-ABL抑制剂奥雷巴替尼是小分子蛋白酪氨酸激酶抑制剂,可有效抑制BCR-ABL酪氨酸激酶野生型及多种突变型的活性,可抑制BCR-ABL酪氨酸激酶及下游蛋白STAT5和Crkl的磷酸化,阻断下游通路活化,诱导BCR-ABL阳性、BCR-ABLT315I突变型细胞株的细胞周期阻滞和调亡。
根据亚盛医药早前公布的数据显示,中国的1期临床研究共入组100例CML患者,包括86例慢性期(CML-CP)患者,15例加速期(CML-AP)患者。奥雷巴替尼的使用方式为口服、隔天给药、28天为一个周期,总共探索的剂量范围从1mg至60 mg共11个剂量组。
结果显示,在CML-CP受试者中,基线未获得缓解的可评估受试者中,完全血液学缓解率(CHR)为100%,完全细胞遗传学缓解率(CCyR)为70%,主要分子学缓解率(MMR)为55%。携带仅T315I突变的可评估的CP受试者中CHR率为100%, MCyR率为90%,CCyR率为84%,MMR率为78%, MMR4.0率为68%,MR4.5率为58%。
在CML-AP受试者中,基线未获得缓解的可评估受试者中, CHR为92%, CCyR为43%,主要分子学缓解率(MMR)为43%。携带仅T315I突变的可评估的AP受试者中CHR率为67%, MCyR率为60%的,CCyR率 为60%,MMR率为60%,MMR4.0率为60%,MR4.5率为40%。
在安全性方面,大部分与治疗相关的不良事件为1级或2级,且不良事件经过暂停给药、降低治疗剂量或给予支持治疗后均可恢复正常。因此,奥雷巴替尼对TKI耐药的CML-CP或CML-AP受试者均有良好的耐受性和较强、较持续的抗肿瘤作用。值得一提的是,作为亚盛医药上市进度最快的重磅产品,奥雷巴替尼的临床进展已连续第四年入选ASH年会口头报告,充分显示了国际血液学界对其疗效和安全性的认可。
亚盛医药董事长、CEO杨大俊博士表示,“亚盛首款获批上市的核心产品奥雷巴替尼是填补国内空白、临床上不可或缺的急需产品,有效地解决了中国携T315I突变的耐药慢粒白血病患者无药可医的这一重大社会需求问题,让电影“我不是药神”里的社会之痛不再发生。未来,我们将继续坚守「解决中国乃至全球患者尚未满足的临床需求」的使命,带来更多满足临床急需的原创新药。希望在不远的将来,奥雷巴替尼这一中国原创、全球领先的创新药能惠及更多的患者。”
为了提升奥雷巴替尼的可及性和可负担性,据了解亚盛医药于今年7月已经与信达生物达成一项高达2.45亿美元的战略合作,合作内容之一就是双方将在中国联合开发及商业化奥雷巴替尼。另外,亚盛医药与基因检测公司、互联网医疗企业等合作伙伴达成合作,期待借助精准检测、互联网医院平台、商业保险等。
随着第三代BCR-ABL抑制剂的上市,期待中国本土创新力量实现弯道超车,让世界知道中国并没有落后。无论如何,CML治疗即将迎来全新的变革,奥雷巴替尼的上市,将惠及全球患者。据悉,奥雷巴替尼将进一步全球化。目前,正在美国开展开放性的桥接试验,旨在评估奥雷巴替尼对伴有或不伴有T315I突变的慢性期、加速期或急变期CML和Ph+ ALL的成人受试者的药代动力学、安全性和有效性。奥雷巴替尼的使用方式为口服、隔天给药。
参考资料
1.NCCN Clinical Practice Guidelines in Oncology: Chronic Myeloid Leukemia (Version 3.2021) available at www.nccn.org/patients
2.Hochhaus A, Breccia M. Leukemia. 2020 Jun;34(6):1495-1502.
3.慢性髓性白血病中国诊断与治疗指南(2020年版). 中华血液学杂志. 2020, 41(5): 353-364.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->