《自然·代谢》:浙大团队揭开胆固醇诱发肝癌之迷!
来源:奇点糕 2022-09-26 13:27
这项研究以SNHG6为突破点,发掘了胆固醇/FAF2/SNHG6/mTOR信号轴在内质网-溶酶体接触区域激活mTORC1信号的作用,揭示了胆固醇促进非酒精性脂肪肝进展为肝癌的机制
肝癌(HCC),是全球第六大癌症,主要病因包括病毒性肝炎、酒精和非酒精性脂肪性肝炎、黄曲霉素污染等。
尽管肝炎病毒疫苗大规模接种、抗肝炎药物广泛应用以及饮食卫生大幅提高,但在过去的十年,肝癌发病率仍旧呈现上升趋势。最近有研究发现,非酒精性脂肪性肝炎是全球肝癌发病增长最快的病因[1]。
非酒精性脂肪性肝病(NAFLD)是酒精和毒素之外的因素引起的肝脏脂代谢障碍疾病。NAFLD首先表现为肝细胞内脂肪过度沉积,随后从脂肪肝进展为脂肪性肝炎,再进一步导致肝硬化,最后癌变为肝癌[2]。在这个过程中,胆固醇被认为是主要的脂毒性分子。
mTOR信号通路在肝癌的发生中具有重要作用,以mTOR为核心的蛋白复合物mTORC1定位至溶酶体表面被激活,促进肝癌细胞增殖。有研究表明,胆固醇是mTORC1的必要激活剂,介导mTORC1在溶酶体的招募和激活[3]。内质网-溶酶体接触是激活胆固醇依赖性mTORC1信号的枢纽,然而,相关机制目前尚不清楚。
近日,浙江大学林爱福和周天华领衔的团队,发现lncRNA SNHG6能充当支架分子,通过结合FAF2和mTOR,增强内质网-溶酶体接触,促进胆固醇招募mTORC1至溶酶体激活,从而加速胆固醇驱动的NAFLD-HCC发展。
相关论文发表于医学顶级期刊《自然·代谢》上[4]。浙江大学生科院博士生刘方舟和张桢,以及暨南大学田甜博士为论文的共同第一作者。

论文首页截图
有研究表明,肿瘤的发生往往与lncRNAs的异常表达有关[5]。研究人员收集肝癌样本进行转录组测序,同时结合多个线上数据库,获得肝癌差异表达lncRNA,其中SNHG6在肝癌中的表达丰度最高。
生存分析显示SNHG6高表达患者预后不良,细胞实验证实SNHG6促进肝癌增殖,这些结果表明,SNHG6作为一个癌基因参与了肝癌的发生。
我们都知道,癌基因能通过改变细胞代谢诱导肿瘤细胞的恶性生物学行为[6]。为了研究SNHG6对肝癌细胞代谢重编程的影响,研究人员使用多种营养物质处理肝癌细胞,发现胆固醇等营养物质都能促进肝癌细胞增殖,但只有胆固醇特异性地上调了SNHG6的表达,敲除SNHG6则胆固醇无法诱导肝癌细胞增殖,表明SNHG6作为胆固醇的效应分子促进肝癌的进展。
随后,研究人员定位了SNHG6在肝癌细胞中的分布,发现SNHG6富集在内质网-溶酶体接触处,胆固醇能促进SNHG6定位于内质网和溶酶体,提示SNHG6作为胆固醇的效应分子,是在内质网-溶酶体接触点发挥生物功能。
那么,SNHG6是如何定位至内质网-溶酶体接触点的呢?
研究人员把目光聚焦在了与SNHG6结合的蛋白,发现蛋白FAF2和mTOR不仅可以结合SNHG6,而且在细胞器的分布也与SNHG6一致。
FAF2是内质网相关蛋白,位于内质网表面,mTOR则形成复合物mTORC1定位至溶酶体表面。进一步的实验证实SNHG6在肝癌细胞中分布于内质网-溶酶体接触点,需要先与FAF2和mTOR结合。
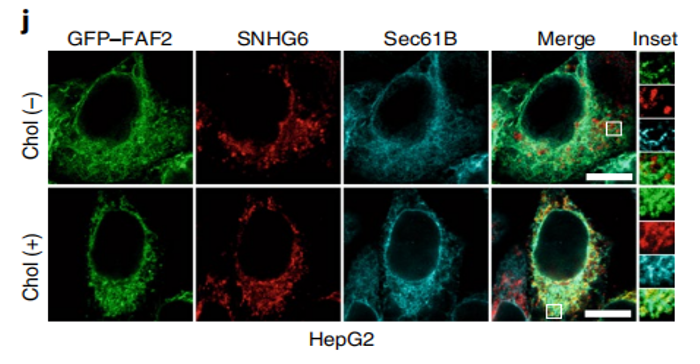
SNHG6在肝癌细胞中与FAF2和mTOR结合,并受到胆固醇的调节
接下来,研究人员对胆固醇和SNHG6-FAF2-mTOR复合物的关系进行了探究。
肝癌细胞补充胆固醇后,SNHG6-FAF2-mTOR复合物的形成显著增多,但敲除SNHG6,即使补充胆固醇,FAF2和mTOR的结合依旧明显降低;而敲除FAF2和mTOR中的任意一个,补充胆固醇也能增加SNHG6与另外一个蛋白的结合。这些结果表明,SNHG6作为一个支架,以胆固醇依赖的方式促进FAF2和mTOR的相互作用。
由于内质网-溶酶体接触是胆固醇激活mTORC1信号的前提,而SNHG6-FAF2-mTOR复合物中的FAF2位于内质网表面,研究人员探究了FAF2在mTORC1信号传导中的功能。
过表达或敲除FAF2,则胆固醇诱导的mTORC1激活增加或减少,肝癌细胞的增殖能力也相应地增强或减弱。
分子对接实验发现在内质网表面胆固醇能与FAF2直接结合,改变FAF2蛋白构象。FAF2构象发生变化后,招募SNHG6,而SNHG6结合了mTORC1复合物中的mTOR,由此SNHG6-FAF2-mTOR形成三元复合物,促进mTORC1转运至溶酶体表面。
这些结果表明,胆固醇在肝癌细胞中通过SNHG6-FAF2-mTOR轴调节mTORC1的激活,促进肝癌细胞恶性增殖。
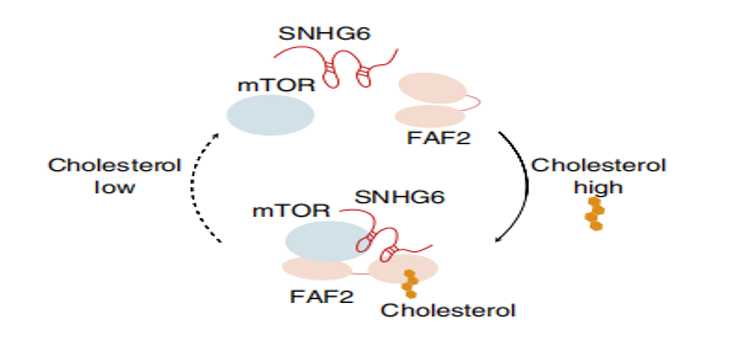
胆固醇调节SNHG6-FAF2-mTOR复合物的形成
最后,研究人员进行动物实验,体内验证SNHG6在胆固醇诱导的肝癌中的作用。
肝癌诱导小鼠饲喂高胆固醇饮食,构建非酒精性脂肪肝癌变动物模型。在第10周,SNHG6过表达小鼠更早地出现肝脏重量增加,肝脏脂肪变性,脂肪生成和炎症相关基因表达水平升高;而SNHG6敲除小鼠肝脏脂肪变性程度降低,mTORC1信号减弱,提示SNHG6在高胆固醇饮食下加速了mTORC1的激活。
至第18周,在高胆固醇饮食的刺激下,SNHG6过表达小鼠进展为非酒精性脂肪性肝炎,肝脏在脂肪变性的基础上炎症水平进一步升高,出现纤维化,肝脏重量和肝脏/体重比显著增加;SNHG6敲除小鼠则更晚出现非酒精性脂肪性肝炎,而且表现更轻微。
至第30周,相比于SNHG6敲除鼠,SNHG6过表达小鼠的肝脏长出更多的肿瘤。这些结果证实,SNHG6通过促进mTORC1的激活,加剧胆固醇诱导非酒精性脂肪肝进展为肝癌。
此外,研究人员还在肝癌原位异种移植模型中验证了SNHG6的促肝癌作用。他们发现胆固醇饮食增加了肝癌移植瘤的体积和重量,而敲除SNHG6,肝癌细胞mTORC1激活减弱,增殖和血管生成减少,高胆固醇诱导的肿瘤生长被抑制。
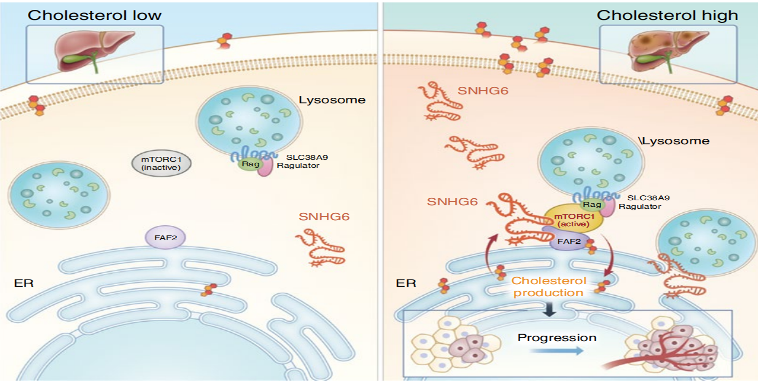
胆固醇/FAF2/SNHG6/mTOR信号轴促进mTORC1激活机制示意图
总的来说,研究人员检测到lncRNA SNHG6在肝癌中高表达导致患者预后不良,是肝癌的一个癌基因,发现SNHG6在内质网-溶酶体接触处作为支架分子,一端连接被胆固醇改变构象的FAF2,另一端结合mTOR,形成SNHG6-FAF2-mTOR复合物,促进mTORC1在溶酶体的激活。
这项研究以SNHG6为突破点,发掘了胆固醇/FAF2/SNHG6/mTOR信号轴在内质网-溶酶体接触区域激活mTORC1信号的作用,揭示了胆固醇促进非酒精性脂肪肝进展为肝癌的机制,拓宽了对lncRNA功能模式及作用方式的认知,为非酒精性脂肪性肝病的干预和肝癌的防治提供了新靶点。
参考文献
[1] Huang DQ, Singal AG, Kono Y, Tan DJH, El-Serag HB, Loomba R. Changing global epidemiology of liver cancer from 2010 to 2019: NASH is the fastest growing cause of liver cancer. Cell Metab. 2022;34(7):969-977.e2. doi:10.1016/j.cmet.2022.05.003
[2] Huang DQ, El-Serag HB, Loomba R. Global epidemiology of NAFLD-related HCC: trends, predictions, risk factors and prevention. Nat Rev Gastroenterol Hepatol. 2021;18(4):223-238. doi:10.1038/s41575-020-00381-6
[3] Lu X, Paliogiannis P, Calvisi DF, Chen X. Role of the Mammalian Target of Rapamycin Pathway in Liver Cancer: From Molecular Genetics to Targeted Therapies. Hepatology. 2021;73 Suppl 1(Suppl 1):49-61. doi:10.1002/hep.31310
[4] Liu F, Tian T, Zhang Z, et al. Long non-coding RNA SNHG6 couples cholesterol sensing with mTORC1 activation in hepatocellular carcinoma. Nat Metab. 2022;4(8):1022-1040. doi:10.1038/s42255-022-00616-7
[5] Xing Z, Lin A, Li C, et al. lncRNA directs cooperative epigenetic regulation downstream of chemokine signals. Cell. 2014;159(5):1110-1125. doi:10.1016/j.cell.2014.10.013
[6] Satriano L, Lewinska M, Rodrigues PM, Banales JM, Andersen JB. Metabolic rearrangements in primary liver cancers: cause and consequences. Nat Rev Gastroenterol Hepatol. 2019;16(12):748-766. doi:10.1038/s41575-019-0217-8
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


