神经干细胞研究进展(第3期)
来源:本站原创 2019-04-27 20:10
2019年4月27日讯/生物谷BIOON/---神经干细胞(neural stem cell)是指存在于神经系统中,具有分化为神经神经元、星形胶质细胞和少突胶质细胞的潜能,从而能够产生大量脑细胞组织,并能进行自我更新,并足以提供大量脑组织细胞的细胞群。需要注意的是,在脑脊髓等所有神经组织中,不同的神经干细胞类型产生的子代细胞种类不同,分布也不同。 神经干细胞的治疗机理是:(i)患病部位组织损伤后释
2019年4月27日讯/生物谷BIOON/---神经干细胞(neural stem cell)是指存在于神经系统中,具有分化为神经神经元、星形胶质细胞和少突胶质细胞的潜能,从而能够产生大量脑细胞组织,并能进行自我更新,并足以提供大量脑组织细胞的细胞群。需要注意的是,在脑脊髓等所有神经组织中,不同的神经干细胞类型产生的子代细胞种类不同,分布也不同。 神经干细胞的治疗机理是:(i)患病部位组织损伤后释放各种趋化因子,可以吸引神经干细胞聚集到损伤部位,并在局部微环境的作用下分化为不同种类的细胞,修复及补充损伤的神经细胞。由于缺血、缺氧导致的血管内皮细胞、胶质细胞的损伤,使局部通透性增加,另外在多种黏附分子的作用下,神经干细胞可以透过血脑屏障,高浓度的聚集在损伤部位;(ii)神经干细胞可以分泌多种神经营养因子,促进损伤细胞的修复;(iii)神经干细胞可以增强神经突触之间的联系,建立新的神经环路。
神经干细胞应用中存在的问题:建立的神经干细胞系绝大多数来源于鼠,而鼠与人之间存在着明显的种属差异;神经干细胞的来源不足;部分移植的神经干细胞发展成脑瘤;神经干细胞转染范围的非选择性表达及转染基因表达的原位调节等等。
基于此,小编针对近年来神经干细胞研究取得的进展进行一番盘点,以飨读者。
1.Cell:在哺乳动物的一生当中,单个干细胞群体促进海马体中的神经发生
doi:10.1016/j.cell.2019.02.010
科学家们曾经认为,哺乳动物在进入成年期时,拥有它们所拥有的所有神经元,但是上世纪60年代的研究发现,成年大脑的某些部位会产生新的神经元,而上世纪90年代的开创性研究帮助确定了它们的起源和功能。如今,在一项新的研究中,来自美国宾夕法尼亚大学的研究人员在小鼠身上发现单个神经祖细胞(neural progenitor)谱系参与了海马体中的胚胎、出生后早期和成年神经发生(neurogenesis),而且这些细胞在一生当中持续产生。相关研究结果于2019年3月28日在线发表在Cell期刊上,论文标题为“A Common Embryonic Origin of Stem Cells Drives Developmental and Adult Neurogenesis”。

神经发生最初被认为具有两个阶段:发育阶段,其主要发生在胚胎中和出生后不久,并且在这个阶段,神经元由构建完整神经系统中的神经回路的干细胞产生。成年神经发生被认为源自一个特殊的“预留”的神经干细胞群体,这些神经干细胞不同于在胚胎发生期间产生神经元的前体细胞。但是,事实证明这并不那么简单。
在这项新的研究中,这些研究人员在大脑发育的早期阶段对小鼠中的前体神经干细胞进行标记。他们随后在发育期间追踪了细胞的谱系一直成年期。他们的发现揭示出具有这些前体细胞标记的新神经干细胞在这些小鼠的一生当中不断产生。
2.Stem Cell Rep:利用体外培养干细胞能够重建鼻腔的组织结构与嗅觉功能
doi:10.1016/j.stemcr.2019.02.014
塔夫茨大学医学院的一组研究人员开发了一种培养嗅觉干细胞的方法,然后用于恢复鼻腔组织。这一发现使人们希望未来的治疗方法可以用来恢复因受伤或退化而受损的个体的嗅觉。这种被称为水平基底细胞(HBC)的干细胞在移植到受损组织中时可以重新填充所有嗅上皮(OE)细胞类型,包括感觉神经元。相关结果发表在《Stem Cell Reports》杂志上,该发展为进一步研究干细胞移植疗法或刺激鼻内干细胞再生组织的药理学方法铺平了道路。
与神经系统的其他部分相比,赋予嗅觉的神经是独特的,因为它们可以在受伤后触发强健且几乎完全的再生反应。鼻腔组织含有两种类型的干细胞 - 球状基底细胞(GBCs)和HBC。 GBCs已经成功培养,并且似乎在重新填充已经失去常规营业额的细胞中起主要作用。然而,HBC仍处于休眠状态,直到受伤才会激活。不幸的是,对这些细胞的研究受限于它们不能在培养中扩增和维持的事实。在这项研究中,研究人员确定了在培养中扩增和维持健康HBC干细胞的最佳条件,借用方法和用于维持呼吸干细胞的因子。
3.Cell:为了不被团灭,衰老脑干细胞在炎症刺激下休眠
doi:10.1016/j.cell.2019.01.040
近日来自德国癌症研究中心(German Cancer Research Center,DKFZ)的研究人员在《Cell》上发表研究表明老鼠衰老之后大脑中的干细胞数量会骤减,剩下的干细胞会通过进入休眠状态来防止它们被完全摧毁。这些衰老的干细胞很难苏醒,但是一旦被再次激活,它们就可以和年轻干细胞一样朝气蓬勃。

这些细胞的休眠主要由干细胞环境中的炎症信号介导,因此抗炎物质也许是唤醒这些干细胞并刺激衰老大脑中的修复过程的关键所在。
成年人大脑中特定部位的干细胞可以终生产生新的神经元。这些干细胞也会在大脑损伤后被激活,此外还可能成为特殊脑癌的源头。但是在衰老的大脑中,年轻神经元的补充会减少。来自DKFZ的干细胞科学家Ana Martin-Villalba及其团队与海德堡和卢森堡大学的研究人员合作发现了干细胞失能的一个原因。他们发现随着衰老的发生,这些干细胞的数量会骤减。
该研究团队发现炎性化学信号以及关键Wnt信号通路中的信号似乎会促进这个休眠过程。当使用抗体终止这些信号的传入后,神经元干细胞的分裂活性增加,会提供更多的新生神经元用于日常生活和修复过程。
4.Nature:揭示一种调节神经干细胞的新机制
doi:10.1038/s41586-019-0962-4
使用干细胞修复器官是现代再生医学的首要目标之一。在一项新的研究中,来自德国亥姆霍兹慕尼黑中心和慕尼黑大学的研究人员发现蛋白Akna在这个修复过程中起着关键作用。比如,它通过一种可能也参与转移瘤形成的机制控制神经干细胞的行为。相关研究结果于2019年2月20日在线发表在Nature期刊上,论文标题为“The centrosome protein AKNA regulates neurogenesis via microtubule organization”。论文通讯作者为亥姆霍兹慕尼黑中心干细胞研究所主任、慕尼黑大学生物医学中心生理基因组学主席Magdalena Götz教授。论文第一作者为Germán Camargo Ortega、Sven Falk和Pia A. Johansson。
在这项新的研究中,Götz及其团队想要确定调节神经干细胞维持或分化的因子。为此,他们分离出神经干细胞,它们要么能够自我更新并产生更多的神经干细胞,要么发生分化。
Ortega解释道,“我们发现Akna蛋白在产生神经元的神经干细胞中具有较高的浓度。我们的实验表明低水平的Akna蛋白导致神经干细胞保持在干细胞微环境(stem cell niche)中,然而较高水平的Akna蛋白促使它们离开这种干细胞微环境,因而促进它们发生分化。”
这些研究人员吃惊地发现了这种蛋白所处的位置---位于细胞内部的中心体(centrosome)。作为一种细胞器,中心体在组装细胞骨架和调节细胞分裂中起着至关重要的作用。Falk报道,“我们发现最初发布的这种蛋白的序列是不正确的。不过,我们的研究清楚地表明蛋白Akna直接位于中心体。”这些研究人员能够证实Akna在中心体处招募和锚定微管。这削弱了神经干细胞与邻近细胞之间的连接,促进它们脱离干细胞微环境并迁移出去。
5.Nature:揭示大脑干细胞转化成为新型神经细胞或引发脑癌的分子机制
doi:10.1038/s41586-019-0888-x
干细胞是我们身体的“万能钥匙”,因为其能转化为所有器官中许多不同类型的细胞,其能够帮助肌肉(甚至是大脑)等组织不断更新并进行损伤后愈合,这种神奇的多潜能性使得干细胞有望成为未来科学家们开发再生医学疗法的关键工具,近日,一项刊登在国际杂志Nature上的研究报告中,来自德国癌症研究中心的科学家们通过研究阐明了大脑干细胞如何制定决策转化成为新型神经细胞。

研究者Ana Martin-Villalba及其同事一直在沿着通往神经元细胞的路径来追踪干细胞的行为,他们追踪了每一个阶段基因的表达情况,并分析了哪些基因会进行表达并翻译成新型蛋白,研究者发现,干细胞只需要完全关闭干细胞的基因就能转变成为神经元细胞,但事实证明这一过程非常复杂,干细胞的基因并没有完全关闭,而是处于待命状态,即通过抑制制造使其处于细胞多潜能性的蛋白产物来实现这一状态。
研究者Ana Martin-Villalba说道,当其处于“待机”模式时,干细胞就开始了转变成为神经元的旅程,其会关闭内在的增殖信号(TOR)并开始停止分裂,让研究人员非常好奇的是,他们还发现,干细胞总是会购买一张“返程票”,就好像在不同国家之间来回飞行的航班一样,开启或关闭TOR信号就能促进细胞在干细胞和神经元细胞之间来回往返,因此,干细胞转变成为神经元的决定在一段时间内是可逆的。
6.Cell Stem Cell:重大进展!将人成熟的血细胞直接重编程为一类新的神经干细胞
doi:10.1016/j.stem.2018.11.015
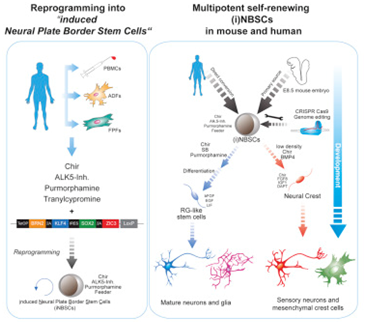
在一项新的研究中,来自德国癌症研究中心(DKFZ)和海德堡干细胞技术与实验医学研究所(HI-STEM)的研究人员首次成功地将人血细胞直接重新编程为一种以前未知的神经干细胞。这些诱导性干细胞类似于在中枢神经系统的早期胚胎发育期间形成的干细胞。它们能够在实验室中进行修饰和无限期地增殖,并且代表着一种用于再生疗法开发的候选对象。相关研究结果于2018年12月20日在线发表在Cell Stem Cell期刊上,论文标题为“Identification of Embryonic Neural Plate Border Stem Cells and Their Generation by Direct Reprogramming from Adult Human Blood Cells”。论文通讯作者为Andreas Trumpp和Marc ChristianThier。
Trumpp团队首次成功地将成熟的人细胞重编程为一种特定类型的能够几乎无限增殖的诱导性神经干细胞,他们称之为诱导性神经板边界干细胞(induced neural plate border stem cell, iNBSC)。Thier解释道,“像日本科学家Shinya Yamanaka样,我们使用了4种遗传因子,不过使用了4种不同的遗传因子用于我们的重编程中。我们认为,我们的遗传因子将允许重编程到神经系统发育的早期阶段。”
这些iNBSC具有广泛的发育潜力。iNBSC具有增殖能力和多能性,能够朝两个方向进行发育。一方面,它们能够选择产生中枢神经系统中的成熟的神经细胞和神经胶质细胞的发育途径。另一方面,它们也能够发育成神经嵴细胞,这些神经嵴细胞产生不同的细胞类型,比如周围敏感性的神经元,颅骨的软骨细胞或骨细胞。
7.Stem Cell Rep:重磅!科学家鉴别出决定细胞命运的干细胞特性
doi:10.1016/j.stemcr.2018.08.011
近日,一项刊登在国际杂志Stem Cell Reports上的研究报告中,来自加利福尼亚大学的科学家们通过研究鉴别出了能够影响神经干细胞命运的固有细胞特性,这些特性或许会影响神经干细胞分化称为哪种脑细胞,比如神经元、星形细胞和少突神经胶质细胞等,相关研究结果或能帮助研究人员开发出新方法来预测或控制干细胞的命运,从而更好地应用于人类的移植治疗中。
研究者Lisa A. Flanagan教授表示,神经干细胞常常会因细胞表面表达不同的糖类模式而表现出不同的的命运,这些糖类分子会促进神经干细胞膜的电位特性并最终决定其细胞命运;干细胞能够帮助治疗多种人类疾病,但研究人员却很难确定当这些干细胞被移植到患者机体中后其会转变成为什么细胞类型。当研究者将相同数量的干细胞分别移植到两名患者机体中后,如果干细胞在其中一名患者体内分化称为神经元,而在另一位患者机体中分化为星形细胞后,这两位患者最后的治疗情况会发生明显差异;基于当前研究结果,研究人员就能够预测神经干细胞的分化终点以及其可能的细胞命运,这或许能够增强干细胞移植疗法治疗多种类型疾病的成功率。
这项研究中,研究人员检测了几种给细胞表面添加糖类分子的通路,结果发现了一种通路能够帮助制造神经元,而另一种通路则能够帮助制造星形细胞,研究人员通过刺激神经干细胞通路,改变细胞电位特性,从而就能够制造更多的星形细胞和较少的神经元细胞这就表明,细胞表面的糖类分子能够控制神经干细胞的命运。(生物谷 Bioon.com)
神经干细胞应用中存在的问题:建立的神经干细胞系绝大多数来源于鼠,而鼠与人之间存在着明显的种属差异;神经干细胞的来源不足;部分移植的神经干细胞发展成脑瘤;神经干细胞转染范围的非选择性表达及转染基因表达的原位调节等等。
基于此,小编针对近年来神经干细胞研究取得的进展进行一番盘点,以飨读者。
1.Cell:在哺乳动物的一生当中,单个干细胞群体促进海马体中的神经发生
doi:10.1016/j.cell.2019.02.010
科学家们曾经认为,哺乳动物在进入成年期时,拥有它们所拥有的所有神经元,但是上世纪60年代的研究发现,成年大脑的某些部位会产生新的神经元,而上世纪90年代的开创性研究帮助确定了它们的起源和功能。如今,在一项新的研究中,来自美国宾夕法尼亚大学的研究人员在小鼠身上发现单个神经祖细胞(neural progenitor)谱系参与了海马体中的胚胎、出生后早期和成年神经发生(neurogenesis),而且这些细胞在一生当中持续产生。相关研究结果于2019年3月28日在线发表在Cell期刊上,论文标题为“A Common Embryonic Origin of Stem Cells Drives Developmental and Adult Neurogenesis”。

图片来自Cell, 2019, doi:10.1016/j.cell.2019.02.010。
神经发生最初被认为具有两个阶段:发育阶段,其主要发生在胚胎中和出生后不久,并且在这个阶段,神经元由构建完整神经系统中的神经回路的干细胞产生。成年神经发生被认为源自一个特殊的“预留”的神经干细胞群体,这些神经干细胞不同于在胚胎发生期间产生神经元的前体细胞。但是,事实证明这并不那么简单。
在这项新的研究中,这些研究人员在大脑发育的早期阶段对小鼠中的前体神经干细胞进行标记。他们随后在发育期间追踪了细胞的谱系一直成年期。他们的发现揭示出具有这些前体细胞标记的新神经干细胞在这些小鼠的一生当中不断产生。
2.Stem Cell Rep:利用体外培养干细胞能够重建鼻腔的组织结构与嗅觉功能
doi:10.1016/j.stemcr.2019.02.014
塔夫茨大学医学院的一组研究人员开发了一种培养嗅觉干细胞的方法,然后用于恢复鼻腔组织。这一发现使人们希望未来的治疗方法可以用来恢复因受伤或退化而受损的个体的嗅觉。这种被称为水平基底细胞(HBC)的干细胞在移植到受损组织中时可以重新填充所有嗅上皮(OE)细胞类型,包括感觉神经元。相关结果发表在《Stem Cell Reports》杂志上,该发展为进一步研究干细胞移植疗法或刺激鼻内干细胞再生组织的药理学方法铺平了道路。
与神经系统的其他部分相比,赋予嗅觉的神经是独特的,因为它们可以在受伤后触发强健且几乎完全的再生反应。鼻腔组织含有两种类型的干细胞 - 球状基底细胞(GBCs)和HBC。 GBCs已经成功培养,并且似乎在重新填充已经失去常规营业额的细胞中起主要作用。然而,HBC仍处于休眠状态,直到受伤才会激活。不幸的是,对这些细胞的研究受限于它们不能在培养中扩增和维持的事实。在这项研究中,研究人员确定了在培养中扩增和维持健康HBC干细胞的最佳条件,借用方法和用于维持呼吸干细胞的因子。
3.Cell:为了不被团灭,衰老脑干细胞在炎症刺激下休眠
doi:10.1016/j.cell.2019.01.040
近日来自德国癌症研究中心(German Cancer Research Center,DKFZ)的研究人员在《Cell》上发表研究表明老鼠衰老之后大脑中的干细胞数量会骤减,剩下的干细胞会通过进入休眠状态来防止它们被完全摧毁。这些衰老的干细胞很难苏醒,但是一旦被再次激活,它们就可以和年轻干细胞一样朝气蓬勃。

图片来源:Cell
这些细胞的休眠主要由干细胞环境中的炎症信号介导,因此抗炎物质也许是唤醒这些干细胞并刺激衰老大脑中的修复过程的关键所在。
成年人大脑中特定部位的干细胞可以终生产生新的神经元。这些干细胞也会在大脑损伤后被激活,此外还可能成为特殊脑癌的源头。但是在衰老的大脑中,年轻神经元的补充会减少。来自DKFZ的干细胞科学家Ana Martin-Villalba及其团队与海德堡和卢森堡大学的研究人员合作发现了干细胞失能的一个原因。他们发现随着衰老的发生,这些干细胞的数量会骤减。
该研究团队发现炎性化学信号以及关键Wnt信号通路中的信号似乎会促进这个休眠过程。当使用抗体终止这些信号的传入后,神经元干细胞的分裂活性增加,会提供更多的新生神经元用于日常生活和修复过程。
4.Nature:揭示一种调节神经干细胞的新机制
doi:10.1038/s41586-019-0962-4
使用干细胞修复器官是现代再生医学的首要目标之一。在一项新的研究中,来自德国亥姆霍兹慕尼黑中心和慕尼黑大学的研究人员发现蛋白Akna在这个修复过程中起着关键作用。比如,它通过一种可能也参与转移瘤形成的机制控制神经干细胞的行为。相关研究结果于2019年2月20日在线发表在Nature期刊上,论文标题为“The centrosome protein AKNA regulates neurogenesis via microtubule organization”。论文通讯作者为亥姆霍兹慕尼黑中心干细胞研究所主任、慕尼黑大学生物医学中心生理基因组学主席Magdalena Götz教授。论文第一作者为Germán Camargo Ortega、Sven Falk和Pia A. Johansson。
在这项新的研究中,Götz及其团队想要确定调节神经干细胞维持或分化的因子。为此,他们分离出神经干细胞,它们要么能够自我更新并产生更多的神经干细胞,要么发生分化。
Ortega解释道,“我们发现Akna蛋白在产生神经元的神经干细胞中具有较高的浓度。我们的实验表明低水平的Akna蛋白导致神经干细胞保持在干细胞微环境(stem cell niche)中,然而较高水平的Akna蛋白促使它们离开这种干细胞微环境,因而促进它们发生分化。”
这些研究人员吃惊地发现了这种蛋白所处的位置---位于细胞内部的中心体(centrosome)。作为一种细胞器,中心体在组装细胞骨架和调节细胞分裂中起着至关重要的作用。Falk报道,“我们发现最初发布的这种蛋白的序列是不正确的。不过,我们的研究清楚地表明蛋白Akna直接位于中心体。”这些研究人员能够证实Akna在中心体处招募和锚定微管。这削弱了神经干细胞与邻近细胞之间的连接,促进它们脱离干细胞微环境并迁移出去。
5.Nature:揭示大脑干细胞转化成为新型神经细胞或引发脑癌的分子机制
doi:10.1038/s41586-019-0888-x
干细胞是我们身体的“万能钥匙”,因为其能转化为所有器官中许多不同类型的细胞,其能够帮助肌肉(甚至是大脑)等组织不断更新并进行损伤后愈合,这种神奇的多潜能性使得干细胞有望成为未来科学家们开发再生医学疗法的关键工具,近日,一项刊登在国际杂志Nature上的研究报告中,来自德国癌症研究中心的科学家们通过研究阐明了大脑干细胞如何制定决策转化成为新型神经细胞。

图片来源:CC0 Public Domain
研究者Ana Martin-Villalba及其同事一直在沿着通往神经元细胞的路径来追踪干细胞的行为,他们追踪了每一个阶段基因的表达情况,并分析了哪些基因会进行表达并翻译成新型蛋白,研究者发现,干细胞只需要完全关闭干细胞的基因就能转变成为神经元细胞,但事实证明这一过程非常复杂,干细胞的基因并没有完全关闭,而是处于待命状态,即通过抑制制造使其处于细胞多潜能性的蛋白产物来实现这一状态。
研究者Ana Martin-Villalba说道,当其处于“待机”模式时,干细胞就开始了转变成为神经元的旅程,其会关闭内在的增殖信号(TOR)并开始停止分裂,让研究人员非常好奇的是,他们还发现,干细胞总是会购买一张“返程票”,就好像在不同国家之间来回飞行的航班一样,开启或关闭TOR信号就能促进细胞在干细胞和神经元细胞之间来回往返,因此,干细胞转变成为神经元的决定在一段时间内是可逆的。
6.Cell Stem Cell:重大进展!将人成熟的血细胞直接重编程为一类新的神经干细胞
doi:10.1016/j.stem.2018.11.015
在一项新的研究中,来自德国癌症研究中心(DKFZ)和海德堡干细胞技术与实验医学研究所(HI-STEM)的研究人员首次成功地将人血细胞直接重新编程为一种以前未知的神经干细胞。这些诱导性干细胞类似于在中枢神经系统的早期胚胎发育期间形成的干细胞。它们能够在实验室中进行修饰和无限期地增殖,并且代表着一种用于再生疗法开发的候选对象。相关研究结果于2018年12月20日在线发表在Cell Stem Cell期刊上,论文标题为“Identification of Embryonic Neural Plate Border Stem Cells and Their Generation by Direct Reprogramming from Adult Human Blood Cells”。论文通讯作者为Andreas Trumpp和Marc ChristianThier。
Trumpp团队首次成功地将成熟的人细胞重编程为一种特定类型的能够几乎无限增殖的诱导性神经干细胞,他们称之为诱导性神经板边界干细胞(induced neural plate border stem cell, iNBSC)。Thier解释道,“像日本科学家Shinya Yamanaka样,我们使用了4种遗传因子,不过使用了4种不同的遗传因子用于我们的重编程中。我们认为,我们的遗传因子将允许重编程到神经系统发育的早期阶段。”
这些iNBSC具有广泛的发育潜力。iNBSC具有增殖能力和多能性,能够朝两个方向进行发育。一方面,它们能够选择产生中枢神经系统中的成熟的神经细胞和神经胶质细胞的发育途径。另一方面,它们也能够发育成神经嵴细胞,这些神经嵴细胞产生不同的细胞类型,比如周围敏感性的神经元,颅骨的软骨细胞或骨细胞。
7.Stem Cell Rep:重磅!科学家鉴别出决定细胞命运的干细胞特性
doi:10.1016/j.stemcr.2018.08.011
近日,一项刊登在国际杂志Stem Cell Reports上的研究报告中,来自加利福尼亚大学的科学家们通过研究鉴别出了能够影响神经干细胞命运的固有细胞特性,这些特性或许会影响神经干细胞分化称为哪种脑细胞,比如神经元、星形细胞和少突神经胶质细胞等,相关研究结果或能帮助研究人员开发出新方法来预测或控制干细胞的命运,从而更好地应用于人类的移植治疗中。

图片来自Cell Stem Cell, doi:10.1016/j.stem.2018.11.015。
研究者Lisa A. Flanagan教授表示,神经干细胞常常会因细胞表面表达不同的糖类模式而表现出不同的的命运,这些糖类分子会促进神经干细胞膜的电位特性并最终决定其细胞命运;干细胞能够帮助治疗多种人类疾病,但研究人员却很难确定当这些干细胞被移植到患者机体中后其会转变成为什么细胞类型。当研究者将相同数量的干细胞分别移植到两名患者机体中后,如果干细胞在其中一名患者体内分化称为神经元,而在另一位患者机体中分化为星形细胞后,这两位患者最后的治疗情况会发生明显差异;基于当前研究结果,研究人员就能够预测神经干细胞的分化终点以及其可能的细胞命运,这或许能够增强干细胞移植疗法治疗多种类型疾病的成功率。
这项研究中,研究人员检测了几种给细胞表面添加糖类分子的通路,结果发现了一种通路能够帮助制造神经元,而另一种通路则能够帮助制造星形细胞,研究人员通过刺激神经干细胞通路,改变细胞电位特性,从而就能够制造更多的星形细胞和较少的神经元细胞这就表明,细胞表面的糖类分子能够控制神经干细胞的命运。(生物谷 Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


