Cell:怀孕会导致母体肠道的永久性扩张
来源:生物世界 2025-04-04 11:05
在这项新研究中,研究团队利用现代遗传工具重新审视并深入探究小鼠肠道的生殖性生长情况,描述了其细胞特征,并揭示了潜在的分子变化和触发因素。
肠道是一个具有非凡可塑性的器官:其上皮组织是哺乳动物中自我更新速度最快的组织。在小肠中,位于隐窝内的增殖细胞分化为细胞,这些细胞向上迁移至绒毛,并分化为肠道上皮细胞和分泌细胞类型,最终在绒毛顶端发生凋亡。
尽管活跃循环的隐窝细胞之间的确切谱系关系仍处于积极研究之中,但位于隐窝底部的 Lgr5 阳性隐窝基底柱状细胞和位于隐窝底部及两侧的 Fgfbp1 阳性峡部祖细胞均能增殖,并可分化为多种肠细胞类型。我们对诸如肠道等器官的可塑性大部分理解都源自对组织损伤、营养缺乏/过剩或微生物群减少所引发反应的研究。令人感到矛盾的是,从历史上看,我们一直忽视了成年器官生长的最具生理相关性的环境之一:生殖。
早在 1939 年,科学家就提出了母体肠道及其他器官的生殖性生长这一观点,此后的研究证实其涉及肠道长度的增加以及吸收面积的扩大。然后,这背后的机制尚不清楚。
英国弗朗西斯·克里克研究所的研究人员在国际顶尖学术期刊 Cell 上发表了题为:Growth of the maternal intestine during reproduction 的研究论文。
该研究发现,怀孕会增加雌性小鼠的小肠和肠道绒毛的长度,以增强母鼠和幼鼠的营养吸收,且小肠长度的增加不可逆。该研究进一步揭示了基因和代谢变化推动了这一过程,其中关键转运蛋白 SGLT3a 发挥了重要作用。令人惊讶的是,即使在没有怀孕的情况下,仅仅是钠离子(食盐)也能引发类似的肠道扩增。

该团队此前已证明,母体肠道的重塑并非哺乳动物所独有。实际上,卵生的果蝇(雌雄肠道存在差异)在雌性生殖期间,其肠道会生长并发生代谢重塑。他们还证明,肠道生长具有可预见性并且受基因控制。此外,生殖期间的肠道生长需要增加营养摄入,但并非被动地由这些因素导致。
在这项新研究中,研究团队利用现代遗传工具重新审视并深入探究小鼠肠道的生殖性生长情况,描述了其细胞特征,并揭示了潜在的分子变化和触发因素。
肠道如何为怀孕做准备?
研究团队在此行小鼠中发现,在妊娠第 7 天,就出现了肠道肠道的增加,并在哺乳期达到峰值。其中,小肠的总长度增加了 18%,肠道绒毛增加了 30%。而且,这些变化在产后并没有得到完全恢复,小肠的长度的增加不可逆,且第二次妊娠期小肠的长度增加的更多了,而肠道绒毛则在产后得到了完全逆转,且在第二次妊娠期没有进一步增加。
此外,该研究还发现,妊娠期间,肠道干细胞的增殖提速,新生细胞在绒毛中的迁移速度也更快了。
对无菌小鼠以及高脂、高糖喂养小鼠的研究显示,这种肠道生长与饮食和肠道菌群变化无关,显示出独特的妊娠特征。而且,这种肠道生长早于食欲增长,在小鼠妊娠中后期食欲增长前就已完成肠道的生长。
研究团队认为,肠道长度和绒毛的增加,可能有助于增加母体以及后代在妊娠期间所需的营养吸收。
转运蛋白 SGLT3a 发挥关键作用
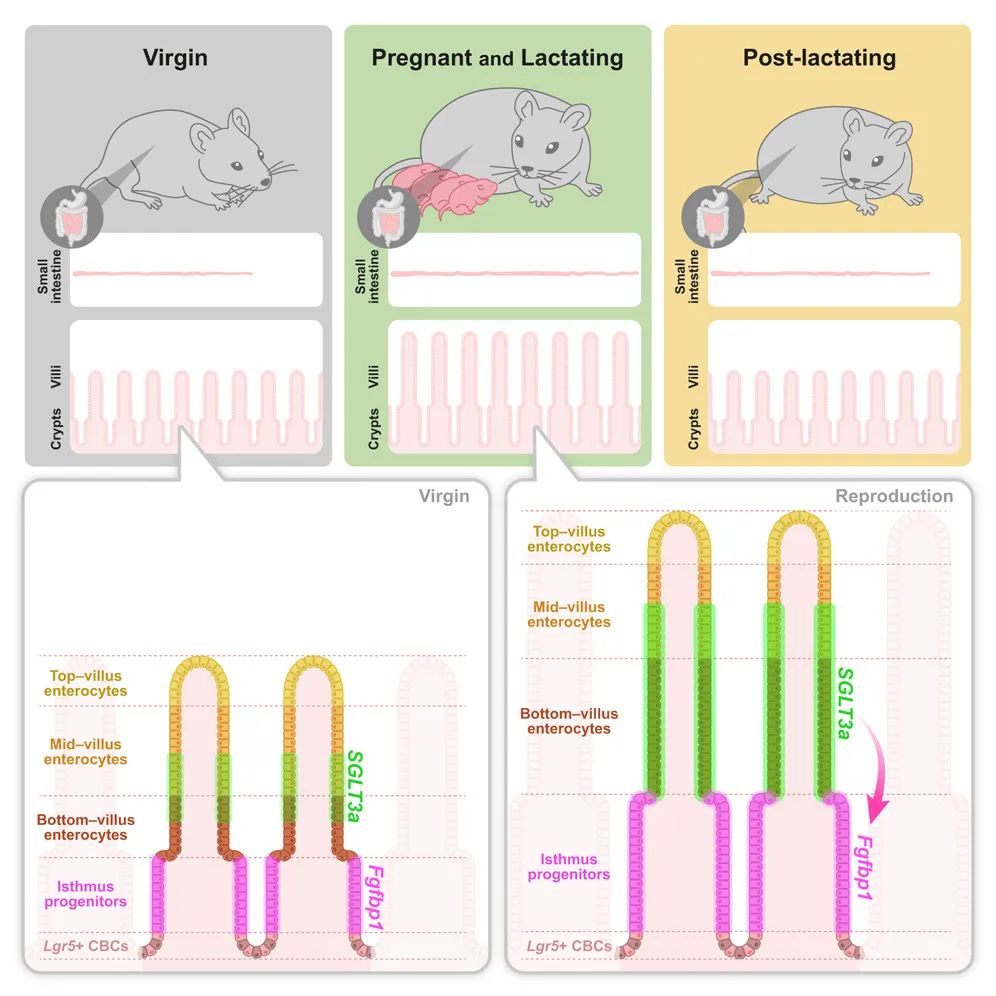
研究团队进一步发现,定位于绒毛中下部肠道细胞的转运蛋白 SGLT3a 的表达量在妊娠期间激增 5 倍,电生理学和遗传学研究显示,SGLT3a 并不维持消化功能或肠道上皮细胞健康;相反,它感应钠离子和 pH 变化,通过局部离子环境变化调控临近干细胞,促进 Fgfbp1+ 峡部祖细胞的增殖,从而促进绒毛生长。
这些发现可能解释了人类妊娠期对咸味食物的特殊偏好,从进化角度来看,远古时期盐分摄入或助力母体应对生殖压力。这些发现也为产后肥胖带来了新见解——妊娠期不可逆的肠道生长可能是导致产后体重难以下降的原因。
该研究的核心发现:
妊娠期母体肠道的重塑具有独特且具有可预见性的特征;
肠道长度的生长是不可逆的,而绒毛的生长则是完全可逆的;
钠离子和质子敏感的 SGLT3a 转运蛋白在妊娠期肠上皮细胞中被诱导表达;
SGLT3a 从外部维持着 Fgfbp1+ 峡部祖细胞的扩增和绒毛的生长。
总的来说,这项研究:
重新定义了器官可塑性:揭示了生殖特异性生长程序的存在;
开辟了代谢调控新维度:发现钠离子作为生长信号的全新角色;
改写了消化生理学:首次证实了非营养物质的器官重塑功能。
研究团队建议,可以利用器官和组织特异性的生长方案来改善妊娠结局或预防此类生长带来的不良后果。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


