Cell:科学家揭示一种癌细胞免疫逃逸的新型分子机制
来源:生物谷原创 2024-11-23 14:03
本文研究揭示了IRGQ或能作为MHC-I质量控制的调节子,从而就能介导机体中肿瘤的免疫逃逸过程。
自噬—溶酶体系统(autophagy-lysosome system)能指导多种货物的降解,同时也参与到了肿瘤的进展过程中。近日,一篇发表在国际杂志Cell上题为“IRGQ-mediated autophagy in MHC class I quality control promotes tumor immune evasion”的研究报告中,来自法兰克福大学等机构的科学家们通过研究识别出了一种能监测MHC-I分子质量的细胞内传感器,MHC-I分子能帮助免疫系统识别并杀灭有害细胞(包括肿瘤细胞),这种传感器能确保缺陷的MHC-I分子留在细胞内,并最终在细胞内被降解。让研究人员惊讶的是,缺乏这种质量保证体系或会导致更多的MHC-I分子抵达癌细胞表面,从而引发抵御肿瘤更强烈的免疫反应。
判断一个细胞的健康状况相对容易,在细胞表面,细胞会展示出其所包含的几乎所有的蛋白片段,这意味着免疫系统能直接识别细胞是否被病毒感染或者被突变危险地改变;无数的分子无线杆(radio masts),即MHC-I分子主要负责呈递这些片段,其能在细胞内被组装随后被运输到细胞膜上,即细胞周围的脂质层。在这里,无线杆会被锚定,这样货物就会面向外部,从而就能被免疫系统不断巡逻的部队检测到,如果这些细胞能检测到MHC-I无线杆上的有害分子,其就会杀死相关细胞,然而,有一个要求就是无线杆本身要功能完整,否则这一机制就无法发挥作用,且有害分子会逃离宿主机体的免疫系统。
Lina Herhaus博士解释道,如今我们在细胞内发现能一种传感器,其能确保只有功能性的MHC-I分子能被运输到质膜上,而有缺陷的单元则会被消除。细胞会不断产生大量的蛋白质来维持其发挥的多种功能,如果在这一过程中出错的话,受影响的分子通常就会被消除,特殊的受体就会识别有缺陷的蛋白质,并将其运输到迷你垃圾袋中,并在那里将其分解。作为研究的一部分,如今研究人员找到了位置功能的受体并发现了一种名为IRGQ的蛋白质,该蛋白专门负责确保MHC-I无线杆的质量控制。
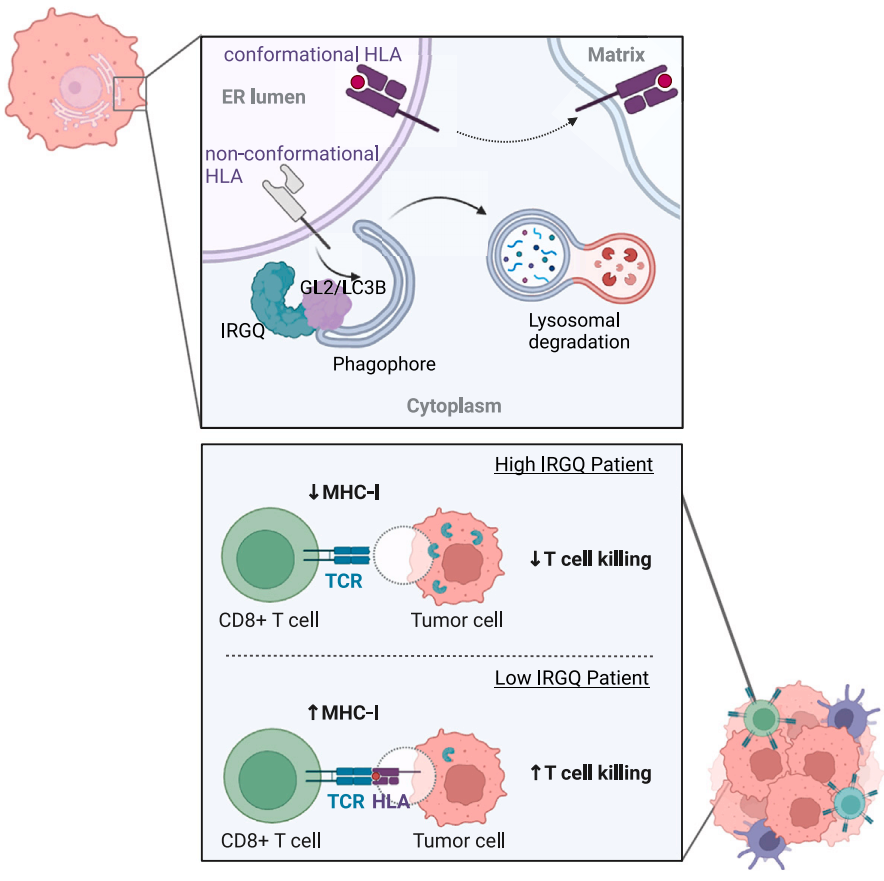
全文的图形摘要
研究人员利用遗传干扰的方式抑制了IRGQ的产生,结果发现,有缺陷的“无线杆”会在细胞中积累,其中一些也会与它们的功能对应物一起被掺入到细胞膜中。研究者解释道,实际上并不携带IRGQ的细胞会诱发微弱的免疫反应,然而,事实显然并非如此,当分析了多种人类肿瘤组织后,研究者发现,较少的IRGQ与肝癌患者较高的存活率有关。
此外,患者的数据也在实验性的肝癌小鼠模型中得到了证实,即在没有IRGQ的动物中,其机体的免疫系统会更加猛烈地攻击肿瘤细胞,结果发现,不携带IRGQ的啮齿类动物的存活时间明显更长。IRGQ能代表新药的靶向结构,至少对于肝细胞癌是这样,肝细胞癌是世界上第二大致死性的癌症类型,如今研究人员发现了肿瘤细胞躲避免疫系统攻击的新型分子机制,未来研究中,他们还将分析IRGQ对其它类型癌症的影响。本文研究发现或有望帮助未来开发治疗人类肝癌的新型疗法,其中一个案例就是利用药物来靶向降解IRGQ分子,从而刺激机体抵御癌症的免疫反应。
尽管如此,研究人员发现的新机制对于基础研究而言也是非常新颖的,如今他们想通过进一步研究阐明IRGQ对于免疫系统的重要性,包括在病毒感染期间;本文的研究结果也提出了一系列有意思的问题,回答这些问题或能加深科学家们对机体免疫防御机制的理解。综上,本文研究揭示了IRGQ或能作为MHC-I质量控制的调节子,从而就能介导机体中肿瘤的免疫逃逸过程。(生物谷Bioon.com)
参考文献:
Lina Herhaus, Uxía Gestal-Mato, Vinay V Eapen, et al. IRGQ-mediated autophagy in MHC class I quality control promotes tumor immune evasion, Cell (2024). DOI:10.1016/j.cell.2024.09.048.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


