Nature重磅:首次在活体动物中实现对肠道细菌的原位、精准基因编辑
来源:生物世界 2024-07-13 09:47
研究证明了直接在活体动物肠道中对细菌进行精准基因编辑的可行性,为研究细菌基因的功能提供了新途径,并为设计新的微生物组靶向疗法打开了大门。
基因编辑公司 Eligo Bioscience 的研究人员在国际顶尖学术期刊 Nature 上发表了题为:In situ targeted base editing of bacteria in the mouse gut 的研究论文。
该研究开发了工程改造的λ噬菌体,利用噬菌体诱导染色体岛(phage-inducible chromosomal island,PICI)复制机制的DNA有效载荷,递送碱基编辑器,首次实现了在活体小鼠体内对肠道细菌的高效、精准基因编辑,且能够避免递送进体内的DNA有效载荷的复制和传播。
该研究开发的碱基编辑系统代表了体内原位编辑细菌的工具的关键性飞跃,开启了编辑微生物以对抗疾病的可能性。

在这项最新研究中,研究团队提出了一种对目标肠道菌群进行原位、精确且稳定的基因修饰策略。
要想在复杂的肠道环境中实现这一目标,需要高效的DNA递送与有效的靶向诱变策略相结合。研究团队探索了将噬菌体来源的颗粒(phage-derived particles)用作递送载体,并与碱基编辑器(base editor)相结合。碱基编辑器能够在不产生DNA双链断裂的情况下,在目标位点将一个碱基对转换为另一个碱基对,并且已在包括广泛的细菌物种在内的各种生物中成功应用。
此前已有多项研究探索了向目标细菌递送CRISPR - Cas系统,这些研究使用了多种递送模式,包括供体细菌的质粒与目标菌株的结合、包装到噬菌体衣壳中的质粒的转导,或者将CRISPR-Cas系统添加到噬菌体基因组中。由于噬菌体DNA递送效率高,它们成为一种有吸引力的载体选择。当目标是只编辑而不杀死细菌时,就不能使用裂解性噬菌体,而是使用噬菌粒或温和噬菌体。
此前向小鼠肠道中大肠杆菌进行DNA递送的研究,要么依赖于M13噬菌粒,要么依赖于基因修饰的λ噬菌体。M13噬菌粒以F菌毛作为受体,这限制了其范围,并且M13在通过小鼠胃肠道时不稳定。而λ噬菌体,在感染大肠杆菌时,λ要么进入裂解周期并产生更多的病毒颗粒,要么进入溶原化并整合到染色体中(从而能够维持递送的诸如I型 CRISPR–Cas系统或dCas9等转基因)。最近还有研究在λ噬菌体基因组中引入了碱基编辑器,尽管其能够在肠道环境中繁殖,但λ噬菌体无法使整个目标群体溶原化。
为了提高肠道环境中的递送效率,研究团队设计了λ噬菌体尾部的多个嵌合变体以靶向不同的受体。
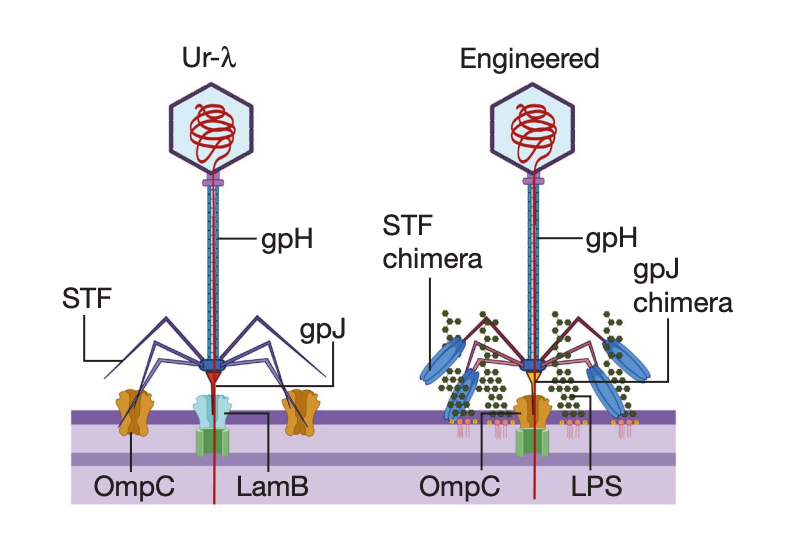
原位靶向诱变策略的另一个理想特征是它不会进一步传播递送进去的转基因。为实现这一目标,研究团队开发了一种利用噬菌体诱导染色体岛(phage-inducible chromosomal island,PICI)复制机制的DNA有效载荷。这一设计能够确保所递送的DNA在受体细菌中不会复制,同时仍能有效表达碱基编辑器。这种策略能够在无需选择压力或维持转基因的情况下,为定植在小鼠肠道中的大多数大肠杆菌群体引入稳定的遗传扰动。
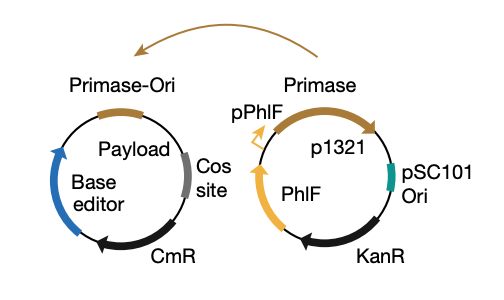
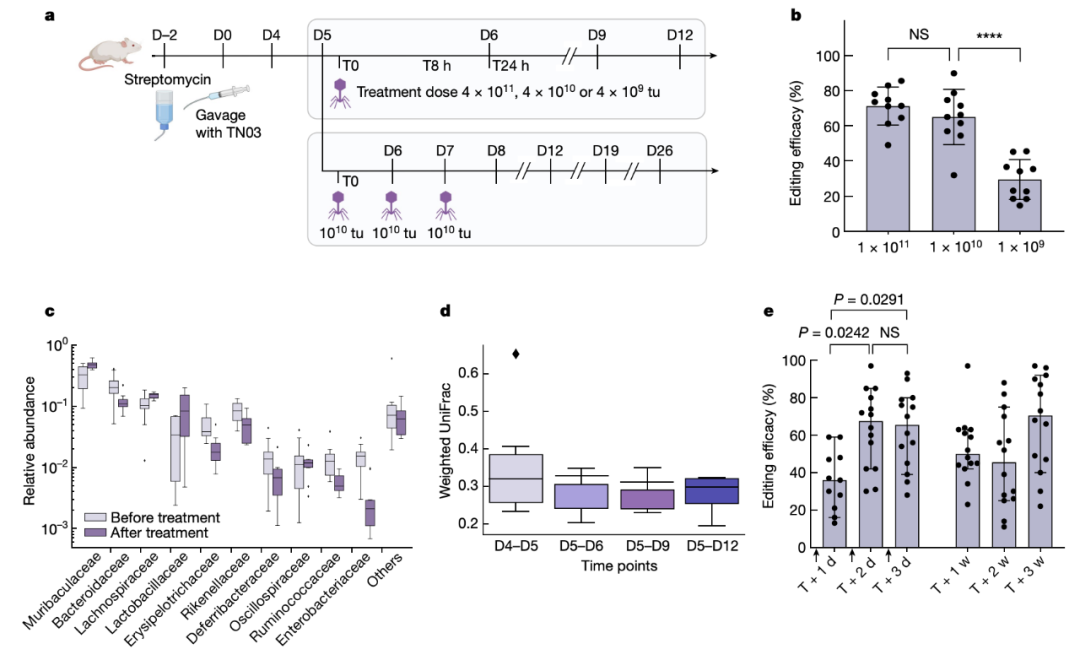
具体来说,该研究设计了一种噬菌体来源的颗粒,用于递送碱基编辑器,并对定植于小鼠肠道中的大肠杆菌的β-内酰胺酶基因(该酶能够水解青霉素等抗生素,帮助细菌抵抗抗生素)进行基因编辑。实验结果显示,单次编辑使目标细菌群体的中位编辑效率达到 93%,编辑后的大肠杆菌在小鼠肠道中稳定维持至少42天。此外,由于该研究使用了非复制型DNA载体,防止了有效载荷的维持和传播。
然后,研究团队利用这种方法在体外成功对大肠杆菌和肺炎克雷伯菌菌株中的几个治疗相关基因进行碱基编辑,并证明了该方法可在体内原位编辑致病性大肠杆菌参与卷曲菌毛(curli,其与多种神经退行性疾病和自身免疫病相关)产生的基因,编辑效率约为70%。
总的来说,这项研究证明了直接在活体动物肠道中对细菌进行精准基因编辑的可行性,为研究细菌基因的功能提供了新途径,并为设计新的微生物组靶向疗法打开了大门。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


